En la época actual el pilar diagnóstico lo constituye la endoscopia digestiva, ya que ella nos permite ver la lesión, tomar muestras para estudio anatomopatológico y da una idea del problema, pudiendo clasificar lo examinado en cualesquiera de los tipos propuestos por Murakami (3, 12, 21, 22). La anatomía patológica es la que nos dirá si es o no cáncer, nos determinará la profundidad y por lo anterior es vital en la elaboración de un pronóstico.
La radiología ha sido utilizada como un método primario de estudio por algunos grupos japoneses, pero su papel primordial se ha enfocado hacia los programas de examen masivo, siendo para los que lo usan el primer paso en el estudio de pacientes sospechosos, mediante la realización de la llamada fotofluorografía (radiología indirecta), en busca de lesiones o alteraciones del contorno gástrico, clasificando así a los pacientes y llevando a los positivos a la endoscopia y a los demás estudios, a fin de descartar o aÍrrmar la presencia de un cl\fcinoma (3, 12, 28). El grupo de Fukuoka en Japón liderado por Hideyatsu Kiyonari, jefe de radiología en Kiushu (Japón), tiene el diagnóstico radiológico en un alto concepto, y ellos con una metodología adecuada dentro de la que se debe nombrar e11lenamiento, la compresión y el doble contraste, detectan lesiones cancerosas y las clasifican incluso en profundidad de acuerdo con la concentración del bario, lo que establece una buena correlación con la endoscopia (29).
Endoscopicamente podemos definir casi con seguridad si una lesión es o no un cáncer gástrico de tipo temprano.
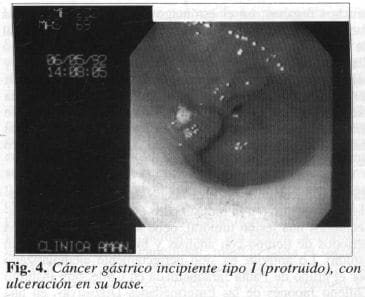
El cáncer temprano de tipo I (protruido) es una lesión que sobresale claramente de la mucosa que la rodea. Esta es una lesión protruida y muchas veces su superficie está ulcerada, se cubre de fibrina o sangra fácilmente (3). La mucosa de alrededor es normal (Fig. 4).
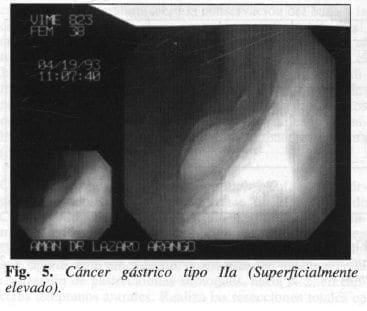
El cáncer gástrico tipo lIa (superficialmente elevado), es una lesión que plantea problemas diagnósticos diferenciales con el adenoma (atipia 3 o lesión border fine). Esta lesión sobresale un poco de la mucosa de alrededor, es de color más pálido que la mucosa que la rodea; a veces se erosiona y por lo general y, a diferencia del adenoma, es mayor de 20 mm (3, 12) (Fig. 5).
El cáncer gástrico tipo IIb, es el menos frecuente; además hay que considerarlo como un hallazgQ del patólogo; es muy difícil endoscópicamente determinar dónde se encuentra y se define como un área más pálida o más enrojecida o como una zona de petequias alrededor de una mucosa normal.
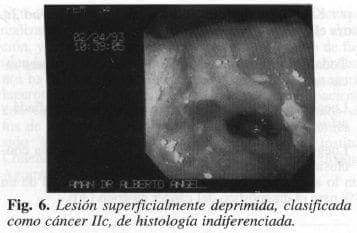
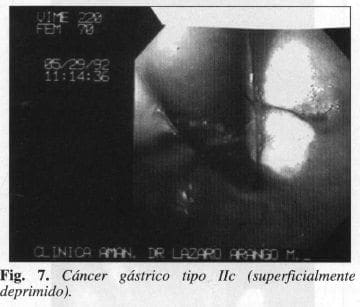
El cáncer gástrico tipo Hc (superficialmente deprimido), es el más frecuente; su patología es casi siempre indiferenciada, se distingue por ser una depresión en medio de una mucosa normal. Esta depresión tiene unos bordes Irregulares como si éstos hubieran sido cortados a pico, y a ella confluyen pliegues que se alteran antes de llegar, sufriendo cuatro alteraciones posibles, a saber: el aguz ento, el ensanchamiento, la amputación y la fusión o confluencia (Figs. 6 y 7).
 |
 |
Muchas veces la lesión anterior presenta en medio de ella un área de mucosa gástrica normal, que se ha denominado “Isla” (3, 12, 27). El cáncer temprano de tipo III o excavado es muy importante ya que debe diferenciarse de la úlcera gástrica; allí es donde debemos poner mayor atención sobre todo en la toma de las biopsias. Si en una endoscopia se accede a una úlcera ligerament~, podría dejarse sin diagnosticar un cáncer temprano de tipo III.
En un estudio multicéntrico de 22 instituciones hecho en Japón por T. Hayashida y col, y publicado en el libro Diagnóstico de las Afecciones Gástricas en Chile en el año de 1987, se muestra la’ frecuencia de los diferentestipos de cáncer temprano del estómago sobre un total de 2.364 pacientes, encontrándose que el más frecuente es el Hc con un 33.8%, seguido por el Hc + III con un 23.4%. Lo anterior es similar a los informes de otros autores.
Por lo tanto, la endoscopia es de vital importancia para el diagnóstico del cáncer temprano. La metodología propuesta por Kiyonari (30), habla del Sistema de Seguridad Japonés el cual consta de varios niveles:
1. Toda lesión sospechosa debe ser fotografiada, para sacar una conclusión.
2. Luego, debe ser coloreada y nuevamente fotografiada y así sacar otra conclusión (Fig. 8).
3. Luego, debe ser biopsiada’y así sacar una nueva conclusión. Con lo anterior debe darse un margen de seguridad de un 98% para el diagnóstico del cáncer gástrico (30).
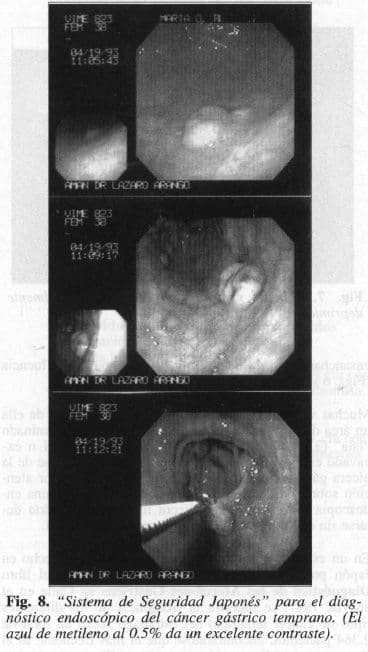
Con la endoscopia podemos realizar coloraciones que nos permiten visualizar por medio de un mejor contraste lesiones pequeñas hasta de 2 mm, que de otra forma sería difícil detectarlas. Estas coloraciones han sido utilizadas en muchos órganos; en el estómago los primeros en usarlas fueron Tsuda y Aoki. Las soluciones utilizadas son el azul de metileno al 0.5%, el azul de Evans al 1% Y el Indigo Carmín. En nuestro hospital y por mayor disponibilidad y bajo precio usamos el primero, que llena los requisitos de ser de fácil disolución, sin efectos colaterales, proporciona excelente contraste y no altera el área lesionada. Con lo anterior hemos podido estudiar en forma detenida muchas lesiones y ha aumentado en forma importante el número de lesiones tumorales encontradas.
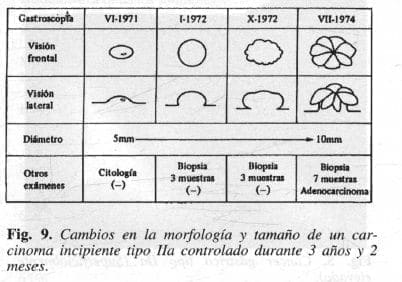
Hay que hacer énfasis en el hecho de que cuando un paciente es negativo á la biopsia pero endoscópicamente sospechamos una lesión tumoral, debe ser seguido por largos períodos de tiempo con análisis y biopsia de la lesión en estudio. Lo anterior ha sido perfectamente ejemplarizado por el grupo de Paula Jaraquemada en Chile, hoy Instituto Chileno Japonés de las Enfermedades Digestivas, en una paciente con una lesión elevada seguida por 3 años y 2 meses, con cuatro endoscopias realizadas en dicho lapso, observándose los cambios de aquella, hasta llegar a detectar el carcinoma (Fig. 9). Es importante anotar que con un número de biopsias superior a 8 se puede diagnosticar con mayor seguridad un cáncer gástrico (25).
La citología y la aspiración con aguja fina no han encontrado todavía un lugar en el estudio de estos pacientes y su utilidad parece estar sólo destinada al diagnóstico del linfoma gástrico.
Tratamiento
El tratamiento definitivo del cáncer es y debe ser quirúrgico. Las resecciones por realizar, pensamos que deben ser las radicales. Pero creemos que este aserto amerita un capítulo diferente de discusión, por lo que sólo mostraremos las conductas por nosotros adoptadas sin plantear puntos de ia controversia existente en el mundo alrededor del tema.
En el Hospital de Caldas nos regimos actualmente por lo dispuesto en el encuentro nacional de Betania, en Neiva. Somos muy amigos de realizar gastrectomías subtotales en cánceres antrales o pilóricos y en esto diferimos de algunos grupos chilenos que prefieren la gastrectomía total, con el argumento de que es frecuente encontrar cánceres multicéntricos. El anterior concepto es apoyado por la literatura, en la cual podemos analizar informes americanos, europeos y japoneses, que muestran una baja recurrencia en pacientes sometidos a gastrectomía subtotal y excelente supervivencia (8). Pensamos que la cirugía gástrica por sí misma deja algunos inválidos digestivos y crea efectos secundarios indeseables, que pueden minimizarse, desde el punto de vista del órgano, mediante la realización de cirugías menos radicales, siempre que sea posible acompañarlas de una resección ganglionar, mínimo hasta el segundo nivel (N 2), lo que es mundialmente aceptado como cirugía curativa en pacientes con cáncer gástrico temprano. En este tipo de cáncer se ha considerado un margen adecuado de la lesión entre 2 y 3 cm (8, 10, 12, 19), siendo así el muñón gástrico libre de lesión tumoral en el 90% de los casos. Cuando el margen está cerca al cardias o la lesión es fúndica o se localiza en la curva mayor del cuerpo o cuando compromete el área de pliegues, realizamos gastrectornías totales con un vaciamiento ganglionar hasta la segunda barrera (N 2). En los últimos años han aparecido estudios en la literatura sobre la conservación del bazo y la cola del páncreas aun en pacientes con gastrectomía total, cuando los ganglios no estén comprometidos o cuando el tumor no es próximo a estos órganos. Suehiro y col, en el Japón, muestran cómo en el cáncer avanzado no hubo diferencias entre los pacientes a los que se les realizó esplenectornía y aquellos a quienes no se les hizo, pero para los de tipo temprano el pronóstico fue peor en quienes se realizó (31). Lo mismo puede decirse de la pancreatectomía (32).
Creemos que mucha de nuestra política y enfoque quirúrgico del problema, puede sintetizarse en el artículo de Csendes, Cáncer Gástrico, Estado Actual de su Tratamiento y Resultados a Largo Plazo, que ha aparecido en la Revista Chilena de Cirugía en septiembre de 1992, en el que, aparte de lo antes dicho, concuerda con nosotros en la realización de gastrectomías subtotales, hasta N 2, en cánceres tempranos antrales. Realiza las resecciones totales en iguales circunstancias a las nombradas y preserva en lo posible el bazo y el páncreas. En su análisis, al igual que en el nuestro, la cirugía del cáncer gástrico ofrece en la actualidad mejores resultados inmediatos, debido a un mejor manejo nutricional, a la realización de cirugías meticulosas, al uso de drenajes, al reposo esofagoyeyunal prolongado (10 días) para los pacientes sometidos a gastrectomía total, al apoyo respiratorio y a la disponibilidad de nutrición parenteral o enteral, según el caso (33). Así mismo, veta la gastrectomía proximal como tratamiento del cáncer, por la alta incidencia de gastritis por reflujo alcalino y por la aparición de un número elevado de fístulas (9, 10, 33), concepto que compartimos firmemente, agregándole a lo dicho que con este procedimiento queda muy difícil realizar una adecuada resección ganglionar.
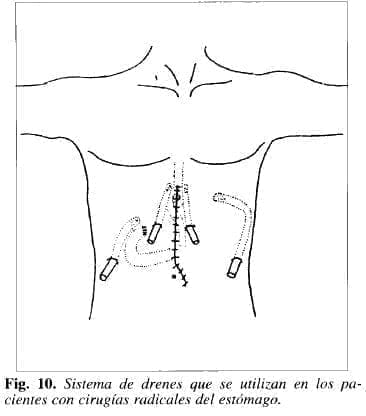
A todo lo anterior, nosotros agregamos drenes cuando realizamos la cirugía radical, observando una mejor evolución, ya que en pacientes que presentan algún tipo de fuga (duodenal o de la esofagoyeyunostomía), esta conducta nos ha evitado en la mayoría de los casos ir a una segunda laparotomía. Así hemos bajado la mortalidad en pacientes con esofagoyeyunostomía, evaluando los resultados con los de los colegas escépticos del drenaje. Esta política ha sido adoptada por los grupos chilenos del Instituto Chileno-Japonés y del grupo del Hospital José Joaquín Aguirre, en Santiago (33) (Fig. 10).
Al tratamiento quirúrgico agregamos quimioterapia gracias a la colaboración del doctor Hemán Daría Salazar y su grupo. Los resultados de ésta apenas podrán evaluarse con el tiempo; nuestros pacientes son seguidos en una consulta hecha en conjunto con los residentes de cirugía general. Hasta el momento estamos muy satisfechos de los resultados, ya que llevamos 2 años con la política quirúrgica descrita y tenemos pacientes vivos de diferentes estadios, incluyendo al estadio IV. Hemos estudiado el trabajo de Juan M. Vanegas realizado en el año de 1987 (35), en el cual revisó la sobrevida de los pacientes con cáncer del estómago tratados en nuestro hospital en 10 años, y realmente los resultados no eran alentadores. Con el autor mencionado concluimos que sólo con programas de búsqueda se puede lograr el objetivo de aumentar la supervivencia al detectarlos en estadios tempranos.
Exámenes Masivos para Detección del Cáncer Temprano o Incipiente
En nuestros países latinoamericanos, los exámenes masivos son los que van a marcar el futuro y alcanzar mejores pronósticos. Nada se gana con llenar protocolos de cánceres que llegan en estadios III y IV, Y cuya sobrevida en años será corta. Por lo tanto, y alentados por la idea de aportar algo, iniciamos en julio del año de 1992, un ambicioso programa de detección de enfermedades gastrointestinales incluyendo el cáncer gástrico. Este es un programa pequeño, realizado sólo en el Departamento de Caldas, apoyado por el doctor Pedro Llorens y su Instituto. Este apoyo es dado en capacitación a personal, habiendo desplazado 8 profesionales a Chile en diferentes épocas y de distintas especialidades, en desarrollo del concepto que rige el trabajo multidisciplinario.
Este programa se desplaza a 3 pueblos (Manzanares-Aranzazu- Salamina), que en el año de 1987 fueron detectados por Salazar y col, sólo con endoscopia, sustentados por los resultados de algunos grupos japoneses que no utilizan la radiología y han encontrado que el tamizado o selección (screenings) con este método únicamente, es excelente y disminuye costos (28). Así mismo, nos apoyamos en los resultados obtenidos en el Japón y especialmente en Chile (3), un país como el nuestro, que ha contado con la ayuda de la nCA en su dotación tecnológica representada en técnicos y especialistas, para la realización de un programa ambicioso que pudo examinar más de 50.000 personas en 4 años, mediante la combinación de la radiología y la endoscopia.
Nosotros hemos iniciado el programa adjunto a IDAQUIPE (órgano de extensión de la Universidad de Caldas), y que está conformada por el Comité Departamental de Cafeteros, quien donó los endoscopios; la Universidad de Caldas, el Servicio de Salud de Caldas y el Hospital de Caldas, quienes donaron nuestros tiempos de trabajo en los días de desplazamiento y han facilitado el transporte y la difusión del programa. A los anteriores se unieron el Banco Cafetero con publicidad, y los Laboratorios Bussié con interés en la investigación alterna de enfermedades benignas, por medio de la “Fundación Poli carpo Bustillo Sierra”.
Así nació un programa que se desplaza los días viernes a diferentes pueblos y que durante la semana se realiza en el Hospital de Caldas con pacientes de otras áreas y de la capital del Departamento. Nuestra base es la endoscopia digestiva con la metodología de seguridad empleada por los japoneses. Hemos adiestrado al personal rural para el empadronamiento de los pacientes y realizamos el estudio en sintomáticos de cualquier edad y en personas mayores de 35 años que quieran someterse al mismo. Tomamos las biopsias que son leídas por los patólogos de nuestro Hospital y cuando el paciente es positivo para cáncer lo ingresamos al programa de la Fundación y se realiza el tratamiento quirúrgico a cargo de cualquiera de los docentes de nuestro Servicio. El programa es excelente a pesar del poco tiempo que lleva y de hallarse en el período de ajustes tendientes a superar algunos problemas operativos; por estas razones no publicamos aún resultados, pero próximamente lo haremos cuando éstos por su número y tiempo de seguimiento, tengan alguna validez estadística. No sabemos si el número de cánceres tempranos que vamos a encontrar en un tiempo determinado justifique el esfuerzo y los costos del mismo, ni si éstos comparados con el beneficio del diagnostico de cáncer temprano, sean un dilema fácil de resolver en conciencia. Hasta el momento hemos aprendido mucho de la enfermedad benigna; en conjunto con los Laboratorios Bussié realizamos estudios de Helicobacter pyloris, con buenas enseñanzas. Hemos encontrado algunos cánceres tempranos, otros intermedios y muchos avanzados; creemos haberlos diagnosticado 1 año antes de que tales pacientes hubiesen consultado a un médico.
Nuestro programa tendiente a la detección del cáncer gástrico temprano, debe interpretarse como una colaboración de nuestro grupo médico al empeño de lograr algún día en nuestro medio, el propósito universal de diagnosticar el cáncer gástrico en su estadio inicial, condición básica para emprender un tratamiento efectivo.
Abstract
We present an update in early gastric cancer. This term was introduced to describe gastric cancer affecting gastric mucosa, mucosa and submucosa with or without cancer bearing adenopathies.
Establishing a correct diagnosis implies deep knowledge of the endoscopic and pathologic clasification according to Lauren and coworkers.
Early gastric cancer should be treated agressively with oncologic type operations improving the 5 and 10 year survival. the solution to this important health problem lies on early detection as has be en proven by the japanese and chilean groups.
At the Universidad de Caldas, the University Hospital of Caldas, the Comite Departamental de Cafeteros and the Health Service of Caldas, we are actually running a program of early detection of gastrointestinal diseases and gastric cancer in high risk areas. Our early results are reasuring.
Referencias
1. Hampson L G, Shennib H, Lough J O et al: Early Cancer Gastric: Is it a distinct clinical entity? Can J Surg 1990; 33: 349-52
2. Arango L et al : Conferencia, Programa Masivo de Detección de Enfermedades Gastrointestinales en Manizales (Caldas) Colombia. XII Curso de Avances en Gastroenterologia. Chile, Marzo 1993
3. Llorens P: Diangóstico de las afecciones Gástricas. Editorial de JICA. Segunda edición Chile 1987
4. Llorens P: Diagnóstico del Cáncer Gástrico y Terapéutica Endoscópica de las lesiones gástricas incipientes. Gastroenterol Latinoam 1991; 2 (2): 29-44
5. Nakamura H: Japanese Research Society for gastric cancer: The general rules for the gastric cancer study. II th edition; Tokyo, Kanehara Publ, Co, 1985
6. Lloren s P et al: Tratamiento del cáncer gástrico. Gastroenterol Latinoam 1991; 2 (1)
7. Hauser G: Das Chronische Mangengenchwur, sein verrnarbugs und des sen Beziehungerzur entearcklung des magen karcinoma . Leipzig, ICW Vogel, 1983
8. Farley D, Donohue J: Early Gastric Cancer. Surg Clin North Am 1992 Apr; 72 (2)
9. Watanabe H: Ulcera péptica. Diagnóstico de las afecciones gástricas. 2da Edición, Santiago JICA 1987; pp. 129-32
10. Maruyama H et al: Principios del tratamiento quirúrgico del cáncer gástrico. Artículo (Japón), 1980
11. Friesen G et al: Superficial carcinoma of stomach. Surgery 1962; 51: 300-12
12. Csendes A, Strauzer T: Tratamiento Quirúrgico del cáncer gástrico En: Cáncer gástrico Ira Edición. Santiago, Edit Andrés Bello, 1984
13. Nyhus LL: Cirugía Gástrica, En: El Dominio de la Cirugía. 2da Edición Edit Panamericana, 1984
14. Richard D: Tomours of the Stomach. Maingot’s Abdominal Operations. 9na Edición, USA, Appleton, 1990, pp. 679-99
15. Nakamura H: Histogénesis del cáncer gástrico. Etapas iniciales de su desarrollo. Gastroenterol Latinoam 1990; I (1): 71-90
16. Bragheto I et al: Gastritis Crónica. Metap1asia intestinal y displasia en pacientes portadores de dispepsia no ulcerosa según edad. Gastroenterol Latinoam 1991; 2 (1) 7-18
17. Jarvi O: Histogenesis of Gastric Cancer. XI Intemational Cancer Congress. Abstracts 1, Florence 105, 1974
18. Lauren P: The two histological main types of gastric carcinoma. Difusse and so called intestinal type carcinoma. An attempt at a histoclinical clasification. Acta Pathol Microbiol Immunol Scan 1965; 63: 31-49
19. Liévano G et al: Diagnóstico y manejo del cáncer gástrico. 2da Edición. Neiva, Láser Impresores, 1993 20. Watanabe H: Histopatología del Cáncer Incipiente. Diagnóstico de las Afecciones gástricas. 2da. Edición. Santiago, JICA 1987; pp. 75-7
21. Murakami T: Early Gastric Cancer. Japan J Cancer Res. Unicversity of Tokyo Press, 197 I
22. Murakami T: Phatomorfological Diagnosis. Definition and gros s clasiffication of early gastric cancer. Tokyo press, 1971
23. ILLorens P: Conceptos generales en endoscopia del carcinoma incipiente gástrico. Diagnóstico de las afecciones gástricas. 2da. Edición, Santiago, JICA, 1987
24. Craig D et al: Extended Lymph Node Dissection in Gastric Cancer. Surg Oncol Clin North Am 1993; 2 (3): 393-41 I CANCER INCIPIENTE DE ESTOMAGO
25. Mc Clelland D et al: Stomach and Duodenum. Select Read Gen Surg 1984; 3: 1-40
26. Mc Clelland D et al Stomach and Duodenum. Select Read Gen Surg 1989; 12: 1-30
27. LLorens P et al: Estudio del cáncer gástrico en Chile. En: Capítulos Escogidos en Gastroenterología. Ira Edición, Santiago. Publicaciones Técnicas Mediterráneo, 1990
28. Masakazu M et al: Review of Clinical Research in Gastroenterology. Ira Ed, Tokyo, Igaku-Shoin Ltda, 1988
29. Kiyonary H: Conceptos generales Radiológicos del carcinoma incipiente gástrico. Diagnóstico de las afecciones Gástricas. 2da. Edición, JICA, 1987
30. Kiyonari H: Diagnóstico Endoscópico del cáncer Gástrico. Conferencia, Santiago de Chile, marzo 1990
31. Suehiro S, Nagasue N, Ojama Y: The negative etIect of splenectomy on the prognosis of gastric cancer. Am J Surg 1984; 148: 645-8
32. Koga S, Koibura N, Kimura O: Prognostic significance of combines splenectomy or pancreatoesplenectomy in total and proximal gastrectomy for gastric cancer: Am J Surg 1981; 142: 546-50
33. Csendes A: Cáncer Gástrico. Estado actual de su tratamiento y resultados a largo plazo. Rev Chil Cirug 1992 (sept); 44 (3): 260-71
34. Arias J, Salazar F et al: Riesgo de padecer Cáncer Gástrico por vivir en determinada región del Departamento de Caldas. Monografía, Manizales, 1987
35. Venegas J M et al: Evaluación de factores pronósticos en pacientes con cáncer gástrico. Evaluación de 10 años de experiencia. Hosp Univ de Caldas.
Monografía, Manizales, 1987
