Presentación de 2 Casos y Revisión del Tema
J. C. MARIN, MD; M. OSORIO, MD; A. ARANGO, MD; A. ANGEL, MD, SCC; G. LOPEZ, MD; L. A. MEJIA, MD.
Palabras claves: Adenocarcinoma, Duodeno, Diagnóstico temprano, Tratamiento precoz.
Se informa sobre 2 casos de adenocarcinoma primario del duodeno tratados en el Hospital General Santa Sofía y el Hospital de Caldas, en la ciudad de Manizales, y se revisa la literatura mundial sobre el tema, recordando que el diagnóstico temprano es la clave del éxito en el tratamiento.
Introducción
Las neoplasias malignas del duodeno son difíciles de diagnosticar debido a la vaguedad de los síntomas, pero su detección temprana permite una resección con buena supervivencia. Los tumores duodenales fueron reconocidos por primera vez en 1655 (2). En 1746 se informó sobre el primer carcinoma duodenal (4); en 1929 Rankin y Mayo registraron 55 casos de cáncer del intestino delgado (1) y en 1932, en John Hopkins University, se describió una serie de 87 tumores del intestino delgado, de los cuales 4 (4.6%) eran malignos. Las neoplasias benignas tuvieron predilección por las últimas porciones del íleon, mientras que las malignas la tuvieron por las primeras porciones (duodeno y yeyuno) (1). Hasta 1942 Berger y Koppelman habían publicado 386 casos de adenocarcinoma del duodeno, de los cuales 19.9% eran supraampulares, 65% periampulares y 15% infraampulares. El primer caso de síndrome de Gardner fue informado en la literatura por Devic y Bussyen 1912(3).
Material y Métodos (Casuística)
Primer caso del Hosp. Gral. Santa Sofía
Paciente de 57 años, quien ingresó al hospital por un cuadro de 15 días de evolución, caracterizado por dolor abdominal, escleras ictéricas y coluria.
Hallazgos de laboratorio: Hb 12 gr/dL; leuc, 7.000/mL; albúm. 3.7 gr/dL; globulina, 3.4 gr/dL; creat. 0.3 mg/dL; bil. total, 6 mg/dL; bil. dir, 3.79 mg/dL; bil. indir, 2.2 mg/dL. Se realizó ecografía, la cual mostró ausencia de vesícula biliar, y dilatación irregular de los canales biliares. El diagnóstico de impresión fue de tumor de la ampolla de Vater.
La TAC mostró: “Hígado sin lesión tumoral. Dilatación de las vías biliares intra y extrahepáticas. Colédoco de 2 cm de diámetro y de forma distal irregular. Páncreas con lesión expansiva en la cabeza, de 4.5 cm, que indica existencia de neoplasia”.
Se intervino quirúrgicamente y se encontró una masa exofítica duodenal, localizada en la papila, rodeada de bastante cantidad de material mucinoide, con gran dilatación del conducto pancreático el cual estaba ocupado por moco. El colédoco se hallaba dilatado, sin signos de invasión neoplásica, motivo por el cual se realizó antrectomía gástrica y pancreatectomía total. Se reconstruyó la continuidad con gastroyeyunostomía en “Y” de Roux con he patoyeyunostomía terminolateral. No había compromiso de las venas cava y porta, ni de la arteria aorta ni de ninguna otra estructura. La patología informó: “Neoplasia epitelial maligna de aspecto papilar arborescente que infiltra profundamente hasta el tejido adiposo con compromiso perineural. Tumor que originado en la mucosa duodenal, infiltra el conducto pancreático en sus 2/3 proximales, respetando la palila” (Figs. 1 y 2).
Diagnóstico final: “Adenocarcinoma del duodeno con infiltración al páncreas y metástasis al epiplón mayor. Ganglios libres de tumor”. Actualmente está vivo y recibe suplemento enzimático e insulina.
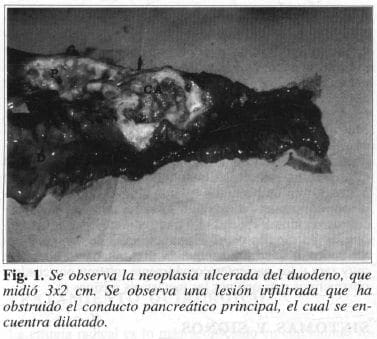 |
 |
P: Páncreas
D: Duodeno
CA: Carcino
Segundo caso
Paciente de 61 años con cuadro clínico de 15 días de evolución, que se inició con vómito posprandial y que fue tratado con antieméticos, sin mejoría. Luego apareció ictericia, y acusó pérdida de peso y adinamia en los últimos días. Al examen se encontró un paciente emaciado, ictérico, con defensa abdominal voluntaria en el hipocondrio derecho, y vesícula palpable. El laboratorio mostró: Hb. 12.5 gr/dL; leucocitos: 1O.500/roL; neutrófilos: 83%; linfocitos: 16%; plaquetas: normales; bil.dir: 3.8 mg/dL; bil. ind: 1.5 mg/dL; TGO: 32 UIL; TGP: 68 UIL; fosfatasa alcalina: 1.258 UIL; creatinina: 1.1 mg/dL; glicemia: 108 mg/dL ..
Ecografía: “Vesícula biliar dilatada sin cálculos. Vías biliares intra y extrahepáticas dilatadas”. Serie esofago- gastroduodenal: “Masa en nivel del páncreas con compresión extrínseca duodenal”. Endoscopia digestiva alta: Esofago normal. Estómago con escasa motilidad y pliegues enantematosos; píloro excéntrico puntiforme. Duodeno: Mucosa enantematosa con pliegues hipertróficos y presencia de ulceración superficial”.
El paciente fue llevado a cirugía, en la que se halló: “Masa duodenal que comprometía el duodeno y el páncreas, por lo cual se realizó duodenopancreatectomía cefálica. En seguida se reconstruyó el tracto digestivo en “Y” de Roux retrocólica y se dejó el páncreas abandonado. No se observaron metástasis ganglionares ni hepáticas. En el estudio patológico macroscópico se identificó en el duodeno, una masa de 5x4x4, de localización mucosa y de aspecto exofítico, la cual respetaba la papila duodenal. La patología informó: “Adenocarcinoma del duodeno. Compromiso de toda la pared duodenal. Epiplón mayor comprometido. Papila libre de tumor”. Evolucionó inicialmente en forma satisfactoria, pero falleció a los 15 días de una pancreatitis hemorrágica aguda (Fig. 3).

Discusión
Incidencia
Sólo el 3% de los tumores del tracto digestivo se originan en el intestino delgado. El 0.3% de las neoplasias del tracto digestivo corresponden al duodeno; del 25 al 48% de los carcinomas del intestino delgado son duodenales (4, 6) (Tabla 1). La Sociedad Americana de Cáncer informa unos 2.700 casos anuales de cáncer del intestino delgado, con una distribución entre hombres y mujeres muy similar; este tumor causa alrededor de 900 muertes anuales (5).

En 1989 la Sociedad Americana del Cáncer estimó en 151.000 los casos nuevos por año de cáncer colorrectal y, en USA, se observan 700 casos de andenocarcinoma del intestino delgado cada año, esto es, l caso por 200 de cáncer colorrectal. La incidencia de neoplasia del intestino delgado ha sido estimada en la raza blanca en 1.2 por 100.000 para los hombres y en 0.8 por 100.000 para las mujeres; en la raza negra: 1.6 para hombres y 0.7 para mujeres (2). En general, el predominio es de los hombres de 3: 1 (6, 9).
Etiopatogenia
A pesar de que el intestino delgado presenta el 75% de la longitud de todo el tracto intestinal y le corresponde más del 90% de la superficie mucosa, la incidencia de neoplasia en él es muy baja. La explicación para ello incluye varias hipótesis: 1) Un rápido tránsito intestinal que disminuye la exposición a carcinógenos. 2) El contenido líquido relativamente estéril del intestino delgado. 3) La rápida proliferación de la mucosa intestinal que inhibe el crecimiento de células malignas. 4) La detoxificación de carcinógenos por enzimas microsomales como la benzopireno-hidroxilasa. 5) La alta concentración de tejido linfoide y la considerable producción de IgA, lo cual mejora la respuesta inmune (5, 7, 8).
Teniendo en cuenta que el duodeno representa menos del 10% del intestino, se deduce que pulgada a pulgada es más propenso al desarrollo del cáncer que el resto del intestino delgado (6).
Los factores predisponentes mencionados en la literatura para el cáncer del intestino delgado son los siguientes: el síndrome de Peutz-Jeghers, la poliposis familiar, los pólipos adenomatosos benignos del duodeno, el síndrome de Gardner, el adnoma velloso, la enfermedad de Crohn y la enfermedad celíaca del adulto (4, 8, 10). Kutin y Localio informan que el riesgo de malignidad aumenta en adenomas vellosos de 4 cm, en pacientes mayores de 50 años cuando este tumor está localizado en el duodeno distal (4). En las series analizadas, los porcentajes son los siguientes: 60% para adenocarcinomas; 27% para linfoma; y 11% para leiomiosarcoma (Tabla 1). Wilson señala en una recopilación de 2.144 tumores malignos del intestino delgado los siguientes porcentajes: adenocarcinoma, 50% y leiomiosarcoma, 11% (8).
El adenocarcinoma es la neoplasia maligna más común del duodeno y su incidencia llega hasta el 80% (6). Otras neoplasias del duodeno incluyen los sarcomas (linfosarcoma, leiomiosarcoma) y los tumores carcinoides malignos. Las neoplasias del duodeno usualmente se clasifican de acuerdo con su posición. Los tumores que están entre la ampolla y el píloro se llaman supraampulares; aquellos que se originan alrededor de la ampolla se definen como periampulares, y los que están entre la ampolla y el ligamento de Treitz, se denominan infraampulares (6). Los más frecuentes son los periampulares con un 50%, aunque Aiwmark encontró predominio de tumores supraampulares (4). El aspecto macroscópico puede ser de tres formas: una polipoide intraluminal; una lesión escirrosa anular e infiltrada y una forma ulcerada. Los tumores polipoides pueden originarse en un adenoma velloso o tubular (4, 9). El carcinoma duodenal se extiende primero a los ganglios linfáticos regionales, luego al hígado y por último a los pulmones. Al momento del diagnóstico 2/3 de los pacientes ya tienen metástasis, aunque la diseminación general es muy rara y los pacientes comúnmente mueren por cuadros obstructivos más que por las metástasis mismas (4).
Síntomas y Signos
Casi siempre son individuos en la sexta década de la vida (2, 6, 8, 13). En pacientes con síndrome de Gardner, el adenocarcinoma se presenta en una edad más temprana (44 años). Los síntomas de neoplasia maligna del duodeno se dividen en cuatro grupos: lesiones obstructivas con dolor posprandial, saciedad temprana y vómito; lesiones ulceradas con sangrado, anemia, melena y rara vez hematemesis.
Lesiones infiltradas con invasión de tejidos adyacentes y sintomatología semejante a la de la úlcera penetrada; y lesiones que comprometen la ampolla de Vater que causan ictericia (6). La pérdida de peso es frecuentemente debida a anorexia. En general, los síntomas son inespecífico s en un comienzo y el diagnóstico puede retardarse entre 6 meses y 1 año, por lo cual no es raro encontrar lesiones irresecables al momento de la intervención quirúrgica (4, 7, 9, 12). Al examen clínico de estos pacientes se puede hallar: anemia, prueba del guayaco positiva, masa palpable, ictericia, dolor abdominal, distensión abdominal; también puede encontrarse peritonitis cuando se ha producido perforación intestinal (2, 7, 9, 11, 12). En el 25% de los casos la masa palpable corresponde a la vesícula dilatada (2). Los síntomas y signos más comunes son: dolor abdominal, anemia, pérdida de peso y masa abdominal (9). Algunos han analizado y correlacionado los síntomas con la morfología del tumor, así: el carcinoma propende a la obstrucción total debido a su crecimiento anular; los carcinoides, linfomas y leiomiosarcomas causan obstrucción parcial y síntomas crónicos; los leiomiosarcomas, los leimiomas y los linfomas producen mayor sangrado; los leiomiosarcomas y los linfomas tienden a causar perforación e intususcepción (12).
Diagnóstico
El diagnóstico correcto preoperatorio se obtiene entre el 35 y el 70% de los casos (11). Los procedimientos diagnósticos son los siguientes: la serie gastroduodenal que alcanza una positividad del 30 al 90% (11); la radiografía simple del abdomen que sólo señala casos de obstrucción; la ecografía ayuda a determinar la presencia del tumor y la obstrucción biliar y permite una punción-biopsia dirigida; la tomografía axial computarizada ayuda en el diagnóstico diferencial al evaluar el páncreas y los tejidos vecinos; la duodenografía hipotónica mejora la sensibilidad de la serie gastroduodenal; la gastroduodenoscopia, es útil en los tumores periampulares y suprapapilares, así como para biopsia y citología por aspirado y cepillado; además, también tiene utilidad terapéutica en los casos de tumores pequeños (19); en los tumores periampulares la colangiografía transparietohepática (CTPH) es igualmente útil; la angiografía es de poca utilidad en el diagnóstico, pero recomendada para definir la resecabilidad del tumor (6, 8, 12); exámenes para investigar ácido 5-hidroxiindolacético, gastrina o somatostatina, se emplean ante la sospecha de tumor carcinoide (14).
Tratamiento Quirúrgico
La cirugía radical es 10 más aconsejado en carcinomas localizados en el duodeno; el procedimiento consiste en la extirpación de todo el duodeno, resección de la cabeza del páncreas, del antro gástrico, del colédoco distal y la linfadenectomía (2, 4, 6, 17, 18, 21, 24, 25).
En presencia de lesiones avanzadas o de enfermedad metastásica, puede ser necesaria la paliación de los síntomas obstructivos (15). La resecabilidad del carcinoma del duodeno varía entre el 46 y el 80%, dependiendo del diagnóstico temprano (4, 6, 18). La mortalidad operatoria en las distintas series oscila entre el O y el 60%, con un promedio, en informes recientes, de 21% (4, 6). Michelassi, en 1989, señala una mortalidad del 10% (18). Pero es necesario señalar que la mortalidad operatoria con el procedimiento de Whipple ha disminuido notoriamente, hasta cifras tan bajas como 0%, según el trabajo de Trede y col (21). La supervivencia a 5 años en el caso del carcinoma duodenal oscila entre ellO y el 35% (18). En el tratamiento del carcinoma duodenal confinado el área periampular, en sujetos viejos y de alto riesgo, se ha empleado la ampulectomía, descrita en 1898 por Halsted. Se encuentran trabajos, como el de Knox, que informan 0% de mortalidad operatoria, con supervivencia a 5 años del 51 %. Otros informan supervivencias entre el 17 y el 41 %, pero con una alta tasa de recurrencia local (16-18).
Por lo anterior, se sugiere emplear este procedimiento en casos muy seleccionados o ante la presencia de un tumor benigno (16). La literatura informa una sobrevida mayor con los procedimientos de resección que con los paliativos (16, 18). Braasch encuentra un 70% de sobrevida a 5 años en pacientes con carcinoma ampular; Crist y Herter refieren un porcentaje de sobrevida a 5 años, del 33% y del 27%, respectivamente, mediante el empleo de la técnica de Whipple para carcinoma duodenal (21). En 1935 fueron conservados el píloro y la primera porción del duodeno durante la operación original de Whipple (21-23). En el año de 1978, Traverso y Longmire preservaron el píloro y restablecieron la continuidad con una duodenoyeyunostomía terminolateral (22, 23). Este procedimiento ha sido aceptado de manera gradual para el tratamiento de condiciones benignas y malignas periampulares, debido al menor consumo de tiempo intraoperatorio, su facilidad técnica y su comportamiento más fisiológico. Se ha pensado que este tipo de cirugía compromete los márgenes de resección, pero la experiencia en tumores periampulares bien seleccionados y en el cáncer pancreático no ha demostrado diferencias en la supervivencia, respecto a los sometidos al procedimiento de Whipple tradicional (21).
La endoscopia ha contribuido al diagnóstico y a la terapéutica al permitir resecciones locales de adenomas con Ca in situ, usando el asa diatérmica o el láser, con ciertos inconvenientes como la resección incompleta, la recurrencia local y la destrucción del espécimen. Ella presta ayuda en la paliación por obstrucción del duodeno o de la vía biliar (19, 20). La radioterapia y la quimioterapia pueden ayudar al tratamiento del carcinoma del duodeno, para la paliación y para mejorar la supervivencia cuando hay enfermedad microscópica residual (2).
Abstract
Information obtained fmm two cases of primary adenocarcinoma of the duodenum treated at the Santa Sofía General Hospital and at the Caldas Hospital in the city of Manizales is presented, a review of the world literature found on this subject is made, with the reminder that early diagnosis is the Key to success in the treatment of this entity.
Referencias
1. Mirizzi P L: Intestino delgado. En: Diagnóstico de los tumores abdominales, 2da Edición. Barcelona, Salvat Edil. 1960. pp. 315- 31
2. Nelson R L: Adenocarcinoma de Intestino delgado En: Nelson R L, Nyhus LL M: Cirugía del Intestino Delgado, la Edición, Barcelona, Salvat Edit, S. A. 1990. pp. 221-8
3. Schnur P L, David E, Brown P W et al: Adenocarcinoma of the Duodenum and the Gardner Syndrome. JAMA 1973 Mar; 223 (11): 1229- 32
4. Alwmark A, Anderson A, Lasson A: Primary Carcinoma of the Duodenum. Ann Surg 1980 Jan; 191 (1): 13-18 5. Mason G R: Tumors of the Duodenum
and small intenstine. In: Sabiston D C: Texbook of Surgery, 14th edition, Philadelphia. W. B. Saunders Comp, 1991, pp. 802-7
6. Lillemoe K, Imbembo A L: Malignant neoplasms of the duodenum. SGO 1980 Jun; 150: 822-6
7. Zollinger R M, Stemfeld W C, Schrelber H: Primary Neoplasms of the small intestine. Am J Surg 1986 Jun; 151: 654-8 8. Millal V K, Bodzin J H: Primary Malignant tumors of the small Bowel. Am J Surg 1980 Sep; 140: 396-9
9. De Lima E, Vemazza A, Salpuero G et al: Carcinoma primario del duodeno. Informe de 4 casos. Rev Col Gastroent 1987 oct-dic; 2 (4): 37-43
lO. Williamson R C, Whelch C E, Malt R A: Adenocarcinoma and Iymphoma of the Small Intestine. Ann Surg 1983 Feb; 197 (2): 172- 7
11. Ciccarelli O, Welch J P, Kcnt G G et al: Primary malignant tumors of the Small Bowcl. Am J Surg 1987 Apr; 153: 350-4
12. Milcs R M, Crawford D, Duras S: The Small Bowel Tumor problem. Ann Surg 1979 Jun; 189 (6): 752-9
13. Goel l P, Didolkar M S, Elias E G: Primary Malignant tumors of the Small Intestine. SGO 1976 Nov; 143: 717-9 14. Lasson A, Alwmark A, Nobin A et al: Endocrinc tumors of the Duodenum. Ann Surg 1983 Apr; 197 (4) 393-8
15. Albornoz H, Arango R, Calderón M: Carcinoma Primario de Duodeno. Rev Col Gastrocnt 1992 dic; 7 (4): 266-8 16. Kahn M B, Rush B F: The overlookcd techniquc of ampullary excision. SGO 1989 Scpt; 169: 253-4
17. Díaz F J, García-Alonso l, Peña J ct al: Ampulomas. Estudio rctrospectivo de 49 casos. Cir Esp 1992 abr; 51 (4): 269-74
18. Michelassi F, Errol F, Dawson P J et al: Experience with 647 Consecutive Tumors of the Duodenum, Ampulla, Head of the Pancreas, and Distal Common Bile Duct. Ann Surg 1989 Oct; 210 (4): 544-56
19. Ponchon T, Berger F, Chavaillon A et al: Contribution of Endoscopy to Diagnosis and Treatment of Tumors of the Ampulla of Vater. Cancer 1989 Jul; 64: 161-8
20. Shemesh E, Nass S, Czerniak A: Endoscopic Sphinterotomy and Endoscopic Fulguration in the Management of Adenoma of the Papilla of Vater. SGO 1989 Nov; 169: 445-8
21. Crist D W, Cameron J L: The Current Status of the Whipple Operation for Periampullary Carcinoma. Adv Surg 1992 Jan; 25: 21- 48
22. Caro A: Tratamiento del Carcinoma del Páncreas. Rev Col Cirug 1990 agt; 5 (2): 75-82
23. Newman Kurt, Vates T, Duffy L et al: Pancrcatoduodenectomy with Preservation of the Stomach and Pylorus: Safe and Effective Alternative in Children. J Pediatr Surg 1992; 27 (lO): 1334-5
24. Cubillos L, Concha R, Lezana G et al: Cancer primitivo de duodeno. Rev Chil Cir 1993; 45 (2): 150-8
25. Burmeister R, León J. Apablaza S et al:
Comentario
Andrés Muñoz Mora, M D, SCC.
Cirujano General
Inst. Nal. de Cancerología, Grupo Gastroenterología.
El pronóstico de los adenocarcinomas del duodeno depende principalmente de la extensión en profundidad a través de su pared y del número de ganglios linfáticos comprometidos, tal como sucede en otros órganos del tracto digestivo. Igualmente, la perforación de un carcinoma duodenal usualmente produce siembras peritoneales. Es evidente la importancia de efectuar diagnósticos precisos de esta entidad. Sin embargo, dada la baja incidencia del adenocarcinoma primario del duodeno en comparación con otros carcinomas del tubo digestivo, es de esperarse que la sospecha clínica del mismo sea infrecuente especialmente si tenemos en cuenta que los síntomas que produce son, en su mayoría, inespecífico s a menos que, tal como sucedió en los dos casos que se presental1, el paciente tenga una ictericia de tipo obstructivo, lo cual permite en cierta medida enfocar el diagnóstico hacia la sospecha de una lesión periampular.
El paciente anémico con melenas y exámenes normales de estómago y colon, amerita una evaluación ordenada del intestino delgado. La radiografía de vías digestivas altas, la endoscopia y la TAC deben ser complementarios. En un momento dado una duodenografía puede detectar, por ejemplo, una estenosis en la cuarta porción doudenal, inalcanzable para el endoscopista, y lo contrario también puede suceder.
Desde el punto de vista terapéutico llama la atención en el primer paciente del presente artículo, la práctica de una pancreatectomía total como tratamiento de una masa que macroscópicamente estaba ubicada en nivel de la papila. Seguramente una pancreatoduodenectomía de Whipplehabría sido suficiente tratamiento para este enfermo, sin comprometer su función endocrina.
En segundo caso, probablemente se trataba de una lesión que aunque no coprometía la papila, sí debía estar infiltrando el colédoco intrapancreático, ya que el enfermo presentaba ictericia obstructiva. Seguramente era un caso más avanzado que el anterior. En este paciente aparentemente se conservó el píloro, lo cual, tal como lo mencionan los autores y ha sido publicado por Rossi, no se ha demostrrado que disminuya la sobrevida, siempre y cuando la selección del caso sea regurosa. Otra modificación técnica de la pancreatoduodenectomía efectuada en este mismo paciente, fue la de dejar el páncreas abandonado. Personalmente me parece un excelente recurso en pacientes con páncreas blandos o que presenten dificultades técnicas para llevar a cabo la anastomosis pancreatoyeyunal; pero especialmente en aquellos individuos deteriorados nutricionalmente que presentan un mayor riesgo de fístula pancreatoyeyunal. Vale la pena anotar que con el páncreas abandonado la función exocrina queda abolida, lo que impone una suplencia enzimática permanente, y la incidencia de fístula pancreática es prácticamente del 100%.
Sin embargo, esta fístula es de manejo relativamente fácil, a diferencia de la fístula pancreatoyeyunal que es la principal causa de mortalidad en el paciente pancreatectamizado.
Doctores: Juan Carlos Marín M., R-lll de Cirugía; Mauricio Osorio Ch., R-1V de Cirugía; Augusto Arango
G., Cirujano Adj., Hosp. Gral. Santa Sofía; Alberto Angel P., Jefe del Servo de Cirugía, Hosp. de Caldas, Fac. de
Med. U. de Caldas; Guillermo López G., Patólogo, Jefe del Lab. Departamental, Servo Seccional de Salud de Caldas; Luis A. Mejía, Patólogo Docente, Hosp. de Caldas, U. de Caldas, Manizales, Colombia.
