Combinación de ICIs con quimioterapia en la primera línea de tratamiento del CPCNP (independiente del nivel de expresión de PD-L1)
En los estudios clínicos que valoraron el papel de los ICIs como monoterapia o en combinación (inhibidores de PD-1/L1 más CTLA-4) en pacientes con expresión de PD-L1 ≥1% (11,16,20,22) se ha documentado un fenómeno donde las curvas de supervivencia se entrecruzan tempranamente.
Este hallazgo ha sugerido que una proporción de pacientes sin beneficio con la inmunoterapia podrían no exponerse a la intervención con base en el uso de biomarcadores con un alto valor predictivo negativo.
Con la finalidad de superar esta situación y tomar ventaja de la actividad sinérgica de los agentes citotóxicos y de la inmunoterapia, diferentes estudios clínicos evaluaron el papel de la combinación de ICIs con quimioterapia.
Hay que resaltar, la existencia de la hiperprogresión, un modelo negativo de respuesta encontrado en aproximadamente 14-26% de los pacientes con CPCNP pretratados que recibieron monoterapia con algún ICI en segunda línea.
Hace poco, el análisis exhaustivo de una cohorte de pacientes tratados con ICIs permitió confirmar que la hiperprogresión se presenta hasta en el 16% de los pacientes con elevada expresión de PD-L1, posiblemente por la presencia de resistencia innata mediada por comutaciones en genes como STK11 y KEAP1.
No obstante, la hiperprogresión es inusual (6%) entre los sujetos expuestos a quimioterapia más inmunoterapia (23), evento que respalda el uso de este tipo de combinaciones en primera línea.
Resultados de múltiples estudios fase 3
Los resultados de múltiples estudios fase 3 incluyendo el KEYNOTE-189 (24,25), IMpower150 (26,27), IMpower132 (28), IMpower130 (29), ORIENT-12 (30) y RATIONALE 304 (31) soportan el uso de nuevas combinaciones con ICIs como primera línea estándar para pacientes con carcinomas no escamosos de pulmón.
De igual forma, los estudios KEYNOTE-407 (32,33), IMpower131 (34) y RATIONALE 307 (35) demostraron el papel de la quimioinmunoterapia para el tratamiento de los carcinomas escamosos, y CheckMate 227 parte 2 (36) y CheckMate 9LA (37) para ambos subgrupos histológicos.
En el estudio KEYNOTE-189:
Se incluyeron pacientes con CPCNP no escamoso avanzado, sin mutaciones en EGFR o ALK, siendo asignados de forma aleatoria en un formato 2:1 para recibir pemetrexed más cisplation o carboplatin y pembrolizumab o placebo cada 3 semans por 4 ciclos; posteriormente, pembrolizumab y pemetrexed o pemetrexed más placebo hasta completar 2 años o 35 ciclos (24).
El uso del pembrolizumab en combinación con quimioterapia mejoró significativamente la mediana de la OS (22,0 meses vs. 10,6 meses, HR 0,56 IC 95% 0,46-0,96), a pesar de que hubo un entrecruzamiento del 55%.
Hay que resaltar que beneficio sobre la OS se observó en todos los subgrupos de expresión de PD-L1 [PD-L1 ≥50% 27,7 meses vs. 10,1 meses (HR 0,59, IC 95% 0,40- 0,86); PD-L1 1-49% 21,8 meses vs. 12,1 meses (HR 0,66, IC 95% 0,46-0,96); y PD-L1 <1% 17,2 meses vs. 10,2 meses (HR 0,51, IC 95% 0,36-0,71)].
La PFS también favoreció la combinación de pembrolizumab más quimioterapia (9,0 meses vs. 4,9 meses, HR 0,49, IC 95% 0,41-0,59) (25). En el estudio KEYNOTE-189, la TMB medida en sangre o en tejido no fue útil como biomarcador predictivo (38,39).
En el estudio IMpower150, la adición de atezolizumab a bevacizumab más quimioterapia (brazo B) mejoró significativamente la PFS (8,3 meses vs. 6,8 meses, HR 0,62, IC 95% 0,52-0,74; P<0,001) y la OS (19,2 meses vs. 14,7 meses, HR 0,78 IC 95% 0,64-0,96; P=0,02) en comparación con el uso de bevacizumab más quimioterapia (brazo C) en pacientes con CPCNP no escamoso metastásico independeinte de la expresión de PD-L1 (26).
El análisis final del IMpower150 también mostró una mejoría numérica en la OS sin modificaciones estadísticamente significativas en el brazo A (atezolizumab más quimioterapia) vs. el brazo C (40). En el subgrupo de sujetos con mutaciones del EGFR el esquema del brazo B vs. el brazo C mejoró la PFS (10,2 meses vs. 7,1 meses, HR 0,56 IC 95% 0,34-0,91) y la OS (26,1 meses vs. 20,3 meses, HR 0,91 IC 95% 0,43-1,39) (27,41).
En contraposición, el brazo A no mejoró la PFS (HR 0,93 IC 95% 0,60-1,44) o la OS (HR 1,16 IC 95% 0,71-1,89) en el grupo de pacientes portadores de mutaciones en el EGFR (41).
El estudio Impower130 (29) fue un experimento multicéntrico abierto y con asignación aleatoria que incluyó pacientes con un formato 2:1 a recibir atezolizumab (1.200 mg c/3 semanas) más carboplatino y paclitaxel unido a nanoparticulas de albumina (nab-P) (4–6 ciclos) seguido de mantenimiento con atezolizumab hasta la intolerancia o progresión.
El IMpower130 (29) reportó un beneficio en la OS con la introducción del monoclonal anti-PD-L1 cuando se comparó con la quimioterapia (18,6 meses vs. 13,9 meses, HR 0,79 IC 95% 0,64-0,98; P=0,033), pese a que se documentó un 59% de entrecruzamiento con la inmunoterapia al momento de la progresión.
No obstante, el beneficio real de esta combinación fue circunscrito a los sujetos sin mutaciones en EGFR/ALK y entre aquellos sin extensión hepática de la enfermedad, sugiriendo un papel aditivo con el uso concomitante del bevacizumab.
Por otra parte, el uso del atezolizumab en combinación también mejoró la PFS (7,0 meses en el brazo de atezolizumab más quimioterapia vs. 5,5 meses en el brazo de quimioterapia, HR 0,64 IC 95% 0,54 -0,77; P<0,0001) y la RR (49,2% vs 39,2%, respectivamente).
Finalmente, dos estudios solo reclutaron pacientes asiáticos; el ORIENT, que aleatorizó (2:1) 397 pacientes con CPCNP no escamoso avanzado sin alteraciones en EGFR o ALK a recibir sintilimab 200 mg más quimioterapia con base en platino vs. cisplatino/pemetrexed/ placebo c/3 semanas por 4 ciclos seguidos, en ambos casos, de mantenimiento con sintilimab/ pemetrexed o pemetrexed/placebo.
La adición del sintilimab mejoró significativamente la PFS en comparación con el control (8,9 meses vs. 5,0 meses, HR 0,48 IC 95% 0,362-0,643; P<0,00001), al igual que incrementó la RR (51,9% vs. 29,8%).
El beneficio para la PFS fue evidente en todos los subgrupos, siento superior para los pacientes con expresión positiva de PDL1 (1-49% HR 0,50 IC 95% 0,28-0,92 y ≥50% HR 0,31 IC 95% 0,19-0,49) vs. aquellos con tumores con PD-L1 negativo (HR 0,66 IC 95% 0,41-1,091) (30).
El otro estudio dirigido a la población asiática exclusiva fue el RATIONALE 307, un experimento clínico fase 3 que incluyó 334 pacientes con CPCNO de patrón no escamoso sin alteraciones en EGFR o ALK.
El estudio asignó de forma aleatoria (2:1) el uso de tislelizumab (200 mg) más la combinación de platino y pemetrexed por 4 ciclos seguido de tislelizumab más pemetrexed vs. el modelo de tratamiento estándar solo con quimioterapia.
El uso del tislelizumab mejoró la mediana de la PFS (9,7 meses vs. 7,6 meses, HR 0,56 IC 95%CI 0,46-0,90; P<0,0044) y la RR (57,4% vs. 37%). Sin embargo, el análisis por subgrupos demostró ineficacia sobre la PFS para aquellos con PD-L1 negativo (HR 0,76 IC 95% 0,46-1,22), mientras el mayor beneficio se vio para la población de altos expresores (PD-L1 ≥50% HR 0,31 IC 0,17-0,57) (31).
En los pacientes con CPCNP de patrón escamoso avanzado el estudio KEYNOTE-407 aleatorizó pacientes (1:1) a recibir carboplatino/paclitaxel o paclitaxel unido a nanopartículas de albumina +/- pembrolizumab hasta completar 35 ciclos o 2 años de tratamiento.
La combinación de quimioterapia más el anti-PD-1 se asoció con una mejora significativa de la RR (58,4% vs. 35,0%; P=0,0004) y de la OS (HR 0,64, 15,9 vs. 11,3 meses; P=0,0008). El beneficio sobre la OS fue homogéneo entre todos los subgrupos de expresión del PD-L1 (TPS <1% HR 0,61, TPS 1%–49% HR 0,57, y TPS ≥50% HR 0,64) (32,33).
De hecho, la adición de pembrolizumab a la quimioterapia mantuvo o mejoró la calidad de vida (HRQoL) valorada a las 9 y 18 semanas de seguimiento (42). En el experimento clínico fase 3 RATIONALE 307, 360 pacientes asiáticos con CPCNP de patrón escamoso avanzado (all comers) fueron aleatorizados a recibir tislelizumab más nab-P o quimioterapia sola.
El brazo de la combinación con el monoclonal alcanzó una PFS más prolongada (7,6 meses vs. 5,5 meses) y una mayor RR (74% vs. 50%). El beneficio sobre la PFS fue evidente en todos los subgrupos de expresión de PD-L1 (35).
Finalmente, el estudio CheckMate 9LA (37) valoró la combinación de nivolumab más ipilimumab y 2 ciclos de quimioterapia vs. quimioterapia en primera línea para pacientes con CPCNP avanzado indistintamente de su variante histológica.
En el análisis intermedio se encontró que la mediana para la S se prologó significativamente con el uso de la inmunoterapia dual más la quimioterapia comparada con la quimioterapia sola (14,1 meses vs. 10,7 meses, HR 0,69 IC 96,71% 0,55–0,87; P=0,0006); el beneficio ocurrió de manera independiente al subtipo histológico (histología escamosa 14,5 vs. 9,1 meses, HR 0,62 e histología no escamosa 17,0 vs. 11,9 meses, HR 0,69), y para los tumores PD-L1-positivos (≥1% HR0,64) y PD-L1-negativos (<1% HR 0,62).
La FDA aprobó este modelo de tratamiento como parte de la primera línea en mayo de 2020 y la EMA en septiembre del mismo año.
El estudio POSEIDON (NCT03164616) actualmente en curso, está evaluando la efectividad del durvalumab en combinación con quimioterapia con y sin tremelimumab vs. la quimioterapia sola en pacientes con CPCNP usando como desenlaces primarios la PFS y OS de acuerdo a una revisión independiente.
Se estima que sus resultados estarán disponibles en abril de 2021. Independientemente de estos resultados clínicamente relevantes, otros estudios no reportaron beneficios en la OS cuando se valoró el uso de la quimioterapia en combinación con ICIs, incluyendo el IMpower132 (28), la parte 2 del CheckMate 22736 y el IMpower131 (34).
En el estudio Impower132, la adición del atezolizumab a la quimioterapia con platino más pemetrexed impactó la PFS vs. la quimioterapia sola (7,6 meses vs. 5,2 meses, HR 0,60 IC 95% 0,49-0,72; P<0,0001) sin modificar significativamente la OS (18.1 meses vs. 13,6 meses, HR 0,81 IC 95% 0,64-1,03; P=0,0797) al término del seguimiento (la OS final aún se encuentra pendiente) (28).
Así mismo, la parte 2 del CheckMate 227 no encontró un impacto positivo con la combinación de nivolumab más quimioterapia vs. la quimioterapia sola en los pacientes con histología no escamosa (18,8 meses vs. 15,6 meses, HR 0,86 IC 95% 0,69-1,08; P=0,1859), aunque un análisis exploratorio demostró impacto con la combinación en los pacientes con PD-L1 ≥50% (HR 0,56) (36).
Por otra parte, el estudio IMpower131, probó la combinación de atezolizumab más quimioterapia en 1.021 pacientes con CPCNP de patrón escamoso sin modificar la OS al comparar con la quimioterapia sola (14,2 meses vs. 13,5 meses, HR 0,88 IC 95% 0,73-1,05; P= 0,16).
Como excepción, el IMpower131 demostró superioridad para el brazo experimental respecto de la OS en el subgrupo de pacientes con alta expresión de PD-L1 (HR 0,48 IC 95% 0,29-0,81) (34). La Figura 3 ilustra las opciones de tratamiento para los pacientes con CPCNP sin blancos moleculares potencialmente modulables.
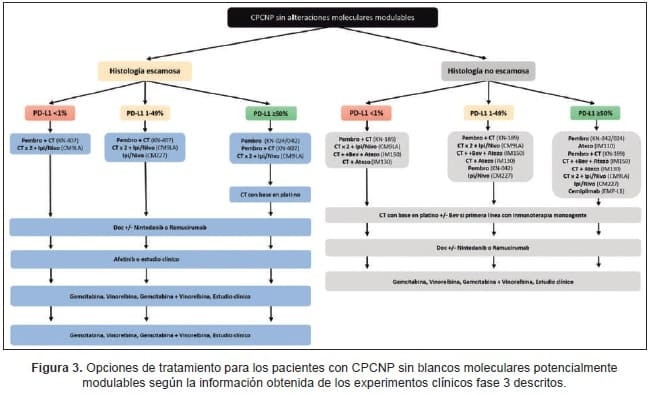
(Lea También: Historia de los Receptores Hormonales y de la Terapia Hormonal en Cáncer de Mama)
Interrogantes abiertos
Globalmente, los datos apoyan el hecho de que los ICIs son el nuevo tratamiento estándar en los pacientes con CPCNP avanzado, independiente del subtipo histológico y de la expresión de PD-L1, siendo la estrategia en combinación la más adecuada para los tumores con PD-L1 negativo (43).
Sin embargo, aún existe controversia alrededor del mejor manejo para aquellos con un PD-L1 ≥50%, ya que ninguno de los experimentos comparó de forma directa el uso de un ICI más quimioterapia vs. la monoterapia con un ICI.
La comparación indirecta entre los estudios mostró desenlaces similares respecto de la OS entre los pacientes con PD-L1 ≥ 50%, con perfiles de toxicidad diferentes, sugiriendo por el momento que la monoterapia con pembrolizumab puede ser la opción más razonable para esta población.
El estudio EA5163/ S1709 está valorando si la inducción con pembrolizumab es superior a la combinación de pemetrexed más platino y pembrolizumab en pacientes con tumores no escamosos avanzados. Dicho experimento se estratificará de acuerdo al nivel de expresión del PD-L1 (≥50% vs. 1-49%) para poder elucidar la mejor estrategia.
El uso de otros biomarcadores y su utilidad para subseleccionar a los pacientes con base en la genómica sigue siendo un área plena de incertidumbre, en especial, si se consideran algunas alteraciones que favorecen la resistencia intrínseca (STK11 y KEAP1) o una mayor sensibilidad a la inmunoterapia (ARID1A). Por el momento, los resultados han sido variables y continúan sin confirmación prospectiva.
Finalmente, la duración óptima del tratamiento permanece indefinida.
Basándose en los datos del estudio CheckMate 153, el tratamiento con ICI debería continuar por más de un año (44). No obstante, para aquellos pacientes que completaron el número de ciclos por protocolo y progresaron, la reinducción con los ICIs puede brindar un beneficio clínico en cerca del 80% de los casos (9).
Actualmente, no hay parámetros definidos para definir cuales sujetos podrían ser candidatos para continuar una estrategia de supresión y reinducción.
Referencias
-
1. Garon EB. Hellmann MD. Rizvi NA. Carcereny E. Leighl NB. Ahn MJ et al. Five-Year Overall Survival for Patients With Advanced Non‒Small-Cell Lung Cancer Treated With Pembrolizumab: Results From the Phase I KEYNOTE- 001 Study. J Clin Onccol, 2019;37(28):2518- 25234
-
2. Faivre-Finn C, Vicente D. Kurata T. Planchard D. Paz- Ares L, Vansteenkiste J et al. LBA49 Durvalumab after chemoradiotherapy in stage III NSCLC: 4-year survival update from the phase III PACIFIC trial. Ann Oncol, 2020;31:S1178-S11781
-
3. Provencio M. Nadal E. Insa A. García-Campelo M. Casal- Rubio J. Dómine M et al. Neoadjuvant chemotherapy and nivolumab in resectable non-small-cell lung cancer (NADIM): an open-label. Multicentre, single-arm. Phase 2 trial. Lancet Onco24, 2020;21(11):1413-14-8
-
4. Benitez JC. Remon J. Besse B. Current Panorama and Challenges for Neoadjuvant Cancer Immunotherapy. Clin Cancer Res, 2020;26(19):5068-50755
-
5. Teixido C. Reguart N, Using biomarkers to determine optimal combinations with immunotherapy (biomarker discovery perspective). Future OnEngl, 2020;16(23):1677- 1671
-
6. Tsao MS. Kerr KM. Kockx M. Beasley MB. Borczuk AC. Botling J et al. PD-L1 Immunohistochemistry Comparability Study in Real-Life Clinical Samples: Results of Blueprint Phase 2 Project. J Thorac Oncer, 2018;13(9):1302- 13113
-
7. Aguilar EJ. Ricciuti B. Gainor JF. Kehl KL. Kravets S. Dahlberg S et al. Outcomes to first-line pembrolizumab in patients with non-small-cell lung cancer and very high PD-L1 expression. Ann Oncol, 2019;30(10):1653-1688
-
8. Reck M. Rodríguez-Abreu D. Robinson AG. Hui R. Csőszi T. Fülöp A et al. Pembrolizumab vs. Chemotherapy for PD-L1-Positive Non-Small-Cell Lung Cancer. N Engl J Med, 2016;375(19):1823-1874
-
9. Brahmer JR. Rodriguez-Abreu D. Robinson AG. Hui R. Csőszi T. Fülöp A et al. KEYNOTE-024 5-year OS update: First-line (1L) pembrolizumab (pembro) vs platinum- based chemotherapy (chemo) in patients (pts) with metastatic NSCLC and PD-L1 tumour proportion score (TPS) ≥50%. Ann Oncol, 2020;31:S1181-S11884
-
10. Mok TSK, Wu Y-L. Kudaba I. Kowalski D. Cho B, Turna H et al. Pembrolizumab vs. chemotherapy for previously untreated. PD-L1-expressing. Locally advanced or metastatic non-small-cell lung cancer (KEYNOTE-042): a randomised. Open-label. Controlled. Phase 3 trial. LancEngl, 2019;393(10183):1819-183-7
-
11. Mok TSK, Wu Y-L. Kudaba I. Kowalski D. Cho B, Turna H et al. Final analysis of the phase III KEYNOTE-042 study: Pembrolizumab (Pembro) vs. platinum-based chemotherapy (Chemo) as first-line therapy for patients (Pts) with PD-L1–positive locally advanced/metastatic NSCLC. Ann Oncol, 2019;30:i363
-
12. Herbst RS. Giaccone G. De Marinis F. Reinmuth N, Vergnenegre A. Barrios CH et al. Atezolizumab for First- Line Treatment of PD-L1-Selected Patients with NSCLC. N Engl J Med, 2020;383(14):1328-13346
-
13. Sezer A. Kilickap S. Gümüş M. Bondarenko I, Özgüroglu M. Gogishvili M et al. LBA52 EMPOWER-Lung 1: Phase III first-line (1L) cemiplimab monotherapy vs platinumdoublet chemotherapy (chemo) in advanced non-small cell lung cancer (NSCLC) with programmed cell deathligand 1 (PD-L1) ≥50%. Ann Oncol, 2020;31:S1182- S11885
-
14. Brahmer JR. Rodríguez-Abreu D. Robinson AG. Hui R. Csőszi T. Fülöp A et al. Health-related quality-of-life results for pembrolizumab vs. chemotherapy in advanced. PD-L1-positive NSCLC (KEYNOTE-024): a multicentre. International. Randomised. Open-label phase 3 trial. Lancet Oncol, 2017;18(12):1600-160-3
-
15. Carbone DP. Reck M. Paz-Ares L. Creelan B. Horn L, Steins M et al. First-Line Nivolumab in Stage IV or Recurrent Non-Small-Cell Lung Cancer. N Engl J Med, 2017;376(25):2415-2493
-
16. Rizvi NA. Cho BC. Reinmuth N. Lee KH. Luft A. Ahn MJ et al. Durvalumab With or Without Tremelimumab vs Standard Chemotherapy in First-line Treatment of Metastatic Non-Small Cell Lung Cancer: The MYSTIC Phase 3 Randomized Clinical Trial. JAMA Oncol, 2020;6(5):661-6737
-
17. Ramalingam SS. Ciuleanu TE. Pluzanski A. Lee J, Schenker M. Bernabe-Caro R et al. Nivolumab + ipilimumab vs. platinum-doublet chemotherapy as firstline treatment for advanced non-small cell lung cancer: Three-year update from CheckMate 227 Part 1. J Clin Oncol, 2020;38(15_suppl):9500-9500
-
18. Hellmann MD. Paz-Ares L. Bernabe Caro R, Zurawski B. Kim S. Carcereny-Costa E et al. Nivolumab plus Ipilimumab in Advanced Non-Small-Cell Lung Cancer. N Engl J Med, 2019;381(21):2020-20331
-
19. Ready N. Hellmann MD. Awad MM. Otterson GA. Gutierrez M. Gainor JF et al. First-Line Nivolumab Plus Ipilimumab in Advanced Non-Small-Cell Lung Cancer (CheckMate 568): Outcomes by Programmed Death Ligand 1 and Tumor Mutational Burden as Biomarkers. J Clin Onccol, 2019;37(12):992-1042
-
20. Hellmann MD. Ciuleanu T-E. Pluzanski A. Lee JS. Otterson GA. Audigier-Valette C et al. Nivolumab plus Ipilimumab in Lung Cancer with a High Tumor Mutational Burden. N Engl J Med, 2018;378(22):2093-2146
-
21. Marabelle A. Fakih M. Lopez J, Shah M, Shapira-Frommer R. Nakagawa K et al. Association of tumour mutational burden with outcomes in patients with advanced solid tumours treated with pembrolizumab: prospective biomarker analysis of the multicohort. Open-label. Phase 2 KEYNOTE-158 study. Lancet Oncol, 2020;21(10):1353-13-9
-
22. Ramalingam SS. Ciuleanu TE. Pluzanski A. Lee J, Schenker M. Bernabe-Caro R et al. Nivolumab + ipilimumab vs. platinum-doublet chemotherapy as firstline treatment for advanced non-small cell lung cancer: Three-year update from CheckMate 227 Part 1. J Clin Oncol, 2020;38(15_suppl):9500-9500
-
23. Ferrara R. Facchinetti F. Calareso G. Kasraoui I, Signorelli D. Proto C et al. Hyperprogressive disease (HPD) upon first-line PD-1/PD-L1 inhibitors (ICI) as single agent or in combination with platinum-based chemotherapy in non-small cell lung cancer (NSCLC) patients (pts). Ann Oncol, 2020;31:S892
-
24. Gandhi L. Rodríguez-Abreu D. Gadgeel S. Esteban E. Felip E. De Angelis F et al. Pembrolizumab plus Chemotherapy in Metastatic Non-Small-Cell Lung Cancer. N Engl J Med, 2018;378(22):2078-2005
-
25. Rodriguez-Abreu D. Powell SF. Hochmair M. Gadgeed SM. Esteban E. Felip E. Et al. Final analysis of KEYNOTE- 189: Pemetrexed-platinum chemotherapy (chemo) with or without pembrolizumab (pembro) in patients (pts) with previously untreated metastatic nonsquamous non-small cell lung cancer (NSCLC). J Clin Oncol, 2020;38(15_suppl):9582-9582
-
26. Socinski MA. Jotte RM. Cappuzzo F. Orlandi F, Stroyakovskiy D. Nogasmi N et al. Atezolizumab for First- Line Treatment of Metastatic Nonsquamous NSCLC. N Engl J Med, 2018;378(24):2288-2348
-
27. Reck M. Mok TSK. Nishio M. Jotte R. Cappuzzo F. Orlandi F et al. Atezolizumab plus bevacizumab and chemotherapy in non-small-cell lung cancer (IMpower150): key subgroup analyses of patients with EGFR mutations or baseline liver metastases in a randomised. Open-label phase 3 trial. Lancet Respir Med, 2019;7(5):387-4-0
-
28. Papadimitrakopoulou V. Cobo M. Bordoni R. Bordoni R. Dubray-Longeras P Szalai Z et al. IMpower132: PFS and Safety Results with 1L Atezolizumab + Carboplatin/ Cisplatin + Pemetrexed in Stage IV Non-Squamous NSCLC. J Thorac Oncol, 2018;13(10):S332-S362
-
29. West H. McCleod M. Hussein M. Morabito A. Rittmeyer A. Conter HJ et al. Atezolizumab in combination with carboplatin plus nab-paclitaxel chemotherapy compared with chemotherapy alone as first-line treatment for metastatic non-squamous non-small-cell lung cancer (IMpower130): a multicentre. Randomised. Open-label. Phase 3 trial. Lancet Oncol, 2019;20(7):924-9-6
-
30. Yang Y, Wang Z. Fang J, Yu Q. Han B. Cang S et al. Efficacy and Safety of Sintilimab Plus Pemetrexed and Platinum as First-Line Treatment for Locally Advanced or Metastatic Nonsquamous NSCLC: a Randomized. Double-Blind. Phase 3 Study (Oncology pRogram by InnovENT anti- PD-1-11). J Thorac Oncer, 2020;15(10):1636-1614
-
31. Lu S, Yu Y, Yu X. Hu Y. Ma Z. Li X et al, Tislelizumab + chemotherapy vs chemotherapy alone as first-line treatment for locally advanced/metastatic nonsquamous NSCLC. Ann Oncol, 2020;31:S816-S877
-
32. Paz-Ares L. Luft A, Vicente D, Tafreshi A. Gümüs M. Mazières J et al. Pembrolizumab plus Chemotherapy for Squamous Non-Small-Cell Lung Cancer. N Engl J Med, 2018;379(21):2040-2065
-
33. Paz-Ares L, Vicente D, Tafreshi A. Robinson A, Soto Parra H. Mazières J et al. Pembrolizumab (pembro) + chemotherapy (chemo) in metastatic squamous NSCLC: Final analysis and progression after the next line of therapy (PFS2) in KEYNOTE-407. Ann Oncol, 2019;30:v918-v980
-
34. Jotte R. Cappuzzo F, Vynnychenko I, Stroyakovskiy D. Rodríguez-Abreu D. Hussein M et al. Atezolizumab in Combination With Carboplatin and Nab-Paclitaxel in Advanced Squamous NSCLC (IMpower131): Results From a Randomized Phase III Trial. J Thorac Oncer, 2020;15(8):1351-1328
-
35. Wang J. Lu S. Hu C, Sun Y, Yang K. Chen M et al, Updated analysis of tislelizumab plus chemotherapy vs chemotherapy alone as first-line treatment of advanced squamous non-small cell lung cancer (SQ NSCLC). Ann Oncol, 2020;31:S878
-
36. Paz-Ares L. Ciuleanu TE, Yu X, Salman P. Pluzanski A. Nagrial A et al. Nivolumab (NIVO) + platinum-doublet chemotherapy (chemo) vs chemo as first-line (1L) treatment (tx) for advanced non-small cell lung cancer (aNSCLC): CheckMate 227 – part 2 final analysis. Ann Oncol, 2019;30:xi67-xi04
-
37. Reck M. Ciuleanu T-E. Dols MC, Schenker M, Zurawski B. Menezes J et al. Nivolumab (NIVO) + ipilimumab (IPI) + 2 cycles of platinum-doublet chemotherapy (chemo) vs 4 cycles chemo as first-line (1L) treatment (tx) for stage IV/recurrent non-small cell lung cancer (NSCLC): CheckMate 9LA. J Clin Oncol, 2020;38(15_suppl):9501-9501
-
38. Garassino M. Rodriguez-Abreu D. Gadgeel S. Esteban E. Felip E, Speranza G et al. Evaluation of TMB in KEYNOTE- 189: Pembrolizumab Plus Chemotherapy vs Placebo Plus Chemotherapy for Nonsquamous NSCLC. J Thorac Oncol, 2019;14(10):S216-S227
-
39. Garassino MC. Gadgeel SM. Rodriguez-Abreu D. Felip E. Esteban E, Speranza G et al. Evaluation of blood TMB (bTMB) in KEYNOTE-189: Pembrolizumab (pembro) plus chemotherapy (chemo) with pemetrexed and platinum vs. placebo plus chemo as first-line therapy for metastatic nonsquamous NSCLC. J Clin Oncol, 2020;38(15_suppl):9521-9521
-
40. Socinski MA. Mok TS. Nishio M. Jotte RM. Cappuzzo F. Orlandi F et al. IMpower150 final analysis: Efficacy of atezolizumab (atezo) + bevacizumab (bev) and chemotherapy in first-line (1L) metastatic nonsquamous (nsq) nonsmall cell lung cancer (NSCLC) across key subgroups. Cancer Res, 2020;80(16 Supplement):CT216
-
41. Reck M. Mok T, Socinski MA. Jotte R. Lim D. Cappuzzo F et al. IMpower150: Updated efficacy analysis in patients with EGFR mutations. Ann Oncol, 2020;31:S837-S807
-
42. Mazieres J. Kowalski D. Luft A, Vicente D, Tafreshi A. Gümüs M et al. Health-Related Quality of Life With Carboplatin- Paclitaxel or nab-Paclitaxel With or Without Pembrolizumab in Patients With Metastatic Squamous Non-Small- Cell Lung Cancer. J Clin Onccol, 2020;38(3):271-248
-
43. Borghaei H. Langer CJ. Paz-Ares L. Rodríguez-Abreu D. Halmos B. Garassino MC et al. Pembrolizumab plus chemotherapy vs. chemotherapy alone in patients with advanced non-small cell lung cancer without tumor PDL1 expression: A pooled analysis of 3 randomized controlled trials. Cancer, 2020;126(22):4867-4842
-
44. Waterhouse DM. Garon EB. Chandler J. McCleod M. Hussein M. Jotte R et al. Continuous Vs. 1-Year Fixed- Duration Nivolumab in Previously Treated Advanced Non-Small-Cell Lung Cancer: CheckMate 153. J Clin Onc10, 2020;38(33):3863-3831
Recibido: Marzo 9, 2021
Aceptado: Marzo 10, 2021
Correspondencia:
Jordi Remon
jremon@hmhospitales.com