Las células T con receptores de antígeno quimérico (CAR-T, por sus siglas en inglés) son linfocitos T que se recolectan de un paciente y son genéticamente alterados en el laboratorio para expresar un receptor modificado compuesto por dos elementos: el componente extracelular que funciona con la especificidad de un anticuerpo para reconocer un antígeno particular en la superficie de las células cancerígenas [Anticuerpo de cadena sencilla (scFV)] , y un componente intracelular , el receptor de célula T (TCR cc, por sus siglas en ingles “T cell receptor”) que activa la célula T (Figura 5).
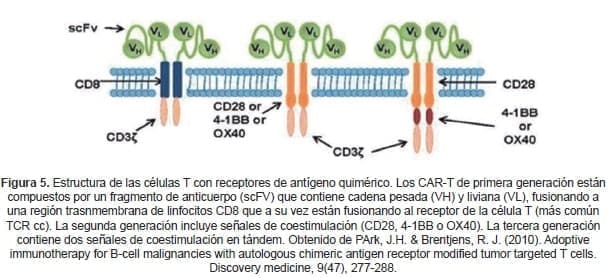
Cuando el anticuerpo de cadena sencilla encuentra el antígeno al cual está dirigido, se activa el TCR cc que a su vez inicia una cascada de activación del linfocito, sin necesidad de la coestimulación del complejo mayor de histocompatibilidad (CMH), esto genera la producción de citosinas, activa la señal para proliferación y expansión de las células CAR-T y causa la citotoxicidad directa contra el tumor (i.e perforinas y eje FAS/FAS ligando).
producción de las células de CAR-T
Las investigaciones que resultaron en la producción de las células de CAR-T llevan más de 60 años e iniciaron con el descubrimiento de las células T.
En 1961, el inmunólogo Jacques Miller estudiaba el timo durante su PhD en la Universidad de Londres, cuando descubrió que este órgano era responsable de producir linfocitos con características particulares para la defensa contra infecciones que luego nombró “linfocitos derivadas del Timo”(60), y hoy conocemos como Linfocitos T.
Los linfocitos T son células que se producen en la medula ósea que migran hacia el timo donde maduran y adquieren el TCR c en su membrana que permite reconocer antígenos (p.ej. péptidos de virus o bacterias) presentados por células del sistema inmune usando la interacción con el CMH en su membrana. La interacción entre el CMH, el TCRcc, el péptido presentado, y las señales de coestimulación producen la estimulación que ocasiona la activación de los linfocitos T.
Uno de los mayores avances en el conocimiento de las implicaciones de las células T en la inmunología tumoral surgió en 1986 cuando Steven Rosenberg publicó una investigación liderada en NIH, que demostró que las células T que infiltran algunos tumores podían aislarse a partir de una biopsia del tumor, expandirse en el laboratorio y curar algunos tumores al ser administradas al paciente con interleucinas (61).
Este descubrimiento demostró que el sistema inmunológico, liderado por las células T, podría jugar un papel importante en la inmunoterapia contra el cáncer. Los avances en la ingeniería genética en la década de los noventa hicieron posible esta idea.
Uno de los lideres principales, el Dr. Michel Sadelain, durante su tesis doctoral en el Instituto de tecnología de Massachusetts (MIT), demostró que era posible usar un vector como un virus retroviral o un lentivirus para introducir un nuevo gen en los linfocitos y manipular la expresión de este. Se demostró que era posible insertar una nueva proteína en el linfocito, como un receptor de membrana usando esta técnica. El código de la proteína es una secuencia de ARN, que se empaca en plásmidos y se inserta en el retrovirus y lentivirus modificados.
Después de que el virus infecta una célula y libera su material genético en ella, la cadena de ARN se transcribe por las enzimas del virus generalmente usadas para su replicación en una cadena de ADN. Este ADN se puede incorporar en el ADN del linfocito donde se inicia la trascripción y traducción de la proteína deseada; en el caso de células CAR-T un nuevo receptor de membrana con los dos componentes extracelulares e intracelulares descritos (scFV –TCR).
La primera célula T con receptor quimérico fue producida por los inmunólogos Zelig Eshhary Gideon Gross en 1993 en el Instituto de Ciencia Weizmann en Israel al insertar un receptor quimérico en el linfocito con una parte de un anticuerpo y fusionarla al receptor de la célula T (scFV -TCR) (62). Aunque no se pudo demostrar eficacia ni persistencia en los modelos animales de la primera generación de células CAR-T, estas en todo caso representan el inicio de esta revolución.
Para mejorar el modelo, era necesario superar dos desafíos principales: primero cómo activar y expandir las células CAR-T en el laboratorio independiente de células dendríticas y segundo, cómo mejorar la coestimulación de las células CAR-T para aumentar su activación y proliferación dentro del organismo.
Los primeros avances en el primer desafío se dieron al descubrir una nueva técnica para hacer cultivos celulares de linfocitos T infectados por el HIV.
Carl H. June y Bruce Levine, que iniciaron sus estudios en el Instituto Naval de Investigación de Medicina en EEUU y continuaron en la Universidad de Pensilvania, usaron una técnica con microperlas diminutas donde adicionaron en la superficie dos proteínas que imitaban moléculas de las células dendríticas (CD3/CD28).
Las células T al estar en contacto con las microperlas se activan y expanden, generando millones de copias que pueden permanecer vivas en cultivos celulares (63). Estos resultados reportados en 1996 fueron fundamentales para establecer los procesos de manufacturación de células CAR-T.
Por otro lado, para mejorar la activación y proliferación dentro del organismo se tuvo que investigar el papel que juegan las señales de coestimulación.
Los CAR-T de primera generación tenían solo CD3 ζ que resultó ser insuficiente para activar la célula T. En 1998, el Dr. Michel Sadelain en su laboratorio del Memorial Sloan Kettering (MSKCC) publicó la eficacia del receptor CD28 para permitir la activación de células T y aumentar la proliferación (64).
En el 2002, el laboratorio del Dr. Levine confirmó estos resultados y publicó sus estudios usando 4-1BB (65). Con esto se inició la creación de los CAR-T de segunda generación que poseen una co-estimulación interna (más frecuentemente CD28 o 4-1BB) fusionado a CD3 ζ. En el 2002 se desarrolló el primer modelo de segunda generación que mostró eficacia en célula CAR-T contra antígenos prostáticos por el equipo en MSKCC en Nueva York compuesto por Michel Sadelin, Renier Brentjens e Isabelle Rivière.
(Lea También: Cáncer de Pulmón de Células no Pequeñas)
En el 2003, el grupo de MSKCC, publicó el primer modelo de ratones usando células CAR-T de segunda generación dirigidos contra el antígeno CD19 – con CD28 que podían ocasionar muerte celular de tumores originados en células B (66).
Utilizar el antígeno CD19 resultó ser un blanco ideal por su frecuencia y alta expresión en tumores de células B. Además, el CD19 es requerido para el desarrollo normal de células B y no se expresa en otras células. Estos estudios preclínicos permitieron conducir ensayos clínicos utilizando este antígeno.
En el 2009, el equipo de MSKCC publicó su evidencia y validación de manufacturación de CAR-T CD19 (con coestimulación de CD28) para humanos y anunció el inicio de estudios clínicos fase 1 para leucemia linfocítica crónica y leucemia linfoblástica aguda de célula B (67).
Simultáneamente el equipo de la Universidad de Pensilvania con Carl June y David Porter iniciaron el primer ensayo clínico utilizando CAR-T contra CD19 (4-1BBB) en 3 pacientes con leucemia linfocítica crónica y en 2011 hacen el primer los primeros reportes con dos remisiones completas y una parcial (68),(69).
Estos estudios ofrecieron la evidencia necesaria para iniciar otros estudios de fase 1. Emily Whitehead, fue una de las primeras pacientes en el ensayo clínico del grupo de la Universidad de Pensilvania que incluyó pacientes con LLA tipo B con células CAR-T (4-1BBB) para pacientes pediátricos.
Su caso en el 2011 es mundialmente conocido porque después de la tercera infusión desarrolló hipertermia severa y coma, la causa en este entonces se desconocía. Se demostraron niveles de interleucina-6 extremadamente altos y el Dr. June decidió tratarla con tocilizumab, un anticuerpo contra el receptor de la IL-6, con el cual estaba familiarizado ya que su hija sufría de artritis reumatoide y era tratada con este medicamento. Después de la primera dosis, Emily Whitehead rápidamente respondió y despertó para su cumpleaños número 7.
Con este caso se empezó a reconocer los dos efectos adversos principales de las células de CAR-T ; el síndrome de liberación de citocinas (CRS por sus siglas en inglés, Cytokine release syndrome) y la neurotoxicidad (70).
Poco después el grupo de MSKCC, liderado por el Dr. Brentjens y Sadelain, publicaron su estudio clínico de CAR-T (CD19-CD28) para tratar la LLA de célula B en adultos (71).
Después de estos reportes, la revista Science anunció la inmunoterapia tumoral como el descubrimiento del año y la FDA designó un estatus de “innovación” a la investigación clínica dándole todo el soporte para acelerar el desarrollo de estas terapias. Esto generó un auge de estudio clínicos y, finalmente en el 2017 la FDA aprobó las células CAR-T de CD19. El producto de Novartis, desarrollado en colaboración con el grupo del Dr. June (Tisagenlecleucel-Kymriah), es CD19 con coestimulación de 4-1BB-CD3 para LLA refractaria o en recaída (menores de 25 años) y para linfoma difuso de células B. El otro producto de Kite/Gilead (Axicabtagene Ciloleucel-Yescarta), es CD19 con co-estimulación de CD28-CD3 ζ para linfoma difuso de células B.
Esta tecnología ha abierto nuevas oportunidades de tratamiento para pacientes que en su ausencia tenían muy pocas opciones terapéuticas y pronósticos inciertos.
En pacientes pediátricos, el 81% de los 75 pacientes con LLA en recaída o refractaria que fueron tratados en el ensayo clínico de fase 2 con Tisagenlecleucel, alcanzaron una respuesta completa (72). La supervivencia libre de progresión al año fue de 50% y la supervivencia global fue del 76%. Aunque el CRS severo (grado III/IV) ocurrió en el 73% de los pacientes, se demostró que el tocilizumab era efectivo. Los eventos neurológicos ocurrieron en el 40% de los pacientes y se trataron con cuidados de soporte.
Por otro lado, los pacientes adultos con linfoma difuso de células B en caída o refractario, tratados en los ensayos clínicos con Tisagenlecleucel o Axicabtagene ciloleucel han mostrado respuestas completas en alrededor del 50% y la supervivencia media libre de progresión para estos pacientes no se ha alcanzado. El CRS severo ocurre en menos del 20% de los pacientes y la neurotoxicidad ocurre en alrededor del 10% (73).
Actualmente la FDA está próxima a aceptar los nuevos CAR-T dirigidos al BCMA (antígeno de maduración de las células B) para pacientes con mieloma múltiple. En este momento hay cientos de ensayos clínicos dirigidos a múltiples antígenos para diferentes cánceres incluyendo tumores sólidos (p.ej. CD22, ERBB2/HER2, EGFR, entre muchos otros). Incluso, nuevos estudios están utilizando CAR-T generados en donantes sanos (CAR-T alogénico). La terapia celular ha avanzado significativamente en la última década y esperamos en los próximos años llevar nuevas opciones de tratamiento personalizado a los pacientes. En todo caso, el mayor desafío actual es poder disminuir el gasto de producción y llevar estas tecnologías mundialmente.
Conclusión
No hay duda de que los avances ocurridos en el siglo XX y en lo que va del XXI en las enfermedades hematolinfoides han mejorado significativamente la supervivencia de pacientes que, de otra forma, fallecerían prematuramente. Sin embargo, queda mucho por avanzar para ofrecer mejores esquemas de tratamiento que, integrando el conocimiento molecular, la inmunoterapia y la terapia dirigida, resulten no solamente en el aumento de la supervivencia, sino también en la mejora de la calidad de vida de los pacientes.
Referencias
-
1. Hütter G, Nowak D, Mossner M, Ganepola S, Müssig A, Allers K et al. Long-term control of HIV by CCR5 Delta32/ Delta32 stem-cell transplantation. N Engl J Med. 2009;360(7):692-8.
-
2. Bennett JH. Case of hypertrophy of the spleen and liver in which death took place from suppuration of the blood. Edinb Med Surg J. 1845;64,:413±23.
-
3. Virchow R. Weisses Blut und Milztumoren. Medicale Zeitung. 1847;16.
-
4. Thorburn AL. Paul Ehrlich: pioneer of chemotherapy and cure by arsenic (1854-1915). Br J Vener Dis. 1983;59(6):404-5.
-
5. Goodman LS, Wintrobe MM et al. Nitrogen mustard therapy; use of methyl-bis (beta-chloroethyl) amine hydrochloride and tris (beta-chloroethyl) amine hydrochloride for Hodgkin’s disease, lymphosarcoma, leukemia and certain allied and miscellaneous disorders. J Am Med Assoc. 1946;132:126-32.
-
6. Farber S, Diamond LK. Temporary remissions in acute leukemia in children produced by folic acid antagonist, 4-aminopteroyl-glutamic acid. N Engl J Med. 1948;238(23):787-93.
-
7. Pui CH, Evans WE. A 50-year journey to cure childhood acute lymphoblastic leukemia. Semin Hematol. 2013;50(3):185-96.
-
8. Freireich EJ, Gehan E, Frei E, Iii, Schroeder LR, Wolman IJ, Anbari R et al. The Effect of 6-Mercaptopurine on the Duration of Steroid-induced Remissions in Acute Leukemia: A Model for Evaluation of Other Potentially Useful Therapy. Blood. 1963;21(6):699-716.
-
9. Frei 3rd E, Karon M, Levin RH, Freireich EJ, Taylor RJ, Hananian J et al. The effectiveness of combinations of antileukemic agents in inducing and maintaining remission in children with acute leukemia. Blood. 1965;26(5):642-56.
-
10. Rodriguez V, Hart JS, Freireich EJ, Bodey GP, McCredie KB, Whitecar JR. JP et al. POMP combination chemotherapy of adult acute leukemia. Cancer. 1973;32(1):69-75.
-
11. Piller GJ. Leukaemia – a brief historical review from ancient times to 1950. Br J Haematol. 2001;112(2):282-92.
-
12. Smith MA, Altekruse SF, Adamson PC, Reaman GH, Seibel NL. Declining childhood and adolescent cancer mortality. Cancer. 2014;120(16):2497-506.
-
13. Hillestad LK. Acute Promyelocytc Leukemia. Acta Med Scand. 1957;159(3):189-94.
-
14. Breitman T, Collins S, Keene B. Terminal differentiation of human promyelocytic leukemic cells in primary culture in response to retinoic acid. Blood. 1981;57(6):1000-4.
-
15. Degos L, Wang ZY. All trans retinoic acid in acute promyelocytic leukemia. Oncogene. 2001;20(49):7140-5.
-
16. Antman KH. Introduction: the history of arsenic trioxide in cancer therapy. Oncologist. 2001;6 Suppl 2:1-2.
-
17. Bruserud O, Gjertsen BT, Huang T. Induction of differentiation and apoptosis- a possible strategy in the treatment of adult acute myelogenous leukemia. Oncologist. 2000;5(6):454-62.
-
18. Wang Z, Sun G, Shen Z, Chen S, Chen Z. Differentiation therapy for acute promyelocytic leukemia with all-trans retinoic acid: 10-year experience of its clinical application. Chin Med J (Engl). 1999;112(11):963-7.
-
19. Nowell PC. The minute chromosome (Phl) in chronic granulocytic leukemia. Blut. 1962;8:65-6.
-
20. Wong S, Witte ON. The BCR-ABL story: bench to bedside and back. Annu Rev Immunol. 2004;22:247-306.
-
21. Goldman JM. Chronic myeloid leukemia: a historical perspective. Semin Hematol. 2010;47(4):302-11.
-
22. McNicholl F. a history of haematology. from herodotus to hiv (oxford medical histories). Ulster Med J. 2017;86(1):50.
-
23. Konopka JB, Watanabe SM, Witte ON. An alteration of the human c-abl protein in K562 leukemia cells unmasks associated tyrosine kinase activity. Cell. 1984;37(3):1035-42.
-
24. Lichtman MA. A historical perspective on the development of the cytarabine (7days) and daunorubicin (3days) treatment regimen for acute myelogenous leukemia: 2013 the 40th anniversary of 7+3. Blood Cells Mol Dis. 2013;50(2):119-30.
-
25. Evans JS, Musser EA, Bostwick L, Mengel GD. The Effect of 1-β-D-Arabinofuranosylcytosine Hydrochloride on Murine Neoplasms. Cancer Res. 1964;24(7):1285- 93.
-
26. Schabel FM, Johnston TP, McCaleb GS, Montgomery JA, Laster WR, Skipper HE. Experimental Evaluation of Potential Anticancer Agents. VIII Effects of Certain Nitrosoureas on Intracerebral L1210 Leukemia. 1963;23(5):725-33.
-
27. Freireich EJ, Wiernik PH, Steensma DP. The Leukemias: A Half-Century of Discovery. J Clin Oncol. 2014;32(31):3463-9.
-
28. Carey RW, Ribas-Mundo M, Ellison RR, Glidewell O, Lee ST, Cuttner J et al. Comparative study of cytosine arabinoside therapy alone and combined with thioguanine, mercaptopurine, or daunorubicin in acute myelocytic leukemia. Cancer. 1975;36(5):1560-6.
-
29. Yates JW, Wallace HJ, Jr., Ellison RR, Holland JF. Cytosine arabinoside (NSC-63878) and daunorubicin (NSC- 83142) therapy in acute nonlymphocytic leukemia. Cancer Chemother Rep. 1973;57(4):485-8.
-
30. Winer ES, Stone RM. Novel therapy in Acute myeloid leukemia (AML): moving toward targeted approaches. Ther Adv Hematol. 2019;10:2040620719860645.
-
31. Hodgkin. On some Morbid Appearances of the Absorbent Glands and Spleen. Med Chir Trans. 1832;17:68-114.
-
32. Bonadonna G, Zucali R, Monfardini S, De Lena M, Uslenghi C. Combination chemotherapy of Hodgkin’s disease with adriamycin, bleomycin, vinblastine, and imidazole carboxamide vs. MOPP. Cancer. 1975;36(1):252-9.
-
33. Bonadonna G. Chemotherapy strategies to improve the control of Hodgkin’s disease: the Richard and Hinda Rosenthal Foundation Award Lecture. Cancer Res. 1982;42(11):4309-20.
-
34. Diehl V, Franklin J, Pfreundschuh M, Lathan B, Paulus U, Hasenclever D et al. Standard and Increased-Dose BEACOPP Chemotherapy Compared with COPP-ABVD for Advanced Hodgkin’s Disease. New England Journal of Medicine. 2003;348(24):2386-95.
-
35. Roullet MR, Bagg A. Recent insights into the biology of Hodgkin lymphoma: unraveling the mysteries of the Reed- Sternberg cell. Expert Rev Mol Diagn. 2007;7(6):805- 20.
-
36. Johnson P, Federico M, Kirkwood A, Fosså A, Berkahn L, Carella A et al. Adapted Treatment Guided by Interim PET-CT Scan in Advanced Hodgkin’s Lymphoma. N Engl J Med. 2016;374(25):2419-29.
-
37. Smith LH. Radiation Chimaeras.D. W. van Bekkum and M. J. de Vries. Academic Press, New York, 1967.x + 277 pp., illus. $20. Science. 1968;159(3812):294-5.
-
38. de la Morena MT, Gatti RA. A history of bone marrow transplantation. Immunol Allergy Clin North Am. 2010;30(1):1-15.
-
39. Thomas ED, Storb R, Clift RA, Fefer A, Johnson L, Neiman PE et al. Bone-marrow transplantation (second of two parts). N Engl J Med. 1975;292(17):895-902.
-
40. Mathé G, Amiel JL, Schwarzenberg L, Cattan A, Schneider M. Adoptive immunotherapy of acute leukemia: experimental and clinical results. Cancer Res. 1965;25(9):1525-31.
-
41. Bortin MM. A compendium of reported human bone marrow transplants. Transplantation. 1970;9(6):571-87.
-
42. Snell GD, Stevens LC. Histocompatibility genes of mice. III. H-1 and H-4, two histocompatibility loci in the first linkage group. Immunology. 1961;4(4):366-79.
-
43. Billingham RE, Brent L, Medawar PB. ‘Actively Acquired Tolerance’ of Foreign Cells. Nature. 1953;172(4379):603- 6.
-
44. Santos GW, Tutschka PJ, Brookmeyer R, Saral R, Beschorner WE, Bias WB et al. Marrow Transplantation for Acute Nonlymphocytic Leukemia after Treatment with Busulfan and Cyclophosphamide. N Engl J Med. 1983;309(22):1347-53.
-
45. Buckley RH. A historical review of bone marrow transplantation for immunodeficiencies. J Allergy Clin Immunol. 2004;113(4):793-800.
-
46. Epstein RB, Storb R, Ragde H, Thomas ED. Cytotoxic typing antisera for marrow grafting in littermate dogs. Transplantation. 1968;6(1):45-58.
-
47. Dausset J. [Presence of A & B antigens in leukocytes disclosed by agglutination tests]. C R Seances Soc Biol Fil. 1954;148(19-20):1607-8.
-
48. Ceppellini R, van Rood JJ. The HL-A system. I. Genetics and molecular biology. Semin Hematol. 1974;11(3):233- 51.
-
49. Aljurf M, Weisdorf D, Alfraih F, Szer J, Müller C, Confer D et al. “Worldwide Network for Blood & Marrow Transplantation (WBMT) special article, challenges facing emerging alternate donor registries”. Bone Marrow Transplant. 2019;54(8):1179-88.
-
50. Gluckman E, Rocha V, Boyer-Chammard A, Locatelli F, Arcese W, Pasquini R et al. Outcome of cord-blood transplantation from related and unrelated donors. Eurocord Transplant Group and the European Blood and Marrow Transplantation Group. N Engl J Med. 1997;337(6):373- 81.
-
51. de Witte T, Hoogenhout J, de Pauw B, Holdrinet R, Janssen J, Wessels J et al. Depletion of donor lymphocytes by counterflow centrifugation successfully prevents acute graft-vs.-host disease in matched allogeneic marrow transplantation. Blood. 1986;67(5):1302-8.
-
52. Daniele N, Scerpa MC, Caniglia M, Ciammetti C, Rossi C, Bernardo ME, et al. Overview of T-cell depletion in haploidentical stem cell transplantation. Blood Transfus. 2012;10(3):264-72.
-
53. Krause DS, Fackler MJ, Civin CI, May WS. CD34: structure, biology, and clinical utility. Blood. 1996;87(1):1-13.
-
54. Kessinger A. Utilization of Peripheral Blood Stem Cells in Autotransplantation. Hematol Oncol Clin North Am. 1993;7(3):535-45.
-
55. Weiden PL, Flournoy N, Thomas ED, Prentice R, Fefer A, Buckner CD et al. Antileukemic effect of graft-vs.-host disease in human recipients of allogeneic-marrow grafts. N Engl J Med. 1979;300(19):1068-73.
-
56. Kolb HJ, Mittermüller J, Clemm C, Holler E, Ledderose G, Brehm G et al. Donor leukocyte transfusions for treatment of recurrent chronic myelogenous leukemia in marrow transplant patients. Blood. 1990;76(12):2462-5.
-
57. Gatti RA, Meuwissen HJ, Allen HD, Hong R, Good RA. Immunological reconstitution of sex-linked lymphopenic immunological deficiency. Lancet. 1968;2(7583):1366-9.
-
58. Bach FH, Albertini RJ, Joo P, Anderson JL, Bortin MM. Bone-marrow transplantation in a patient with the Wiskott- Aldrich syndrome. Lancet. 1968;2(7583):1364-6.
-
59. Santos GW. Preparative regimens: chemotherapy vs. chemoradiotherapy. A historical perspective. Ann N Y Acad Sci. 1995;770:1-7.
-
60. Miller JF. Immunological function of the thymus. Lancet. 1961;2(7205):748-9.
-
61. Rosenberg SA, Spiess P, Lafreniere R. A new approach to the adoptive immunotherapy of cancer with tumorinfiltrating lymphocytes. Science. 1986;233(4770):1318- 21.
-
62. Eshhar Z, Waks T, Gross G, Schindler DG. Specific activation and targeting of cytotoxic lymphocytes through chimeric single chains consisting of antibody-binding domains and the gamma or zeta subunits of the immunoglobulin and T-cell receptors. Proc Natl Acad Sci U S A. 1993;90(2):720-4.
-
63. Levine BL, Cotte J, Small CC, Carroll RG, Riley JL, Bernstein WB, et al. Large-scale production of CD4+ T cells from HIV-1-infected donors after CD3/CD28 costimulation. J Hematother. 1998;7(5):437-48.
-
64. Krause A, Guo HF, Latouche JB, Tan C, Cheung NK, Sadelain M. Antigen-dependent CD28 signaling selectively enhances survival and proliferation in genetically modified activated human primary T lymphocytes. J Exp Med. 1998;188(4):619-26.
-
65. Maus MV, Thomas AK, Leonard DG, Allman D, Addya K, Schlienger K, et al. Ex vivo expansion of polyclonal and antigen-specific cytotoxic T lymphocytes by artificial APCs expressing ligands for the T-cell receptor, CD28 and 4-1BB. Nat Biotechnol. 2002;20(2):143-8.
-
66. Brentjens RJ, Latouche JB, Santos E, Marti F, Gong MC, Lyddane C, et al. Eradication of systemic B-cell tumors by genetically targeted human T lymphocytes co-stimulated by CD80 and interleukin-15. Nat Med. 2003;9(3):279-86.
-
67. Hollyman D, Stefanski J, Przybylowski M, Bartido S, Borquez-Ojeda O, Taylor C, et al. Manufacturing validation of biologically functional T cells targeted to CD19 antigen for autologous adoptive cell therapy. J Immunother. 2009;32(2):169-80.
-
68. Porter DL, Levine BL, Kalos M, Bagg A, June CH. Chimeric antigen receptor-modified T cells in chronic lymphoid leukemia. N Engl J Med. 2011;365(8):725-33.
-
69. Kalos M, Levine BL, Porter DL, Katz S, Grupp SA, Bagg A, et al. T cells with chimeric antigen receptors have potent antitumor effects and can establish memory in patients with advanced leukemia. Sci Transl Med. 2011;3(95):95ra73.
-
70. Grupp SA, Kalos M, Barrett D, Aplenc R, Porter DL, Rheingold SR, et al. Chimeric antigen receptor-modified T cells for acute lymphoid leukemia. N Engl J Med. 2013;368(16):1509-18.
-
71. Brentjens RJ, Davila ML, Riviere I, Park J, Wang X, Cowell LG, et al. CD19-targeted T cells rapidly induce molecular remissions in adults with chemotherapy-refractory acute lymphoblastic leukemia. Sci Transl Med. 2013;5(177):177ra38.
-
72. Maude SL, Laetsch TW, Buechner J, Rives S, Boyer M, Bittencourt H, et al. Tisagenlecleucel in Children and Young Adults with B-Cell Lymphoblastic Leukemia. N Engl J Med. 2018;378(5):439-48.
-
73. Neelapu SS, Tummala S, Kebriaei P, Wierda W, Gutierrez C, Locke FL, et al. Chimeric antigen receptor T-cell therapy – assessment and management of toxicities. Nat Rev Clin Oncol. 2018;15(1):47-62.
Recibido: Noviembre 10, 2020
Aceptado: Noviembre 27, 2020
Correspondencia:
Beatriz Wills-Sanín
willssab@mskcc.or