Actualidad Inmediata
Debido a la importancia de esta investigación y al impacto en el medio, presentamos un resumen de este artículo y los comentarios de la NAMS (Wolf Uthian), León Spèroff, Andrea Genazzani y Marco Gambacciani para información de nuestros afiliados y nuestros lectores y para poner en perspectiva el tema.
Aumento del riesgo de cáncer de seno y ECV en usuarias de TRH cuando se usa por más de 5 años
Risk and benefits of estrogen plus progestin in healthy postmenopausal women. Principal results from the Women´Health Initiative randomized controlled trial. JAMA2002 (July 17);188:321-33
Writing Group For The Women´S Health Initiative Investigators
El Women´s Health Initiative (WHI) está enfocado en definir los riesgos y beneficios de estrategias que potencialmente pueden reducir la incidencia de enfermedad cardiaca, cáncer de mama y colorrectal, y fracturas en mujeres postmenopáusicas. Entre 1993 y 1998, el WHI reclutó 161.809 mujeres postmenopáusicas entre 50 y 79 años de edad en un grupo de ensayo clínico (un grupo con dieta baja en grasa y suplementos de calcio y vitamina D), y 2 grupos de uso hormonal postmenopáusico en 40 centros clínicos de los Estados Unidos. En este artículo se informa de los principales resultados del esquema combinado estrógenos y progestinas en mujeres con útero conservado. El estudio fue suspendido en ese grupo basado en que los riesgos superaban los beneficios en un promedio de seguimiento de 5.2 años. Un grupo paralelo de estrógenos solos en pacientes histerectomizadas, continuó abierto hasta la fecha planeada en marzo del 2005 cuando el promedio de seguimiento será de alrededor de 8.5 años.
El WHI es un estudio randomizado controlado para prevención primaria. El objetivo principal fue la enfermedad cardiovascular ECV (infarto no fatal y muerte por ECV) y cáncer invasivo de mama como factor adverso primario.
En mayo 31 del 2002, después de 5.2 años de seguimiento, la comisión de datos y seguridad recomendó parar el estudio de estrógenos mas progestinas versus placebo porque el test estadístico para cáncer invasivo de mama excedía el tope para este efecto adverso y el índice global estadístico establecía un aumento de los riesgos sobre los beneficios. Este informe incluye datos de los parámetros clínicos mayores hasta abril 30, 2002. Los riesgos de peligro (HR) (95% índice de confiabilidad, IC) fueron: ECV 1.29 (1.02-1.63) con 286 casos; cáncer de mama 1.26 (1.00-1.59) con 290 casos; apoplejía cerebral 1.41 (1.07-185) con 212 casos; embolia profunda 2.13 (1.39-3.25) con 101 casos; cáncer colo rectal 0.63 (0.43-0.92) con 112 casos; cáncer endometrial 0.83 (0.47-1.47) con 47 casos; fracturas de cadera 0.66 (0.45-0.98) con 106 casos; y muerte por otras causas 0.92 (0.74-1.14) con 331 casos. El HR para variables combinadas fue 1.22 (1.09-1.36) para ECV total (enfermedad arterial y venosa), 1.03 (0.90-1.17) para total de cáncer, 0.766 (0.69-0.85) para fracturas combinadas, 0.98 (0.82-1.18) para mortalidad total y 1.15 (1.03-1.28) para el índice global. El exceso de riesgo absoluto por 10.000 personas año, atribuible a estrógenos mas progestinas fue de 7 eventos CV, 8 apoplejías, 8 embolias profundas, y 8 cánceres invasivos de mama, mientras la reducción absoluta de riesgos por 10.000 personas-año fue 6 cánceres colo-rectales y 5 fracturas de cadera. El exceso de riesgo absoluto incluido en el índice global fue 19 por 10.000 personas-año.Las conclusiones del estudio fueron que los riesgos excedían los beneficios cuando se usaba una combinación de estrógenos (0.625 mg EEC) mas progestinas (2.5 mg de AMP) por un promedio de 5.2 años de seguimiento en mujeres americanas postmenopáusicas. No todas las causas de mortalidad se vieron afectadas durante el estudio. La relación riesgos (ECV y cáncer de mama) deben sopesarse con relación a los beneficios (prevención de cáncer colorrectal y fracturas). Los resultados encontrados en este estudio no son consistentes con una intervención viable para prevención primaria de enfermedades crónicas, e indican que este régimen debería no iniciarse o continuarse para prevención primaria de ECV
Comentario 1
NAMS
Executive Director
El estudio Women Health Initiative, WHI, investigaba los efectos del régimen de TRH de 0.625 mg de estrógenos equinos conjugados, EEC y 2.5 m de acetato de medroxiprogesterona, AMP para prevención de enfermedad cardiovascular, ECV, en mujeres americanas jóvenes (entre 50 y 79 años). Después de 5.2 años de seguimiento, el estudio fue suspendido prematuramente con relación a lo planeado para las mujeres que usaban este esquema porque el aumento del riesgo de salud total (en particular, la tasa de cáncer invasivo de mama) excedía los beneficios. La conclusión fue que este tipo de régimen de TRH “no debería ser iniciado ni continuado para prevención primaria de ECV”.
Es un procedimiento estandarizado en un régimen combinado agregar un progestágeno (en este caso AMP) a toda mujer con útero para protegerla del aumento de riesgo de cáncer uterino asociado con el uso de estrógenos sin oposición. Después de una histerectomía está estandarizado el uso de estrógenos solos. En el WHI el grupo de estrógenos solos para mujeres sin útero no presentan significativos efectos adversos que requieran la terminación prematura del estudio.
Los resultados del estudio WHI y el del HERS II despiertan una seria preocupación en particular, para las mujeres posmenopáusicas. Para la mujer, nunca ha sido tan importante como ahora, discutir su caso específico con su proveedor de salud. Para las mujeres con útero intacto, hay otras opciones más apropiadas que la TRH para reducir el riesgo CV.
Al momento de detenerse el estudio, el WHI mostraba que las mujeres que usaban TRH tenían un aumento del 26% (que se traduce en 38 casos entre las usuarias de TRH vs. 30 casos entre el grupo placebo por 10.000 personas-año) para cáncer invasivo de mama. Sin embargo, no hubo diferencia significativa para cáncer de mama in situ. Aunque estudios previos han sugerido una asociación entre TRH y cáncer de mama, este primer estudio randomizado y controlado ha confirmado que la combinación EEC mas AMP aumenta la incidencia de cáncer de mama y cuantifica el grado de riesgo. Dados estos resultados, la definición de “por cuanto tiempo” se recomienda el uso a largo plazo, debe acortarse.
Una limitación importante del estudio WHI es el uso de un solo régimen de TRH. Así pues, los resultados no necesariamente son aplicables a dosis bajas de EEC y AMP, otros estrógenos y progestágenos orales, o estrógenos y progestágenos transdérmicos. Por lo tanto, aunque el estudio fue detenido prematuramente, no sabemos si en un estudio a más largo plazo se hubieran encontrado beneficios mas pronunciados, particularmente en la prevención de fracturas.
En el estudio WHI las tasas totales de eventos cardiovasculares fueron bajas para mujeres que usaban este régimen de TRH. Las que usaban TRH experimentaron un aumento de 29% en eventos CV comparados con placebo (lo cual se traduce en 37 casos entre las usuarias de TRH vs 30 casos entre las usuarias de placebo por 10.000 personas año). La mayoría del exceso fue en infarto del miocardio no fatal. Las tasas de apoplejía fueron del 41% mayor (29 vs 21 por persona año). Las tasas de tromboembolismo venoso fueron el doble del placebo (34 vs 16 por 10.000 personas-años).
Consistente con los estudios previos (HERS y PEPI), este régimen de TRH mostró una gran reducción en las LDL (-12.7%) un aumento en las HDL (7.3%) y triglicéridos (6.9%) en relación con el placebo.
A pesar de los hallazgos negativos, el WHI respalda los efectos benéficos de la TRH en el riesgo de fracturas osteoporóticas y cáncer colo-rectal. El estudio WHI es el primer ensayo con datos definitivos mostrando la prevención de fracturas asociadas con osteoporosis postmenopáusica (con 10 fracturas de cadera en usuarias de TRH vs 15 en usuarias de placebo por 10.000 personas-año). Las tasas de cáncer colo-rectal también fueron significativamente menores, reduciéndose en un 37% (10 para usuarias de TRH vs 156 para usuarias de placebo por 10.000 personas año). El cáncer endometrial, cáncer de pulmón, y la totalidad de los cánceres no fueron afectados. Esta publicación del WHI no considera en el análisis de los beneficios globales una variedad de otras condiciones que podían positiva o negativamente ser afectadas por la TRH, como cálculos biliares, diabetes, funciones cognitivas, y calidad de vida.
En las mujeres que están tomando EEC y AMP sólo para prevenir ECV podría eventualmente suspenderse la terapia. Las mujeres quienes están usando EEC y AMP u otra terapia combinada de TRH para recibir los beneficios diferentes a la prevención de ECV, van a necesitar una cuidadosa re evaluación de la razón primaria por la que están usando TRH, determinando si los beneficios potenciales exceden los riesgos potenciales. No se justifica en este momento cambiar la terapia en mujeres sin útero y que usan estrógenos solos.
Referencias
1. Grady D, Herrington D, Bittner V, et al, for the HERS Research Group. Heart and estrogen/progestin replacement study follow-up (HERS II): Part 1. Cardiovascular outcomes during 6.8 years of hormone therapy. JAMA 2002;288:49-57.
2. Hulley S, Furberg C, Barrett-Connor E, et al, for the HERS Research Group. Heart and estrogen/progestin replacement study follow-up (HERS II): Part 2. Non-cardiovascular outcomes during 6.8 years of hormone therapy. JAMA 2002;288:58-66.
3. Writing Group for the Women’s Health Initiative Investigators. Risks and benefits of estrogen plus progestin in healthy postmenopausal women: principal results from the Women’s Health Initiative randomized controlled trial. JAMA 288:321-333.
Comentario 2
Una iniciativa personal para la salud de las mujeres: análisis del WHI
Andrea Riccardo Genazzani
Editor in Chief
Marco Gambacciani
Menopause Clinic, Pisa Italy
En los Estados Unidos un estudio randomizado, controlado con placebo, doble ciego que evaluó el efecto de una combinación de estrógenos-progestágenos en mujeres postmenopáusicas fue suspendido después de 5.2 años (el Women´s Health Initiative, WHI), porque los riesgos fueron considerados más altos que los beneficios por un estrecho margen. Los resultados fueron publicados rápidamente por el JAMA (Journal of American Medical Association)1, Julio 17 vol 288, pág 321, 2002. El estudio fue realizado en 40 centros investigando los efectos de la terapia de reemplazo hormonal TRH, sobre la enfermedad cardiaca y el cáncer de mama, teniendo como puntos secundarios la incidencia de cáncer endometrial y cáncer colo-rectal y fracturas, en mujeres postmenopáusicas entre los 50 y 79 años de edad. De las 16.608 mujeres en el estudio, 8.506 fueron randomizadas a recibir estrógenos conjugados orales (EEC 0.625 mg/día) mas progestágeno (AMP 2.5 mg/día) y 8.102 a recibir placebo. Desafortunadamente este ensayo fue realizado en una población con características totalmente diferentes de aquellas consideradas como mujeres típicas para TRH. De hecho el WHI no se realizó en mujeres postmenopáusicas sanas como repetidamente se menciona en el trabajo y en el editorial anexo1-2. En este “estándar de oro” de investigación (los trabajos randomizados), la población no fue ideal para sacar resultados que “ayuden a la información médica práctica y sirva de ayuda para que millones de mujeres hagan un decisión crítica acerca de su salud, cuando están envejeciendo”. De hecho una vasta proporción de estas mujeres no fueron tan saludables como los autores dicen: 35% eran tratadas por hipertensión, 35% tuvieron sobrepeso (IMC 25-29) y 34% obesas (IMC >30), 4% eran diabéticas, 12.5% tenían colesterol elevado y requerían medicación, 6.9% usaban estatinas. Tal como se reportó en el trabajo escrito, el estudio WHI encontró un aumento del riesgo para cáncer de mama, ECV, apoplejía cerebral, y trombosis venosa profunda. Primero que todo el número pequeño de aumento en número de pacientes con cáncer de mama está en concordancia con estudio poblacionales previos3. Los resultados inesperados fueron el aumento de los eventos CV, en contraste a todas las evidencias experimentales y epidemiológicas de estudios observacionales que sugieren que la TRH puede reducir la enfermedad cardiaca coronaria4. Generalmente hablando, los datos de un estudio describen el riesgo para una población dada, y los datos reportados para la población no se refieren al exceso individual de riesgo para una mujer individualmente. Al suspender el estudio, los investigadores del WHI notaron que las mujeres usuarias de TRH mostraban un aumento del 26% (es decir, 38 casos entre usuarias de TRH vs 30 casos entre mujeres usuarias de placebo, por 10.000 personas-año) en cáncer invasivo de mama, sin observarse una diferencia significativa en cáncer de mama in situ, y 29% de aumento en eventos CV comparados con placebo (es decir, 37 casos entre el grupo de TRH vs 30 casos entre el grupo placebo por 10.000 personas-año). De acuerdo con los datos ya reportados de estudios experimentales, epidemiológicos, y observacionales4, el grupo tratado con TRH experimenta el doble de la tasa de tromboembolismo, comparado con el grupo placebo (34 vs 16 por 10.000 personas año). El cáncer endometrial, el pulmonar y los cánceres en general, no fueron afectados, como se conoce ya en la literatura3. La tasa de mortalidad general, la tasa de mortalidad por ECV o cáncer de mama no fue afectada por la TRH.
De acuerdo a los autores del WHI, los resultados de este ensayo indican que el promedio de riesgo en la mujer individualmente es 0.1% por año para cáncer de mama y similar a los ataques cardiacos y no hay cambio en las tasas de mortalidad y aún la tendencia en tasas de mortalidad es favorable a la TRH1. El WHI no considera, en su análisis riesgo-benéfico general, una variedad de otras condiciones que la TRH puede afectar positiva o negativamente, incluyendo cálculos biliares, diabetes, funciones cognitivas, y calidad de vida.
En las mujeres que nunca fueron tratadas con TRH antes de entrar al estudio, los 5.2 años de TRH no inducen a un exceso de riesgo de cáncer de mama. El aumento del riesgo fue evidente en mujeres quienes previamente se habían expuesto a hormonas por 5-10 años. La exposición previa a hormonas también puede jugar un papel importante en las tasa de fracturas. Las mujeres bajo TRH tenían una reducción del 34% en fracturas de cadera y 24% reducción total de fracturas. Es la primera evidencia sólida de un estudio randomizado que muestra que la TRH previene la ocurrencia de fracturas. Sin embargo, el efecto de 5.2 años de TRH fue sorprendente en esta población con un riesgo presumible muy bajo de fracturas (en base a la DMO). Mas aún, la tasa de fracturas puede haber sido influida positivamente por el hecho que un grupo de mujeres habían sido tratadas previamente con hormonas. Por otra parte, los datos de fracturas está en concordancia con la probada eficacia de la TRH en la prevención de la pérdida de hueso que puede llevar a osteoporosis como recientemente se demostró en un estudio clínico randomizado demostrando que tanto con dosis estándar como con dosis bajas de TRH se aliviaban los síntomas vasomotores y se prevenía la osteoporosis5-6. El WHI demuestra que la TRH puede determinar un 37% de reducción de cáncer colo-rectal. Ésta es una pieza importante de la información debido a la relevancia de este cáncer para la salud de las mujeres y su bienestar3.
Los autores sostienen que los resultados del WHI tienen una aplicación amplia. En contraste, nosotros creemos que las limitaciones de la edad, el estado de salud y otras características permanecen. El régimen de TRH consistía en una dosis diaria oral de 0.625 mg de EEC y 2.5 mg de AMP. Esta combinación es una de las más usadas alrededor del mundo particularmente en las mujeres postmenopáusicas para la prevención y tratamiento de los síntomas de la menopausia. Por lo tanto este tratamiento se ha dado a mujeres postmenopáusicas al menos 10-15 años más jóvenes que las del estudio WHI. Los datos del WHI y las recomendaciones posteriores pueden no aplicar a otras formas de TRH con diferentes estrógenos y progestágenos o inclusive a otras dosis de EEC y AMP. TRH es un nombre general, pero no todos los tipos de TRH son lo mismo. Primero que todo, diferentes grupos de edad tienen diferentes requerimientos de dosis de estrógenos, con mujeres mayores necesitando dosis bajas6-7. Básicamente en la clínica práctica, mujeres en el rango de edad similar a las integrantes del estudio WHI, no deberían haber sido tratadas con productos con una potencia similar a las drogas usadas en el estudio7, 9. Aunque los autores del WHI puntualizan que la decisión acerca de TRH debe ser personalizada, el manejo clínico de las participantes del WHI puede ser severamente criticada. Por ejemplo, ¿por qué mujeres de 79 años de edad fueron tratadas con dosis estándar de TRH? Nosotros nunca escogeríamos esa clase de combinación para nuestras pacientes mayores con esas características clínicas. Como ginecólogos endocrinólogos nosotros siempre hemos personalizado nuestras terapias, mucho antes de la publicación del WHI. En Europa, tenemos una docena de progestágenos diferentes, que pueden hacer la diferencia, lo mismo que diferentes estrógenos para usos orales, transcutáneos, transdérmicos, nasales y parenterales. El estudio WHI despierta serias preocupaciones sólo para ciertas mujeres postmenopáusicas: las obesas y las mayores de 65 años.
Los resultados del WHI no son ni mucho menos concluyentes, y no podemos hacer recomendaciones finales para el manejo clínico basados en un estudio con una población completamente diferente a la que vemos en nuestras clínicas. Usada por más de 60 años en más de 100 millones de mujeres postmenopáusicas, la TRH es una de las más usadas y estudiadas de todas las terapias con drogas. Como lo dice la NIH en las últimas declaraciones, para mujeres tomando una combinación de TRH para tratamiento a corto plazo de los síntomas, los beneficios superan los riesgos. Hay suficiente evidencia general que respalda el uso de TRH en individuos que necesitan hormonas para sus síntomas como, fogajes, sudoraciones nocturnas, sequedad vaginal asociada con la atrofia, calidad de vida y prevención de osteoporosis.
Los beneficios biológicos sobre la prevención cardiovascular no han sido respaldados por este artículo. Más que todo, los estudios clínicos randomizados no han podido ni pueden borrar los resultados de cantidad de datos experimentales, epidemiológicos y observacionales. Las posibles fallas en los estudios observacionales de TRH y enfermedad cardiaca coronaria, llevan a parte de la comunidad científica, a rechazar lo positivo de los hallazgos disponibles sobre TRH y ECV. Esos científicos sólo creen en ensayos clínicos randomizados asumiendo que ellos son “estándar de oro” y que las fallas son sólo para otros diseños de estudios. Grandes estudios observacionales tienen números suficientes para corregir las potenciales fallas, demostrando aún que la TRH es benéfica sobre los lípidos sanguíneos, la pared vascular y eventos cardiovasculares. El efecto negativo o nulo sobre la ECC reportada por el WHI como también la prevención secundaria por el HERS10-11 se puede explicar fácilmente por las características de la población del estudio (edad, estado de salud, medicaciones concomitantes). Estudios randomizados futuros sobre TRH son necesarios para prevención primaria y secundaria. Sin embargo, debemos subrayar que esos estudios deben ser realizados en mujeres que sean candidatas para TRH en la práctica clínica. Críticamente ellos deben incluir diferentes tipos y dosis de TRH.
Por el momento, las recomendaciones del WHI deberían ser usadas en una población similar a la incluida en este estudio. Para las mujeres mayores, dosis bajas de TRH han demostrado los mismos beneficios de altas dosis sobre el control subjetivo de los síntomas y particularmente la prevención de osteoporosis. El estudio WHI también incluye un brazo de estrógenos solos para mujeres histerectomizadas. El NIH estableció que no hay evidencia, al momento, de aumento del cáncer de mama en mujeres que toman estrógenos solos en este estudio. Ni se recomienda hacer ningún cambio en la terapia de mujeres histerectomizadas que están bajo estrógenos solos.
Referencias
1. Writing Group for the Women; Health Initiative Investigators. Risks and benefits of estrogen plus progestin in healthy postmenopausal women: principal results from the Women Health Initiative randomized controlled trial. JAMA 2002; 288: 321-333.
2. Failure of estrogen plus progestin therapy for prevention. JAMA 2002; 288: 366-68.
3. Genazzani AR, Gadducci A, Gambacciani M. Controversial issues in climacteric medicine II. Hormone replacement therapy and cancer. International Menopause Society Expert Workshop. 9-12 June 2001, Opera del Duomo, Pisa, Italy. Climacteric 2001; 4(3): 181-93.
4. Genazzani AR, Gambacciani M. Hormone replacement therapy: the perspectives for the 21st century. Cardiovascular disease and hormone replacement therapy. International Menopause Society Expert Workshop. 13-16 October 2000, Royal Society of Medicine, London, UK. Climateric 2000; 3(4): 233-40.
5. Lindsay R, Gallagher JC, Kleerekoper M, Pickar JH. Effect of lower doses of conjugated equine estrogens with and without medroxyprogesterone acetate on bone in early postmenopausal women. JAMA 2002; 287(20): 2668-76.
6. Gambacciani M, Monteleone P, Genazzani AR. Low-dose hormone replacement therapy: effects on bone. Climateric 2002 Jun; 5(2): 135-9.
7. Ettinger B. Personal perspective on low-dosage estrogen therapy for postmenopausal women. Menopause. 1999; 6: 273-276.
8. Lobo RA, Whitehead MI. Is low-dose hormone replacement therapy for postmenopausal women efficacious and desirable? Climacteric 2001; 4: 110-119.
9. Gambacciani M, Genazzani AR. Hormone replacement therapy: the benefits in tailoring the regimen and dose. Maturitas 2001; 40(3): 195-201.
10. Grady D, Herrington D, Bittner V, et al, for the HERS Research Group. Heart and estrogen/progestin replacement study follow-up (HERS II): Part 1. Cardiovascular outcomes during 6.8 years of hormone therapy. JAMA 2002; 288: 49-57.
11. Heart and estrogen/progestin replacement study follow-up (HERS II): Part 2. Non-cardiovascular outcomes during 6.8 years of hormone therapy. JAMA 2002; 288: 58-66.
Comentario 3
Concepto sobre el estudio WHI
León Speroff
En mayo 31 de 2002, el Consejo de Control de Datos y Manejo (Data And Safety Moni toring Board_DSMB) realizó su 10ª revisión provisional de los datos acumulados por el Estudio Women´s Health Initiative (WHI). El DSMB hizo dos recomendaciones las cuales fueron hechas públicas en julio 9/02: 1) Descontinuar el brazo del estudio el cual administraba diariamente la combinación de 0.625 mg. de Estrógenos Equinos Conjugados, EEC, y 2.5 mg de AMP o placebo, y 2) Continuar el brazo del estudio el cual daba estrógenos solos (EEC 0.625 mg/día) o placebo en mujeres histerectomizadas. El brazo del estudio con estrógenos y progestágenos combinados fue suspendido después de un promedio de 5.2 años de seguimiento (rango: 3.5_8.5 años), debido a un aumento de cáncer invasivo de mama, el cual casi llegó a alcanzar significancia estadística. Los resultados presentados fueron los siguientes:
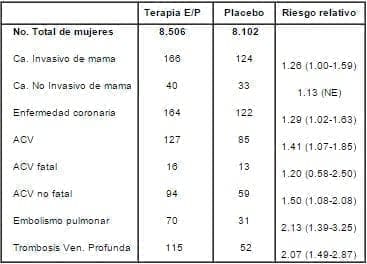
Estas cifras se refieren a riesgos atribuibles a la combinación de 0.625/2.5 de estrógenos conjugados/acetato de medroxiprogesterona, en dosis diarias así:

Otros resultados del brazo descontinuado del WHI con E/P diario, fueron:

El Estudio WHI colectó sus participantes entre 1993 y 1998 en 40 centros y estaba programado para terminar en 2005. Los parámetros estadísticos para daño o beneficio fueron establecidos en 1997, temprano en el estudio. Cuando el aumento en cáncer de mama sobrepasó los límites predeterminados, el DSMB se vio obligado a recomendar la suspensión de este brazo del estudio. El WHI concluyó que esta combinación de E/P no se debería prescribir o continuar para la prevención primaria de la Enfermedad Cardiaca Coronaria, ECC, y que ella conlleva un aumento sustancial de cáncer de mama (Writing Group for WHI Investigators) JAMA 2002; 288: 321-333.
Tomada en conjunto, esta decisión de terminar el brazo de terapia EP combinada del WHI, fue frustrante, perturbadora, importante y necesaria.
El Instituto Nacional del Corazón, los Pulmones y la Sangre, concluyó en su informe de prensa que es improbable que la terapia hormonal combinada beneficie al corazón. Desde mi punto de vista los resultados no justifican una conclusión definitiva. En primer lugar el WHI ha sido promovido como un ensayo clínico para la prevención primaria en mujeres sanas; sin embargo, la edad promedio de las participantes es 63 años y el rango de edades 50-79 (45% estaban en sus 60´s y 21% en sus 70´s). Aunque sólo el 7.7% de las mujeres informaron padecer enfermedad cardiovascular al ingreso, un número significante de las participantes tenían ya ateroesclerosis debido a su edad y nosotros estamos convencidos cada vez más de que los efectos benéficos de la terapia hormonal sobre el sistema cardiovascular disminuyen progresivamente a medida que aumente la aterosclerosis1. El aumento en eventos cardiovasculares en el grupo tratado ¿refleja un efecto concentrado en las pacientes mayores con ateroesclerosis significante? El WHI responde a esta crítica señalando una falta de interacción con la edad pero ésto aún no aclara el punto: en relación con la enfermedad cardiovascular este no fue un ensayo puro de prevención primaria.
La información proporcionada a partir del WHI no establece la prevalencia del uso de estatinas o de aspirina entre las participantes. Al respecto, un análisis año por año de la enfermedad cardiaca coronaria es de interés e importancia:
ECC

Es fácil observar que los resultados de la ECC están influenciados por los eventos del 5º año. ¿Qué paso en el año 5? Refleja ésto el uso de tratamientos nuevos con estatinas /aspirina en el grupo placebo, con disminución de la tasa de eventos y mostrando una falsa tasa alta en el grupo tratado? Aunque el uso de estatinas/aspirina en la línea de base fue comparable en el grupo tratado y en el grupo placebo, no se ofrece información acerca de nuevos tratamientos durante el periodo de seguimiento. Recordemos que hay una buena evidencia de que el efecto benéfico de los estrógenos sobre el sistema cardiovascular se pierde en mujeres tratadas con estatinas2. Con los pocos casos informados, la variación de unos pocos casos puede tener un impacto importante sobre las conclusiones.
Durante varios años, yo he sostenido que la falta de acuerdo, uniformidad y consistencia entre los más de 60 estudios de casos y controles y de cohorte son una fuerte razón para asumir que el riesgo de cáncer de mama asociado con terapia hormonal debe ser pequeño. Los resultados del WHI respaldan esta conclusión, mostrando un incremento del 26%, 8 casos por 10.000 mujeres por año. Más aún, yo he argumentado que aquellos estudios con un aumento en el riesgo podrían reflejar la aceleración hormonal del crecimiento en tumores preexistentes. ¿Es esa una posibilidad en los resultados del WHI? Una vez más, el análisis año por año es aquí útil:
Ca. mama

Es aparente que los resultados sobre cáncer de mama están fuertemente influenciados por los años 4 y 5. Recordemos que el crecimiento de los tumores de mama es lento (toma 10 años para que una neoplasia maligna alcance un diámetro de 1 cm. y pueda ser clínicamente detectable.
Los resultados del WHI sobre cáncer de mama son consistentes con una estimulación hormonal de tumores preexistentes. Nótese que el riesgo regresó a casi 1.0 en el año 6.
La salud de las participantes estará supuestamente vigilada hasta el año 2005 y por lo tanto, nosotros aprenderemos aún más acerca de esta posibilidad.
También es importante subrayar que una historia familiar para cáncer de mama no afectó los resultados.
Los estudios de casos y controles y de cohortes han mostrado en forma uniforme un riesgo disminuido de muerte por cáncer de mama en mujeres diagnosticadas durante la terapia hormonal. Ésto es debido no sólo al mayor empleo de la mamografía sino también a un menor grado y estadio de la enfermedad en las usuarias de hormonas, hallazgo consistente con el crecimiento acelerado de tumores preexistentes. En el estudio WHI sólo hubo tres muertes por cáncer de mama en el grupo tratado y dos en el grupo placebo; el seguimiento no fue lo suficientemente largo para mostrar el resultado de los casos de cáncer de mama entre las participantes.
Hay algunas buenas noticias. La reducción de fracturas osteoporóticas responde a quienes hacen énfasis en la falta de datos de estudios aleatorizados sobre el efecto de los estrógenos sobre la osteoporosis y las fracturas. La reducción del cáncer colo-rectal es consistente con una historia uniforme en un número grande de estudio de casos y controles. Es muy importante destacar que el brazo del estudio con sólo estrógenos se continúa porque no ha habido aumento de cáncer de mama. Ténganse también en la cuenta que el riesgo de trombosis venosa está concentrado en los dos primeros años de uso3 y entonces no existe razón para preocuparse por esta complicación infrecuente en usuarias a largo plazo.
¿Qué le diremos a las pacientes? Casi todas las pacientes habrán conocido ya los hechos, pronta y masivamente informados por los medios. Es adecuado puntualizar que el riesgo es pequeño y sin efecto mayor, pero desde luego esta información es de poco alivio para las pacientes.
La desparecida Trudy Bush siempre arguyó que el propósito de las ciencias básicas y clínicas es conocer la verdad. Y cada estudio epidemiológico, no importa cuán bueno o cuán largo sea, muestra sólo una cara de la verdad. Ella siempre llamó la atención acerca de que hacen falta muchos aspectos para alcanzar la verdad. El WHI es sólo una visión de la verdad. Los resultados pueden reflejar el uso de estatinas-aspirina y el efecto de la terapia hormonal sobre tumores preexistentes de cáncer de mama. Yo creo que es adecuado compartir con las pacientes estas explicaciones alternativas para los resultados del estudio WHI.
Referencias
1. Mikkola TS, Clarkson TB. Estrogen replacement therapy: atherosclerosis, and vascular function. Cardivoasc Res 2002; 53: 619.
2. Hodis NH, Mack WJ, Lobo RA, et al. Estrogen in the prevention of atherosclerosis; a randomized, double-blind, placebo-controlled trial. Ann Intern Med 2001; 135: 939-953.
3. Grady D, Wenger NK, Herrington D, et al. Postmenopausal hormone thrapy increases risk for venous thromboembolic disease: The Heart and Estrogen/progestin Replacement Study. Ann Intern Med 2000; 132: 696.
