El término estado cognitivo describe el grupo de procesos mentales por el cual el conocimiento es adquirido o usado. Acompaña destrezas mentales como concentración, aprendizaje y memoria, lenguaje, habilidades espaciales, juicio y razonamiento.
Las habilidades cognitivas cambian a través de la vida con el avance de la edad, las realizaciones tienden a declinar en muchos, aunque no en todos los test. La demencia es la disminución progresiva en la función cognitiva debido a cambios o enfermedad en el cerebro más allá de lo esperado por el envejecimiento normal. La enfermedad de Alzheimer (EA) es la causa más común de demencia.
Los problemas de memoria son más comunes en la edad mediana, pero los hallazgos en cohortes bien caracterizadas sugieren que la menopausia natural tiene poco efecto en la acción de la memoria u otras áreas de función cognitiva.
Limitados estudios clínicos pequeños entre mujeres posmenopáusicas más jóvenes sugieren que la TEP no tiene un impacto sustancial en el estado cognitivo después de la menopausia natural. Como se infiere de muy pequeños estudios a corto plazo, la TE iniciada rápidamente después de ooforectomía bilateral puede mejorar la memoria verbal. Varios estudios observacionales reportan no asociación entre la edad de la menopausia y la EA. Sin embargo, un estudio de casos y controles encontró que la ooforectomía bilateral antes de la menopausia estaba asociada con un riesgo elevado de trastorno cognitivo o demencia, y este riesgo aumentaba con lo más temprano de la ooforectomía.
Para mujeres posmenopáusicas de más de 60 años de edad, los hallazgos en estudios grandes, bien diseñados, indican que la TE/TEP no mejora la memoria u otras habilidades cognitivas.
Un estudio dentro del WHI, (Women‘s Health Initiative Memory Study, WHIMS) de mujeres de 65 a 79 años de edad reportó un aumento de la incidencia de demencia con uso TE y TEP. El estimado de casos de demencia atribuido a la TH fue de 12 por 10.000 personas año de uso de TE y 23 por 10.000 personas por año por uso de TEP.
En contraste, un número de estudios observacionales han reportado asociación entre el uso de TH y la disminución del riesgo de desarrollar EA. La exposición a TH en estudios observacionales comúnmente involucra a mujeres más jóvenes cerca de la menopausia que las mujeres elegidas en el WHIMS.
Especulativamente, esta diferencia implica una ventana temprana durante la cual el uso de TH podría reducir el riesgo de EA. Sin embargo, sesgos repetidos y sesgo de uso en mujeres sanas cuentan para la asociación protectiva en estudios observacionales, muchos de los cuales son difíciles de interpretar debido al escaso y pequeño número de participantes en los estudios.
La ventana de oportunidad es apoyada por una evidencia limitada, pero no hay datos de estudios clínicos que estudien a largo plazo las consecuencias cognitivas de la exposición a TE/TEP durante la transición menopáusica y la posmenopausia temprana. Para mujeres con EA, estudios clínicos limitados sugieren que la TH no tiene efectos sustanciales sobre los síntomas de demencia o su progreso.
Basados en estas consideraciones, la TH no puede ser recomendada a ninguna edad como indicación primaria de prevención del envejecimiento cognitivo o la demencia. La TH parece que aumenta la incidencia de demencia cuando se inicia en mujeres de 65 años o mayores. Similarmente, la TH no debería ser usada para aumentar la función cognitiva en mujeres posmenopáusicas con ovarios intactos, aunque algunos estudios clínicos pequeños apoyan el uso de TE inmediatamente después de menopausia inducida por ooforectomía bilateral. Los datos disponibles no estudian adecuadamente si la TH usada después de la menopausia aumenta o disminuye más tarde la demencia. Datos limitados no apoyan el uso de TH como tratamiento de la EA.
Menopausia prematura y falla ovárica prematura
Las mujeres que experimentan menopausia prematura (40 años) o son un grupo diferente que las mujeres que llegan a la menopausia a la edad típica de 51.3 años.
La menopausia prematura y la falla ovárica prematura están asociadas con un riesgo menor de cáncer de mama y un inicio más temprano de osteoporosis y ECV. Hay datos inadecuados acerca de TH en esas poblaciones. La mayoría de los reportes que sugieren un aumento del riesgo de ECV con la menopausia temprana natural o quirúrgica también sugieren un efecto protector de la TH. Los datos existentes acerca de TH en mujeres que tienen menopausia a la edad típica no deben ser extrapolados a mujeres que tienen menopausia prematura e inician TH a esa edad. Los riesgos atribuibles a la TH usada por mujeres jóvenes parecen ser menores y los beneficios potencialmente mayores que aquellos en mujeres que son mayores cuando comienzan la TH en o más allá de la edad típica de la menopausia, aunque no existen datos de estudios.
Mortalidad total
Los estudios del WHI son consistentes con los estudios observacionales indicando si la TH puede reducir la mortalidad total cuando se inicia pronto en la menopausia. El WHI sugiere en ambos brazos de TE y TEP que la mortalidad se reduce en un 30% cuando es iniciada a edades menores de 60 años y cuando se combinan los datos del RCT de TE y TEP, y que la reducción con el uso de TH fue estadísticamente significante. En contraste, la TH no estuvo asociada con reducción de la mortalidad entre mujeres que iniciaron la TH a los 60 o más años.
Efecto genérico versus producto específico
Estrógenos y progestágenos comparten algunas características y efectos comunes como también diferentes propiedades potenciales.
Sin embargo, los actuales estándares para determinar el objetivo clínico neto para cualquier agente dado (solo o en combinación) son a través de RCTs. En ausencia de RCTs rigurosos, cabeza-cabeza de varios estrógenos y progestágenos, los cuales no parecen estar haciendo nada, los clínicos van a tener que generalizar los resultados de estudios clínicos de un agente a todos los agentes dentro de una misma familia hormonal. En una base teórica, sin embargo, parece haber diferencias dentro de cada familia basado en factores como la potencia relativa del compuesto, androgenicidad, efecto glucocorticoide, biodisponibilidad y ruta de Administración
Indicación de progestágeno
La primera indicación relacionada con la menopausia para el uso de progestágeno es bloquear el riesgo aumentado de cáncer de endometrio por el uso sistémico de TE. A todas las mujeres con útero intacto que usan TE sistémica se les debe prescribir un progestágeno adecuado.
A las mujeres posmenopáusicas sin útero generalmente no se les debe prescribir un progestágeno con TE sistémico. Un progestágeno generalmente no está indicado cuando las bajas dosis recomendadas de TE se administran localmente para la atrofia vaginal. El progestágeno concomitante puede mejorar la eficacia de dosis bajas de TE para el tratamiento de los fogajes. Algunas mujeres que usan TEP pueden experimentar efectos secundarios indeseables del componente progestacional.
Dosis
La dosis efectiva más baja de estrógenos consistente con los objetivos del tratamiento, riesgo y beneficios de una mujer individualmente debe ser la meta terapéutica, con una correspondiente dosis baja de progestágeno que se agrega para contrarrestar los efectos adversos de la TE sistémica sobre el útero. La más baja TE y TEP son mejor toleradas y pueden tener más favorable relación beneficio-riesgo que las dosis estándar. Sin embargo, no se han probado dosis más bajas en estudios a largo plazo. Entre las dosis más bajas diarias típicamente usadas cuando se trata de TE sistémica están: 0.3 mg oral de EEC, 0.5 mg oral de 17estradiol micronizado y 0.014 a 0.025 mg de 17estradiol transdérmico en parche; la dosis de progestágeno varía de acuerdo al progestágeno usado y la dosis de estrógeno, típicamente comenzando con las dosis efectivas más bajas de 1.5 mg de AMP, 0.1 mg de acetato de noretisterona, 0.5 mg de drospierenona o 50 a 100 mg de progesterona micronizada.
Las diferentes dosis pueden tener diferentes resultados de salud. Algunas mujeres pueden requerir TE local para síntomas vaginales persistentes.
Vías de administración
No hay en la actualidad claros beneficios de una ruta de administración frente a otra para TE sistémica. Las rutas no orales pueden ofrecer ventajas o desventajas comparadas con la ruta oral, pero el riesgo-beneficio a largo plazo no se ha demostrado. Las diferencias podrían estar relacionadas con el papel del efecto del primer paso por el hígado, la concentración de hormona alcanzada en la sangre por una ruta dada, y la actividad biológica de los componentes. Hay evidencia observacional de que los TE transdérmicos pueden estar asociados a un menor riesgo de tromboembolismo venoso profundo (TEVP) (comparado con la ruta oral), pero no hay evidencia RCT. La administración local de TE es preferida cuando se tratan solo los síntomas vaginales.
Aunque es posible una absorción mínima sistémica, no hay reportes de efectos adversos. Los progestágenos sistémicos se necesitan para la protección endometrial de los TE sin oposición. La progesterona tópica no es recomendada (ver indicaciones de progestágenos, abajo).
Regímenes
Hay múltiples opciones de régimen de dosis para la seguridad endometrial cuando se agrega progestágenos a los estrógenos (ver tabla 3). La investigación no es adecuada para preferir uno u otro régimen.
Los datos actuales soportan la recomendación de minimizar la exposición de una o varias opciones. No hay evidencia suficiente en relación con la seguridad endometrial para recomendarcomo una alternativa a regímenes estándar de TEP de productos de venta libre o regímenes de ciclos largos, administración vaginal de progesterona, el contraceptivo intrauterino de levonorgestrel, o bajas dosis de estrógenos sin progestágenos.
Si cualquiera de las opciones anteriores es usada, se debe vigilar de cerca el endometrio, pendientes de más investigación, la cual está en progreso.
Hay múltiples opciones de regímenes de dosis de las cuales escoger cuando se usa TE sola para mujeres después de histerectomía; no hay datos que den guías sobre cuál es la mejor para las mujeres.
Tabla 3. Terminología de algunos tipos de regímenes de TEP.
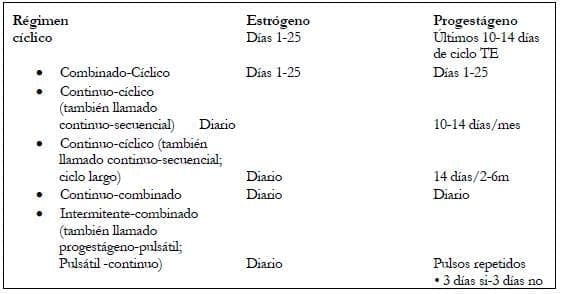
Hormonas bioidénticas
La NAMS reconoce que un área de confusión en la práctica clínica son las llamadas preparaciones hormonales bioidénticas.
Este término ha sido usado para referirse a muchos nombres de productos marcas muy bien probados por las agencias regulatorias que contienen hormonas químicamente idénticas a las hormonas producidas por la mujer (primariamente en el ovario), tales como el 17b estradiol o progesterona. Sin embargo, elnombre es más a menudo usado para escribir las formulaciones de fórmulas preparadas (llamadas terapia hormonal bioidéntica o BTH) que son hechas por un individuo de acuerdo a la prescripción de un proveedor.
Los compuestos preparados de TH pueden proveer diferentes dosis, ingredientes (p. ej. estriol) y rutas de administración, (p. ej. Implantes subdérmicos) que no están disponibles en el comercio, y terapia sin ingredientes no hormonales (p. ej. colorantes, preservativos) que algunas mujeres no pueden tolerar. El uso de BTH ha aumentado en los últimos años, a menudo con la dosis determinada por pruebas hormonales en la saliva, un procedimiento que no ha sido aprobado como seguro o confiable. Hay muchos riesgos para el paciente.
Las fórmulas de compuestos preparados incluyendo BTH, no han sido probadas para eficacia o seguridad; la información de seguridad no está consistentemente dada a los pacientes con su prescripción, como se requiere para la TH disponible comercialmente; la estandarización y pureza de cada lote producido puede ser incierta. La formulación de las preparaciones de drogas no está aprobada por ninguna oficina regulatoria, aunque algunos ingredientes cumplen las especificaciones de la farmacopea de EUA. Los costos son otro tema; como muchas preparaciones de fórmulas son vistas como drogas experimentales y no están cubiertas por la tercera parte de los que pagan, resultan en un alto costo para el paciente.
La US Food and Drug Administration (FDA) ha anunciado que las farmacias que preparan fórmulas han reclamado acerca de la seguridad y la efectividad de las que no están respaldadas por evidencia médica y lo consideraron falso y equívoco (ver la posición en www.fda.gov/ cder/pharmcomp/default).
Las farmacias pueden no hacer drogas que contienen estriol sin una nueva autorización investigativa. La FDA también establece que no hay bases científicas para usar la saliva para medir el ajuste de los niveles hormonales.
La NAMS recomienda que las prescripciones de BTH deben tener un inserto en el empaque, idéntico al que se requiere para productos que tienen probación por una agencia regulatoria. En el caso de falta de datos de eficacia y seguridad por cualquier prescripción específica, la relación riesgos-beneficios generales de los productos comerciales de TH disponibles se podría aplicar de forma similar a los productos BTH. Hay casos particulares de mujeres para las cuales los positivos exceden los negativos, pero para la vasta mayoría de mujeres, la TH aprobada por las agencias regulatorias va a proveer una terapia apropiada sin asumir los riesgos y costos de preparaciones según pedido (a la medida).
