La HAC se presenta como consecuencia de alteraciones enzimáticas en los diferentes niveles de la esteroidogénesis, siendo la más frecuente, en un 95%, la deficiencia de la 21-hidroxilasa y en segundo lugar la deficiencia de 11- hidroxilasa, trastorno que compromete la síntesis del cortisol en algunas pacientes o de cortisol y aldosterona en pacientes perdedoras de sal1 (Figura 4).
En esta entidad hay predominio de compuestos androgénicos delta 5, los cuales se aromatizan a nivel del sistema nervioso central, lo cual altera la pulsatilidad de la GnRH y por lo tanto de las gonadotropinas, produciendo niveles elevados de LH y disminución de la FSH; lo que genera alteración en la maduración folicular.
Al mismo tiempo los andrógenos adrenales alteran las aromatasas en el ovario, situación que se agrava por la disminución del factor de crecimiento insulinoide II (IGF-II) secundaria a la elevación de la ACTH, lo que genera disminución del crecimiento folicular, provocando grave compromiso de la esteroidogénesis e hiperandrogenismo y por lo tanto un cuadro compatible con un síndrome de ovario poliquístico (Figura 5).
Si extrapolamos los hallazgos informados por el grupo de Charmandari E10 en el 2004, donde se describe una mayor alteración endocrina en pacientes con HAC-clásica durante la época de la pubertad, como resultado del incremento de la hormona del crecimiento (GH) y del factor de crecimiento insulinoide I (IGF-I), fenómeno que desencadena disminución de la 11-hidroxilasa e impide la síntesis de cortisol, lo cual genera un mayor hipocortisolismo secundario.
Este proceso se agrava debido que la GH y el IGF-I incrementan la 17,20 desmolasa y disminuyen la 3 -hidroxi-esteroide deshidrogenada, lo cual genera mayor producción androgénica, y luego al incrementarse en la pubertad la excreción de metabolitos del cortisol por vía renal, fenómeno que es mayor que durante la prepubertad y la edad adulta. El mayor metabolismo del cortisol se hace a nivel hepático y menos del 1% se elimina directamente por el riñón (Figura 6). Además la vida media del cortisol es menor en la pubertad de las mujeres que en la pubertad de los hombres.
Tabla 3. Ejemplos de mutaciones del gen CYP21 que dan origen a la hiperplasia adrenal no clásica por deficiencia de 21-hidroxilasa9.
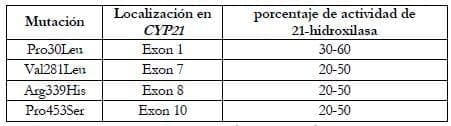
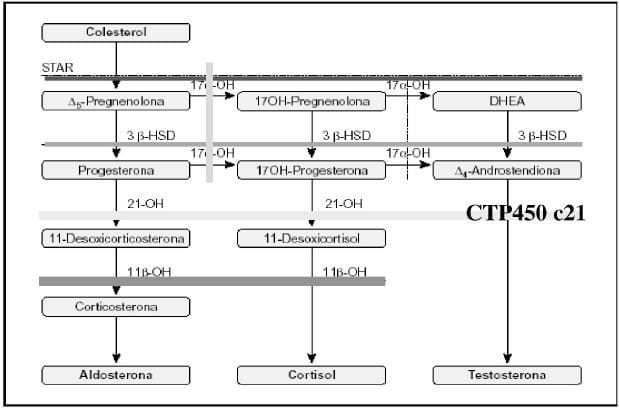 Figura 4.
Figura 4.
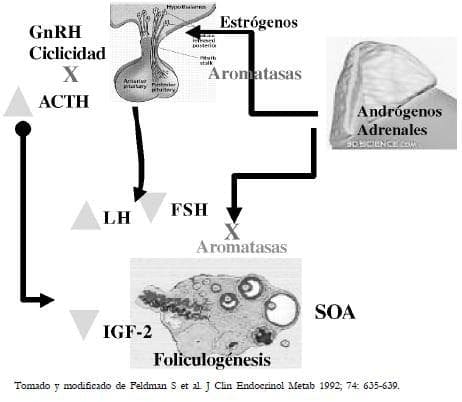 Figura 5.
Figura 5.
El aumento de GH, IGF-I e IGF II altera la esteroidogénesis adrenal y su respuesta a la ACTH, constituyéndose en un factor importante para el agravamiento del hiperandrogenismo, siendo mucho menor su acción a nivel ovárico.
Además el incremento de la IGF-I durante la pubertad se asocia a disminución de la sensibilidad e incremento de las concentraciones de insulina.
Todo este conjunto de eventos haría que las manifestaciones de hiperandrogenismo se agraven durante la adolescencia en pacientes con HAC-clásica y pudiera explicar también el inicio o el agravamiento de la HAC-NC en esta etapa, requiriéndose a veces una sustitución mayor con glucocorticoides.
Las pacientes con HAC-NC tienen un cuadro bioquímico caracterizado por cortisol y aldosterona normal, secundaria a la elevación de la ACTH, incremento moderado de la 17- hidroxiprogesterona y elevación de los andrógenos adrenales principalmente DHEAS y androstendiona en cantidades variables, de acuerdo al grado de compromiso enzimático.
Diagnóstico
Es importante diferenciar el diagnóstico etiológico de los estados de hiperandrogenismo debido a que: 1) el tratamiento del SOP y la HSC-NC es diferente, 2) el pronóstico reproductivo de las pacientes con HSC-NC tratadas adecuadamente es mejor, 3) es posible la consejería de las pacientes afectadas con HSC-NC, con respecto a la posibilidad de tener hijos(as) afectados con HSC o HSC-NC9.
En muchas pacientes los exámenes de laboratorio basales son normales y sólo en cerca del 10% se encuentra una 17-hidroxiprogesterona aumentada. Es por ello que en muchas oportunidades es necesario practicarles la prueba de estimulo con ACTH, la cual se considera como el mejor método para descartar o confirmar el diagnóstico. Los valores normales van de 0.1 a 1.2 ng/mL. Niveles menores de 2 ng/mL descartan el problema, niveles de 2 a 9 ng/mL son sospechosos y requieren la prueba de ACTH, y niveles iguales o mayores a 10 ng/mL son diagnóstico de la entidad.
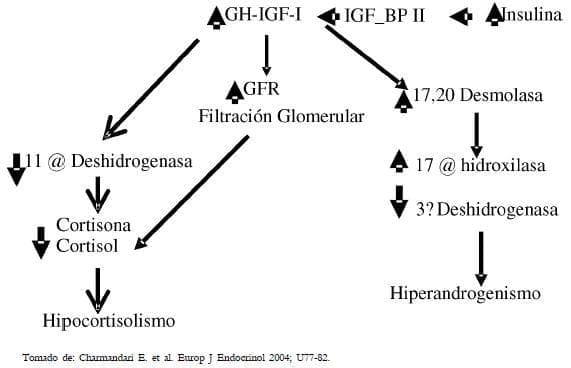
Figura 6.
Para la prueba de estímulo es necesario que cada laboratorio tenga un esquema estandarizado y validado para practicar la prueba a estas pacientes. El esquema más utilizado es la toma de una muestra basal entre los días 3 y 8 del ciclo normal o de un ciclo inducido (o en cualquier día sin inducción) en una paciente que ha estado en amenorrea; se practica en las horas de la mañana, antes de las 8 am, estando en ayunas, aunque algunos investigadores conceptúan que no lo requiere. Se toma una muestra basal y luego se aplican 0.25 mg (UI) IV o IM de ACTH acuoso con el nombre de Cortrosyn ®, que contiene los aminoácidos 1 a 24 de la hormona natural. La paciente debe permanecer en reposo y se toma una segunda muestra a los 60 minutos. Hay estudios que dicen que se puede tomar la muestra indistintamente a los 30, 60 ó 90 minutos. La respuesta después del estímulo es positiva para el diagnóstico de HAC-NC cuando se obtienen cifras mayores a 10 ng/mL 7, 11.
Los resultados de la 17-hidroxiprogesterona en la prueba de estímulo con ACTH permiten clasificar a las pacientes, de una forma aproximada, como normales cuando son menores a 100 ng/dL, portadoras cuando están entre 100 y 1000 ng/dL, HAC-NC entre 1000 y 10.000 ng/ dL, y HAC-clásica por encima de 10.000 ng/dL1 (Figura 7). En muestra médica usamos ng/mL.
