MARÍA CRISTINA FLORIÁN1, ALEJANDRO URIBE2, CLAUDIA PATRICIA CARDONA3
Palabras clave: tumor carcinoide; apendicitis; apendicectomía.
Resumen
Los tumores carcinoides del tracto gastrointestinal se originan de las células endocrinas situadas en las criptas de la mucosa del tubo digestivo, generalmente llamadas células de Kulchitsky. El apéndice es la localización más frecuente de los tumores carcinoides intestinales, seguido del intestino delgado, sobre todo el íleon, el recto, el estómago y el colon. El pico de incidencia se presenta en la tercera y cuarta décadas de la vida. Estos tumores se encuentran, aproximadamente,en una de cada 300 apendicectomías de rutina, su detección preoperatoria es rara y es el tumor más común del apéndice; casi siempre se descubre al estudiar una apendicitis. Generalmente, están localizados en la punta del apéndice.
Presentamos un caso de tumor carcinoide apendicular. El paciente era un hombre de 30 años de edad, al cual se le practicó una apendicectomía, al parecer, por un cuadro agudo de apendicitis. El resultado anatomopatológico confirmó un tumor neuroendocrino bien diferenciado de 1,2 cm de diámetro mayor con compromiso de toda la pared, incluida focalmente la serosa y el mesoapéndice, con presencia de invasión vascular tumoral, la base del apéndice libre de tumor, y una apendicitis aguda perforada. Se discute la conducta frente al hallazgo de dicho tumor.
Caso clínico
Se trata de un paciente de sexo masculino de 30 años de edad, previamente sano con un cuadro clínico de dos días de evolución de dolor abdominal de inicio agudo en la fosa ilíaca derecha, vómito e hiporexia. En los antecedentes personales refirió gastritis crónica no comprobada por estudios endoscópicos. Tomaba omeprazol ocasionalmente, autoformulado.
Desde cinco años antes había presentado episodios ocasionales de enrojecimiento facial, sensación de “calor” y sudoración, que no estaban asociados con la actividad física ni con los alimentos. Concomitantemente, presentaba de tres a cinco deposiciones diarias, blandas, sin sangre, sin moco, con dolor abdominal crónico y síntomas dispépticos frecuentes.
Fue valorado por cirugía general y se solicitaron exámenes de laboratorio, en los que se encontró: hemoglobina, 13,2 g/dl; hematocrito, 40,1%; leucocitos, 16.400 /mm3; neutrófilos, 89%; linfocitos, 6,2% y monocitos, 4%; recuento de plaquetas, 418.000/mm3; tiempo de protrombina (TP) de 12,4 segundos, con International Normalized Ratio (INR) de 1, y tiempo parcial de tromboplastina (TPT) de 26,8 segundos. En el examen parcial de orina no hubo hallazgos patológicos.
Fue programado para apendicectomía por el cuadro clínico muy sugestivo de apendicitis aguda. El informe quirúrgico reportó apendicitis gangrenada. Se practicó apendicectomía más drenaje de la peritonitis, sin complicaciones.
En el informe anatomopatológico se reportó el hallazgo de un tumor neuroendocrino bien diferenciado de 1,2 cm de diámetro mayor, con compromiso de toda la pared, incluida focalmente la serosa y el mesoapéndice, presencia de invasión vascular tumoral, con la base del apéndice libre de tumor, y apendicitis aguda perforada.
Según el informe de inmunohistoquímica, se observaban células tumorales positivas en forma difusa para la combinación de citoqueratina, sinaptofisina y cromogranina, ocasionalmente positivas para antígeno carcinoembrionario (CEA) y negativas para el factor de transcripción intestinal CDX-2. El índice de proliferación con el marcador ki 67 fue de 2%. El perfil obtenido confirmó el diagnóstico: carcinoma neuroendocrino bien diferenciado (carcinoide atípico).
En la valoración en consulta externa de medicina interna se encontró que habían desaparecido la diarrea crónica y la sensación de sofoco luego de dos meses de habérsele practicado el procedimiento quirúrgico, en el que se encontró tumor carcinoide de intestino medio de 1,2 cm de diámetro, con bajo riesgo de metástasis.
Se solicitaron los siguientes exámenes: marcadores de actividad tumoral o metastásica (cromogranina A-5 HIAA), endoscopia digestiva y tomografía computadorizada (TC) abdominal con contraste, con el fin de determinar la necesidad de tratamientos complementarios.
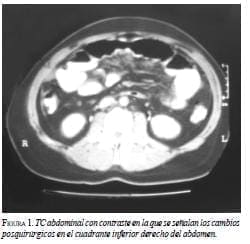
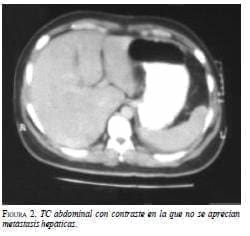
En la TC con contraste de abdomen se observó distensión de asas del íleon atribuible a íleo o a oclusión, líquido en la grasa de la gotera parietocólica y fascia lateroconal derecha, y edema en grasa pericecal; además, cambios posoperatorios en la pared abdominal del cuadrante inferior derecho (figuras 1 y 2).
En la esófago-gastro-duodenoscopia se informó gastritis aguda, gastritis crónica atrófica y presencia de Helicobacter pylori.
El valor de la cromogranina A fue de 19,4 ng/ml (valor normal, menos de 36,6 ng/ml) y el del ácido 5-hidroxi-indol acético (5-HIAA) de 6,7 mg en 24 horas (valor normal, 2 a 10 mg en 24 horas).
 |
 |
Dado el reporte negativo de los estudios para actividad tumoral, resaltando el valor negativo del ácido 5-hidroxi-indol acético, la desaparición del síndrome carcinoide, el tamaño de la lesión (1,2 cm) y la base apendicular libre de tumor, se determinó no realizar otros manejos quirúrgicos aparte de la apendicectomía. Asimismo, se definió hacer el seguimiento por consulta externa de medicina interna cada sexto mes. Hasta el momento, el paciente se encuentra asintomático, después del procedimiento quirúrgico practicado hace 20 meses.
Discusión
La primera descripción de las características del “carcinoide” se le atribuye a Lubarsh en el año 1888; poco después, en 1890, Obendorfert introdujo el término en un intento de destacar el comportamiento “benigno” de estos tumores, y no se le confirió importancia a su naturaleza maligna sino hasta finales del decenio de 1940, a pesar de que desde 1890 se conocía que producían metástasis (1,2).
Los tumores apendiculares tienen baja incidencia y el tumor carcinoide es el más frecuente (77,3%) de los carcinoides digestivos, seguido por el de intestino delgado (33,7%). La mayoría se diagnostica en el estudio anatomopatológico de la pieza de resección de pacientes intervenidos por apendicitis aguda (3,4), lo que resalta el valor del envío de las piezas al laboratorio de anatomía patológica (5,6).
Se presentan con una frecuencia cercana a 0,5% de todas las apendicectomías, con una incidencia anual de 1 en 100.000 habitantes por año (7,8). La edad de presentación se sitúa entre los 20 y los 40 años, edad de mayor concentración de las células argentafines en el organismo (9,10). Son neoplasias de origen neuroendocrino, en las células situadas en las glándulas de Lieberkhun, conocidas como células de Kulchitsky. Tienen la capacidad de secretar péptidos vasoactivos, 5-hidroxitriptamina, con efecto estimulante de los receptores alfa (11,12).
Frente a la distribución anatómica apendicular, se ubican por orden de frecuencia, así: sector distal, 75%; medio, 15%, y 10% en la base (13,14); 80% de los carcinoides apendiculares miden menos de 1 cm de diámetro, 14% miden entre 1 y 2 cm, y 6% miden más de 2 cm de diámetro. Raramente cursa con metástasis o síndrome carcinoide (15,16).En relación con las técnicas para el diagnóstico histológico, se utilizan dos procesos: 1) la técnica de Grinelius, que demuestra la característica argentafín de las células granulares de las criptas de Lieberkhun, 2) la cromogranina, que es una técnica de inmunohistoquímica específica, que ha ido desplazando a la anterior (17,18).
El estudio imaginológico convencional para la valoración de pacientes con tumor carcinoide apendicular es la tomografía computadorizada, simple o con contraste (19,20); sin embargo, se han incorporado nuevas técnicas a dicho estudio, entre ellas la gammagrafía de receptores de somatostatina (Octreoscan In111) y la tomografía por emisión de positrones (PET, Positron Emission Tomography), lo que representa un importante avance en el campo de las imágenes médicas, especialmente en oncología, por entregar información de tipo metabólico o molecular (21,22).
Cuando a esta última técnica se le incorpora en el mismo aparato un tomógrafo computarizado de múltiples cortes y un radionúclido, como el Ga68, se obtienen simultáneamente imágenes funcionales y anatómicas fusionadas conocidas como PET/CT Ga68 (23). Las características de este radionúclido permiten una adecuada marcación mediante un procedimiento simple de radioquímicos de péptidos análogos de la somatostatina, como el DOTA0-Tir3-octreotato (DOTATATE) (24,25).
Una vez que el radiofármaco es inyectado al paciente, se fija específicamente en las células que presentan aumento de la expresión de los receptores de somatostatina, como ocurre con los tumores neuroendocrinos y sus metástasis; este tipo de técnicas nos permitirían hacer diagnósticos y estratificaciones mucho más precisas y, de igual forma, la toma de decisiones terapéuticas acertadas (26,27).
El tratamiento de los tumores apendiculares depende de diversos factores: el diámetro del tumor, la localización dentro del apéndice, la profundidad de la infiltración local, la infiltración linfática, la presencia de metástasis, el tipo histológico y la edad del paciente; el diámetro tumoral es el factor pronóstico más importante para indicar el potencial de metástasis (28,29).
En los tumores menores de 1 cm de diámetro, el tratamiento de elección es la apendicectomía simple, mientras que en los tumores mayores de 2 cm se debe practicar una hemicolectomía derecha con disección de ganglios linfáticos. En los tumores entre 1 y 2 cm el tratamiento debe ser individualizado. Así, en tumores próximos a la base del apéndice, con invasión vascular o de los linfáticos de la submucosa o infiltración del mesoapéndice, se aconseja practicar una hemicolectomía derecha cuando se trata de pacientes jóvenes, mientras que, en pacientes mayores de 60 años o con elevado riesgo quirúrgico, el tratamiento recomendado es la apendicectomía. Algunos autores también recomiendan la hemicolectomía derecha en tumores malignos de alto grado y en adenocarcinoides con afectación difusa del apéndice. En presencia de metástasis en los ganglios linfáticos, se aconseja la hemicolectomía derecha, independientemente de la edad del paciente (30).
La frecuencia de metástasis es rara, sólo alrededor de 3% en el caso de lesiones de 2 cm de diámetro mayor, y pueden presentar amplia infiltración local. Un número todavía menor produce el síndrome carcinoide caracterizado por niveles elevados de serotonina en sangre y orina, que producen rubefacción, diarreas, broncoconstricción y cianosis; aparece en 1% de los enfermos y hasta en 20% de quienes tienen metástasis. Éstas se diseminan al hígado, el hueso y el pulmón; en estos casos está indicada la quimioterapia (31,32).
El pronóstico del tumor carcinoide apendicular es bueno, con una tasa de supervivencia a 5 años de 95% a 100% y una tasa de recidiva inferior a 1% (33).
Los tumores carcinoides malignos del apéndice son raros y difíciles de diagnosticar preoperatoriamente; es extremadamente importante el seguimiento de los pacientes con apendicitis aguda y las conclusiones del examen anatomopatológico, asimismo, incorporar las nuevas técnicas de imágenes diagnósticas a nuestro arsenal médico, dado que esto puede representar la toma de decisiones sobre procedimientos quirúrgicos óptimos para cada uno de los casos. El tratamiento adyuvante se debe considerar después de la evaluación oncológica para los pacientes con alteraciones hormonales debidas al síndrome carcinoide, lesiones metastásicas sintomáticas mensurables en el hígado o los pulmones, o recidivas locales tardías.
Carcinoid Tumor of the Appendix. Case Presentation
Abstract
The carcinoid tumors of the gastrointestinal tract originate in endocrine cells located in the crypts of the mucosa of the digestive tract, usually called Kulchitsky cells. The appendix is the most common site for the development of intestinal carcinoid tumors, which are usually located at the tip of the appendix; they also occur in the small bowel, especially the ileum, rectum, stomach and colon. The peak incidence is in the third and fourth decades of life. These tumors are found in about one of every 300 appendectomies, routine preoperative detection is rare, and they represent the most common tumor of the appendix. Almost always they are found as appendicitis.
We report a case of appendiceal carcinoid tumor. The patient is a male aged 30, which underwent appendectomy because of appendicitis. The pathology study confirmed a well differentiated neuroendocrine tumor of 1.2 cm in diameter with involvement of the entire wall including the serosa and focally the mesoappendix, tumor vascular invasion, base of the appendix free of tumor, perforated appendicitis. Behavior will be discussed against the findings of this tumor.
Key words: tumor carcinoide; appendicitis; appendectomy.
Referencias
1. Bronzino P, Cassinelli G, Cuneo A, Rassu PC, Partipilo F, Bianchi M, et al. Appendiceal carcinoid: Report of 3 clinical cases and review of the literature. G Chir. 2003;24:198-201.
2. Salinas AM. Estudio retrospectivo de cáncer de apéndice en el Instituto Oncológico Nacional “Dr. Juan Tanca Marengo”, SOLCA, Guayaquil, 1991-2002. Oncología. 2005;15:215-28.
3. Ordóñez NG, Rosai J. Gastrointestinal tract. En: Rosai J, editor. Ackerman’s Surgical Pathology. Eigth edition. St. Louis, MO: Mosby-Yearbook, Inc.; 1996. ¿Páginas?
4. Medina M, Carnicero JL. Tumor carcinoide psamomatoso del apéndice cecal. Patología. 1997;30:52-5.
5. Stinner B, Rothmund M. Neuroendocrine tumours (carcinoids) of the appendix. Best Pract Res Clin Gastroenterol. 2005;19: 729-38.
6. Uherek F, Barría C, Larraín C, Birrer E. Carcinoide apendicular. Comunicación de 6 casos y actualización del tema. Cuadernos de Cirugía. 2004;18:52-6.
7. Crawford JM. Aparato gastrointestinal. Cotran RS, Kumar V, Collins T, editors. Patología estructural y funcional. Sexta edición. Madrid: McGraw- Hill-Interamericana de España, S.A.U.; 1999;405,661-2.
8. Leotlela PD, Jauch A, Holtgreve-Grez H, Thakker RV. Genetics of neuroendocrine and carcinoid tumours. Endocr Relat Cancer. 2003;10:437-50.
9. Modlin IM, Lye KD, Kidd M. A 5-decade analysis of 13,715 carcinoid tumors. Cancer. 2003;97:934-59.
10. Moertel CG, Dockerty MB, Judd ES. Carcinoid tumors of the vermiform appendix. Cancer. 1968;21:270-8.
11. Roggo A, Wood WC, Ottinger LW. Carcinoid tumors of the appendix. Ann Surg. 1993;217:385-90.
12. Connor SJ, Hanna GB, Frizelle FA. Appendiceal tumors: Retrospective clinicopathologic analysis of appendiceal tumors. From 7,970 appendectomies. Dis Colon Rectum. 1998;41:75-80.
13.Ganim RB, Norton JA. Recent advances in carcinoid pathogenesis, diagnosis and management. Surg Oncol. 2000;9:173-9.
14. Rufini V, Calcagni ML, Baum RP. Imaging of neuroendocrine tumors. Semin Nucl Med. 2006;36:228-47.
15. Díaz JA, Vásquez J. Tumores carcinoides gastrointestinales en dos pacientes, Hospital Manuel Uribe Ángel de Envigado, Antioquia. Revista CES Medicina. 1999;13:80-3.
16. Sandor A, Modlin IM. A retrospective analysis of 1570 appendiceal carcinoids. Am J Gastroenterol. 1998;93:422-8.
17. Rindi G, Capella C, Solcia E. Pathobiology and classification of gut endocrine tumors. En: Mignon M, Coombel JF, editors. Recent advances in the pathophysiology and management of inflammatory bowel disease and digestive endocrine tumors. Paris: John Libbey Eurotext Publishing; 1999;177-91.
18. Esmer-Sánchez DD. Tumores apendiculares. Revisión clínicopatológica de 5.307 apendicetomías. Cir Ciruj. 2004;72:375-8.
19. Bodei L, Cremonesi M, Grana C, Rocca P, Bartolome IM, Chinol M, et al. Receptor radionuclide therapy with 90Y-[DOTA] 0- Tyr3-octreotide (90YDOTATOC) in neuroendocrine tumores. Eur J Nucl Med. 2004;31:1038-46.
20. Bremman WA, de Jong M, de Blois E, Bernard BF, Konijnenberg M, Krenning EP. Radiolabelling DOTApeptides with 68Ga. Eur J Nucl Med Mol Imaging. 2005;32:478-85.
21. Koukouraki S, Strauss LG, Georgoulias V, EIisenhut M, Haberkorn U, Dimitrakopoulou-Strauss A. Comparison of the pharmacokinetics of 68Ga-DOTATOC and [18F]FDG in patients with metastatic neuroendocrine tumours scheduled for 90YDOTATOC therapy. Eur J Nucl Med Mol Imaging. 2006;33: 1115-22.
22. Zhermosekov KP, Filosofov DV, Baum RP, Aschoff P, Bihl H, Razbash AA, et al. Processing of generator-produced 68Ga for medical applications. J Nucl Med. 2007;48:1741-8.
23. Breeman WA, Verbruggen AM. The 68Ge/68Ga generator has high potential, but when can we use 68Galabelled tracers in clinical routine? Eur J Nucl Med Mol Imaging. 2007;34:978-81.
24. Gabriel M, Decristoforo C, Kendler D, Dobrozemsky G, Heute D, Uprimny C, et al. 68Ga- DOTA-Tyr(3)-octreotide PET in neuroendocrine tumors: Comparison with somatostatin receptor scintigraphy and CT. J Nucl Med. 2007;48:508-18.
25. Mondragón SRJ, Castillero PC, Saldívar MC, Oñate OLF, Ruiz MJM, Aiello CV. Manejo del tumor carcinoide del aparato digestivo y del síndrome carcinoide. Rev Gastroenterol Mex. 1998;63:204-10.
26. O’Donnell ME, Carson J, Garstin WIH. Tratamiento quirúrgico de los tumores carcinoides malignos del apéndice. Int J Pract. 2007;61:431-7.
27. Kerström G, Hellman P, Hessman O. Management of midgut carcinoids. J Surg Oncol. 2005;89:161-9.
28. Wheeler MH, Maddox P, Maddineni S, Jordan S, Amer K, Butchart E. Surgical treatment of carcinoid tumours. Przegl Lek. 2000;57(Suppl.5):95-7.
29. Kawahara M, Kammori M, Kanauchi H, Noguchi C, Kuramoto S, Kaminishi M, et al. Immunohistochemical prognostic indicators of gastrointestinal carcinoid tumours. Eur J Surg Oncol. 2002;28:140-6.
30. Goede OC, Caplin ME, Winslet MC. Carcinoid tumour of the appendix. Br J Surg. 2003;90:1317-22.
31. Carr NJ, Sobin LH. Neuroendocrine tumors of the appendix. Semin Diagn Pathol. 2004;21:108-19.
32. MacGillivray DC, Heaton RB, Rushin JM, Cruess DF. Distant metastasis from a carcinoid tumor of the appendix less than one centimeter in size. Surgery. 1992;111:466-71.
33. Buchholtz M, Zúñiga JM, Valdés F, Fernández R. Carcinoide gastrointestinal. Experiencia de siete años en el Instituto Nacional del Cáncer (2000-2006). Revista Chilena de Cirugía. 2010;62:480-5.
1 Médica internista, intensivista; coordinadora, Unidad de Cuidado Intensivo, Hospital Departamental Santa Sofía de Caldas, Manizales, Colombia.
2 Médico internista, Unidad de Cuidado Intensivo, Hospital Departamental Santa Sofía de Caldas, Manizales, Colombia.
3 Médica cirujana, Unidad de Cuidado Intensivo, Hospital Departamental Santa Sofía de Caldas, Manizales, Colombia.
