¿Se puede prevenir el rechazo agudo celular y humoral en trasplante de intestino?
PRESENTACIÓN DE CASO
Anti-HLA antibody immunological follow up by the Luminex TM. Is it possible to prevent the acute cell and humoral immune rejection in small bowel transplant?
Report of one case
Gabriel J. Echeverri1, Luis Armando Caicedo1, Laura S. Thomas2, Adriana Villegas3,
Ana M. Aristizábal2, Catalina Gómez2, Víctor H. García2, María C. Pérez2,
Ana M. Arrunátegui4, Óscar Serrano1, Jorge I. Villegas1, Diego Jiménez5
1 Cirujano de trasplantes de órganos abdominales, Centro para la Investigación en Cirugía Avanzada y Trasplantes,
Universidad ICESI; Centro de Investigaciones Clínicas, Fundación Valle del Lili, Cali, Colombia
2 Médico en investigación, Centro para la Investigación en Cirugía Avanzada y Trasplantes, Universidad
ICESI; Centro de Investigaciones Clínicas, Fundación Valle del Lili, Cali, Colombia
3 Inmunología de Trasplantes, M. Sc., Fundación Valle del Lili, Cali, Colombia
4 Patóloga de trasplantes, Fundación Valle del Lili, Cali, Colombia
5 Medicina Interna, Gastroenterología, Fundación Valle del Lili, Cali, Colombia
Resumen
Introducción. El trasplante de intestino mejora la supervivencia de pacientes con falla intestinal secundaria al síndrome de intestino corto. Estos receptores tienen gran riesgo de rechazo agudo, por lo cual, de manera protocolaria y como método de referencia, se practican biopsias intestinales.
En este reporte de caso se hizo el seguimiento inmunológico de anticuerpos anti-HLA por tecnología Luminex™ (LSA) de un paciente con trasplante de intestino más biopsias por protocolo para un diagnóstico temprano, y una adecuada correlación histológica.
Presentación del caso. Se trata de un paciente de 20 años de edad con síndrome de intestino corto, que ingresó a la Fundación Valle del Lili (Cali, Colombia) y requirió un trasplante aislado de intestino.
El seguimiento inmunológico se hizo con tecnología Luminex™ y biopsias intestinales mensuales. Según la tamización contemplada en el protocolo previo al trasplante, el paciente tuvo anticuerpos anti-HLA (PRA de clase I y II) negativos; y a los 11 meses después del trasplante, los anticuerpos anti-HLA de clase I y II fueron positivos. Con la prueba de LSA se detectó un anticuerpo específico contra donantes (Donor Specific Antibodies, DSA) y varios anticuerpos contra otros subtipos moleculares.
Se tomó una biopsia que mostró un leve rechazo celular agudo y se inició tratamiento con plasmaféresis. Hasta 21 meses después del trasplante, el paciente no ha presentado rechazos clínicos y ha tenido una adecuada evolución clínica y paraclínica.
Conclusión. Este es el primer trasplante de intestino en nuestro centro, en el que se hace seguimiento inmunológico con tecnología Luminex™. Consideramos que la detección con DSA es un buen marcador de rechazo agudo humoral, que permitiría una aproximación diagnóstica y una intervención oportuna.
Palabras clave: intestino delgado; trasplante de órganos; antígenos HLA; antígenos de histocompatibilidad; inmunología del trasplante; rechazo de injerto.
Abstract
Background: Small bowel transplant improves survival of the recipients that have intestinal failure secondary to short bowel syndrome. These patients have a high risk of acute rejection; for this reason bowel biopsies are performed as protocol and is the gold standard. Immunological follow-up of anti-HLA antibodies with Luminex ® technology (LSA) was carried out in a patient with intestinal transplant and biopsies were performed to achieve an early diagnosis and a suitable histological correlation.
Case report: A 20-year-old patient with short bowel syndrome secondary to extensive intestinal resection due to a complicated appendicitis underwent isolated bowel transplantation. The post-transplant immunological follow-up was performed with LSA and monthly intestinal biopsies. Antibodies with mean fluorescence intensity greater than 1500 were positive. During the pre-transplant protocol, the patient was screened for anti-HLA antibodies with negative results. Eleven months post-transplant, the screening test for anti-HLA Class I and II antibodies was positive; the specificity of the LSA test detected one specific donor antibody (DSA) and several antibodies against other molecular subtypes. The biopsy result was a mild acute cellular rejection and plasmapheresis therapy was started. The patient has not presented a clinical rejection, and at 21 months post-transplantation exhibits an adequate clinical and paraclinical evolution.
Conclusions: This is the first small bowel transplant where immunological follow-up is done with LSA. We believe that the detection of DSA is a marker of acute humoral rejection that allows a diagnostic approach and a timely intervention.
Keywords: Intestine, Small; organ transplantation; HLA antigens; histocompatibility antigens; transplantation immunology; graft rejection.
Fecha de recibido: 30/05/2017 Fecha de aceptado: 07/07/2017
Correspondencia: Gabriel J. Echeverri, MD / Carrera 98 N° 18-49, Cali, Colombia / Teléfono: (572) 331-9090, extensión 7550 / Correo
electrónico: gjecheverri@hotmail.com
Citar como: Echeverri GJ, Caicedo LA, Thomas LS, Villegas A, Aristizábal AM, Gómez C, et al. Seguimiento inmunológico con anticuerpos
anti-HLA por tecnología Luminex™, ¿se puede prevenir el rechazo agudo celular y humoral en trasplante de intestino? Reporte de un caso. Rev Colomb Cir. 2018;33:100-6.
Introducción
El trasplante de intestino mejora la supervivencia y la calidad de vida de los pacientes con falla intestinal, la cual puede ser secundaria al síndrome de intestino corto o a una alteración de la motilidad 1. No obstante, los resultados a largo plazo son un reto debido al gran riesgo de rechazo agudo, por lo cual se debe hacer un seguimiento estricto del paciente con trasplante 2,3.
El rechazo agudo es una reacción inmunológica mediada por anticuerpos, linfocitos T o ambos. En el trasplante de intestino delgado hay un mayor riesgo de rechazo debido a la gran cantidad de tejido linfoide en la lámina propia, los ganglios linfáticos mesentéricos y las placas de Peyer 4. Actualmente, el estándar de referencia para el diagnóstico del rechazo agudo, es la evidencia histopatológica sumada a manifestaciones clínicas como fiebre, sangrado y síntomas gastrointestinales 5.
En muchas ocasiones, los anticuerpos anti-HLA son responsables de la disfunción y pérdida del injerto 6. El seguimiento con anticuerpos específicos contra donantes (Donor Specific Antibodies, DSA) para determinar si el paciente está cursando con un rechazo agudo mediado por anticuerpos, tiene un valor predictivo positivo del 44 % y un valor predictivo negativo del 85 % 7,8.
Un resultado positivo de DSA puede preceder los síntomas clínicos de rechazo crónico del injerto y se podría considerar como un factor predictivo de rechazo 9.
Actualmente, el diagnóstico de rechazo agudo de trasplantes mediado por anticuerpos se puede establecer por medio del DSA circulante, la presencia de C4d (producto de degradación del complemento), y las manifestaciones clínicas e histopatológicas 10. Las estrategias de manejo cuando el DSA es positivo incluyen plasmaféresis e inmunoglobulinas, ante la sospecha de un rechazo humoral 8.
Se han realizado varios estudios observacionales en los cuales se asocia la presencia de DSA de novo con la aparición de rechazo agudo temprano; los factores de riesgo para la formación de estos anticuerpos son eventos sensibilizantes previos, incompatibilidad del HLA y pobre observancia del tratamiento inmunosupresor 11,12.
En este caso, se hizo el seguimiento inmunológico de anticuerpos anti-HLA en un paciente con trasplante de intestino delgado, por medio de tecnología Luminex™ (LSA). Inicialmente, se utilizó una prueba de tamización (LIFECODES LifeScreen Deluxe) y, después, para determinar la especificidad de los anticuerpos detectados, se utilizó la prueba de antígeno único por Luminex™ (LSA Clase I, LSA Clase II, Immucor), para lograr un diagnóstico temprano y una adecuada correlación histológica, con el fin de impactar en la supervivencia del paciente y del injerto.
Un resultado mayor de 1.500 de los anticuerpos con intensidad media de fluorescencia, se consideró positivo para anticuerpos anti-HLA del donante, lo que en la literatura científica mundial corresponde a un paciente con gran riesgo inmunológico o hipersensible.
Presentación del caso
Se trata de un paciente de sexo masculino de 20 años de edad, con antecedentes de apendicitis complicada y laparotomía por peritonitis.
Ingresó inicialmente a otra institución por un cuadro clínico de dolor abdominal súbito, intenso, asociado a náuseas y deposiciones blandas, cuya radiografía de abdomen mostró niveles hidroaéreos, por lo que consideraron el diagnóstico de obstrucción intestinal. No hubo una adecuada respuesta al tratamiento farmacológico, por lo cual fue sometido a cirugía. Durante la intervención, se encontró isquemia intestinal por trombosis mesentérica, lo que requirió una amplia resección intestinal.
El paciente fue remitido a nuestra institución para su manejo multidisciplinario, y requirió múltiples reintervenciones quirúrgicas. Durante la cirugía se observó isquemia intestinal por trombosis venosa mesentérica con isquemia intestinal generalizada, lo cual requirió una amplia resección intestinal; primero, se resecaron 210 cm desde una distancia aproximada de 5 cm del ángulo de Treitz, y se dejaron 130 cm, y después, se resecaron casi 50 cm de íleon, a partir de una distancia de 10 cm de la válvula ileocecal.
Se diagnosticaron falla intestinal, síndrome de intestino corto, gastroparesia grave y desnutrición proteico-calórica. Asimismo, durante la hospitalización presentó múltiples complicaciones, entre estas, una sepsis por Candida spp. Asociada a infección del catéter central de nutrición. Se inició nutrición parenteral total que se prolongó durante 27 días de hospitalización, debido a que la lejanía de su residencia imposibilitaba el manejo domiciliario. Por el cuadro clínico del paciente, los Servicios de Gastrohepatología y de Cirugía de Trasplante, en conjunto, decidieron su ingreso a la lista de espera para trasplante aislado de intestino.
Según la tamización contemplada en el protocolo previo al trasplante, se solicitaron el perfil infeccioso, la prueba cruzada por CDC (citotoxicidad dependiente de complemento) para linfocitos T y B, y una prueba de tamización para anticuerpos anti-HLA (PRA de clase I y II negativo), cuyos resultados fueron todos negativos.
Antes del trasplante, recibió 2 mg/kg de timoglobulina, esteroides y profilaxis antimicrobiana. Después de seis días en lista de espera, se llevó a cabo el trasplante de intestino delgado de donante cadavérico (tiempo de isquemia en frío de 4,5 horas). Se encontró la cavidad peritoneal completamente bloqueada por adherencias y se practicó una yeyunostomía de tipo Witzzel, sin que se presentaran complicaciones.
Se inició el protocolo de inmunosupresión con timoglobulina (2 mg/kg), tacrolimus (3 mg), azatioprina (50 mg) y prednisolona (5 mg); además de profilaxis con ganciclovir (500 mg), fluconazol (200 mg) y trimetoprim-sulfametoxazol (160/800 mg).
Se hicieron estudios de extensión para determinar la posible etiología del episodio trombótico mesentérico. No obstante, se descartaron trastorno autoinmunitario, procoagulante u otras alteraciones, por lo cual, finalmente, se diagnosticó un episodio trombótico mesentérico idiopático.
Durante el seguimiento clínico y paraclínico, se encontraron los niveles de tacrolimus entre los límites normales, la carga de virus Epstein- Barr fue menor de 500 copias/ml, la carga para citomegalovirus no fue detectable y la prueba LSA fue negativa (5,7 g/dl). A los 40 días después del trasplante, se logró la tolerancia a la vía oral, la gastrostomía no mostraba producción y había deposiciones, por lo cual se decidió suspender la nutrición parenteral.
El seguimiento inmunológico posterior al trasplante se hizo mediante tecnología Luminex ™ (LIFECODES LifeScreen Deluxe, LSA Clase I, Clase II) y biopsias intestinales mensuales por endoscopía y mediante el uso de la técnica quirúrgica de ileostomía en T invertida o ‘chimenea’ (chimney). La biopsia de un mes después del trasplante demostró cambios leves de reperfusión, sin evidencia de rechazo agudo; el C4d fue negativo en los capilares de la mucosa, y negativo para displasia o neoplasia maligna.
A los 11 meses después del trasplante (enero de 2016), continuaba su tratamiento inmunosupresor con dosis diarias de prednisolona (5 mg), tacrolimus (10 mg) y everolimus (3 mg). Se obtuvo un resultado positivo en la prueba de tamización para anticuerpos anti-HLA de clase I y II. Con la prueba de especificidad LSA, se detectó un anticuerpo específico contra donante y varios anticuerpos contra otros subtipos moleculares; este fue el único momento en que la prueba LSA fue positiva (tabla 1, figura 1).
[enc_su_row][enc_su_column size=”1/2″ center=”no” class=””]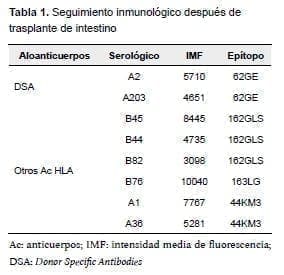 [/enc_su_column] [enc_su_column size=”1/2″ center=”no” class=””]
[/enc_su_column] [enc_su_column size=”1/2″ center=”no” class=””]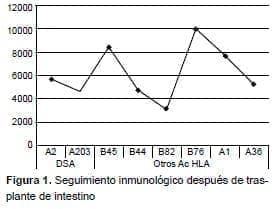 [/enc_su_column][/enc_su_row]
[/enc_su_column][/enc_su_row]
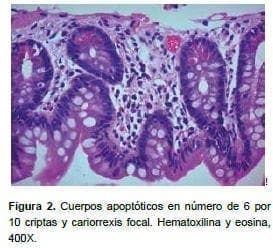
Se practicaron exámenes de extensión: niveles de tacrolimus (4,7 ng/ml) y everolimus en sangre total (4,4 ng/ml). Debido a esto, se decidió tomar una biopsia por endoscopia, en la cual se observaron células inflamatorias de tipo linfoplasmocitario en las criptas, con cuerpos apoptóticos en número de 6 por 10 a 12 criptas y cariorrexis focal; de acuerdo con la clasificación de Phillip Ruiz (2004), se consideró como un leve rechazo celular agudo (figura 2).
Con todo lo anterior, se hizo diagnóstico presuntivo de rechazo celular agudo y el paciente recibió tratamiento con seis sesiones de plasmaféresis y gammaglobulina hiperinmune (100 g/día).
Después del tratamiento se obtuvo mejoría clínica y paraclínica: en la biopsia de control se encontró infiltrado linfoplasmocitario en la lámina propia, sin eosinófilos, arquitectura conservada, cuerpos apoptóticos en número de 2 por 10 a 12 criptas y cariorrexis focal, sin evidencia histológica de rechazo. De acuerdo con la clasificación de Phillip Ruiz (2004) se consideró como indeterminado para rechazo celular agudo, por lo cual se iniciaron nuevamente everolimus (3 mg), prednisolona (40 mg) y tacrolimus (10 mg), y se dio de alta con seguimiento clínico y biopsia de control a los 15 días.
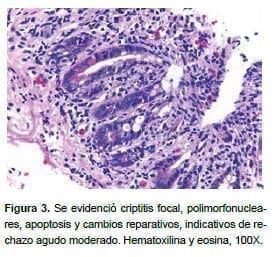
A los 18 meses después del trasplante (junio de 2016), se practicó una biopsia protocolaria, en la cual hubo cambios indicativos de rechazo agudo moderado, por lo que requirió nuevamente tratamiento con plasmaféresis (figura 3).
En la actualidad, 24 meses después del trasplante, el paciente ha tenido una adecuada evolución clínica y paraclínica; asimismo, la prueba LSA continúa siendo negativa.
Discusión
El rechazo agudo después de un trasplante de intestino es una complicación que afecta tanto al paciente como al injerto, lo cual genera una necesidad de vigilancia continua. En pacientes con sospecha de rechazo humoral y antecedentes de una prueba negativa para anticuerpos anti-HLA, se puede hacer el seguimiento del trasplante utilizando la prueba de tamización con tecnología Luminex™. En caso de tener una prueba para LSA positiva, se determina la especificidad para DSA y, así, se hace una intervención oportuna para el paciente.
La tecnología Luminex™ es un método no invasivo, muy sensible y especifico 8. En este reporte, se expone un caso de trasplante de intestino delgado debido a síndrome de intestino corto, al cual se le hizo seguimiento inmunológico de anti-HLA por Luminex™. Según nuestro conocimiento, este es el primer trasplante de intestino con este tipo de seguimiento inmunológico en Colombia.
El paciente ha tenido una adecuada evolución y no ha presentado rechazo clínico; además, se logró hacer un diagnóstico temprano de rechazo agudo del injerto mediado por anticuerpos con correlación histológica y, asimismo, se inició de manera temprana el tratamiento.
En los pacientes con evidencia clínica o subclínica de rechazo agudo y prueba positiva de DSA, que tengan biopsia negativa para rechazo, se debería iniciar tratamiento contra el rechazo. Su éxito se puede comprobar con la disminución en los valores de intensidad media de fluorescencia de los DSA o su desaparición, y la mejoría en la función del injerto 13. En el caso de este paciente, los resultados para anticuerpos anti-HLA y DSA fueron negativos después del tratamiento.
En un estudio de Gerlach, et al., se encontró una asociación entre los anticuerpos anti-HLA de novo en pacientes con trasplante de intestino y el rechazo humoral agudo; la formación de los anticuerpos DSA de novo se dio en los primeros seis meses después del trasplante 12. Durante el rechazo agudo mediado por anticuerpos, se activan respuestas de rechazo humoral y celular secundario a la cooperación BT, lo cual genera un mayor daño en el injerto. Por lo tanto, se puede considerar que los anticuerpos anti-HLA son un biomarcador para rechazo agudo del injerto de tipo celular 12,14.
Kuba, et al., no encontraron asociación entre los anticuerpos preformados y el cuadro clínico de los pacientes; no obstante, sí hubo una tendencia a la pérdida del injerto debido a rechazo agudo, con la aparición por primera vez de anticuerpos circulantes inmediatamente después del trasplante 15.
Tsai, et al., hicieron un estudio de pacientes sometidos a trasplante aislado de intestino o multivisceral.Hubo 6 trasplantes de intestino aislado, 2 de los cuales presentaron episodios de rechazo clínico y se asociaron con la presencia de DSA (p = 0,041). Además, obtuvieron 291 biopsias de íleo y se relacionaron con los DSA; en el 21,6 % de las biopsias se encontró rechazo agudo y una asociación positiva entre los resultados de la biopsia y la presencia de DSA (kappa=0,30). Por lo anterior, concluyeron que el aumento de los DSA debe alertar sobre la presencia de rechazo agudo 4.
Se ha comprobado que el aumento de los anticuerpos anti-HLA, medido por PRA (Panel Reactive Antibody), tiene una asociación importante con los episodios de rechazo agudo 8. También, González-Pinto, et al., reportaron que un resultado positivo de PRA se asocia con un rechazo en el 44 % de los casos, mientras que en el 79 % de casos PRA negativos estaban libres de rechazo 16.
Consideramos que, para poder comprobar nuestra hipótesis, se requieren estudios prospectivos multicéntricos para evaluar el seguimiento inmunológico con los anticuerpos anti-HLA mediante la tecnología Luminex™ en este tipo de trasplante. Por el momento, creemos que la detección de DSA es un marcador de rechazo agudo humoral que permite una aproximación diagnóstica y una intervención oportuna.
Referencias
1. Ueno T, Fukuzawa M. Current status of intestinal transplantation. Surg Today. 2010;40:1112-22. doi: 10.1007/s00595-010-4324-y
2. Clark CL. The immune response in small bowel transplantation. Ann R Coll Surg Engl. 1996;78:97-102.
3. Lauro A, Marino IR, Matsumoto CS. Advances in allograft monitoring after intestinal transplantation.
Curr Opin Organ Transplant. 2016;21:165-70. doi: 10.1097/MOT.0000000000000279
4. Tsai HL, Island ER, Chang JW, González-Pinto I, Tryphonopoulos P, Nishida S, et al. Association between donor-specific antibodies and acute rejection and resolution in small bowel and multivisceral transplantation. Transplantation. 2011;92:709-15. doi: 10.1097/ TP.0b013e318229f752
5. Juliao-Baños F, Guzmán C, Hoyos S, Mena Á, Echeverri C, Ruiz M, et al. Transplante de intestino delgado: “una realidad en Colombia.” Rev Colomb Gastroenterol. 2008;23:166-78.
6. Süsal C, Opelz G, Morath C. Role and value of Luminex ™-detected HLA antibodies before and after kidney transplantation. Transfus Med Hemotherapy. 2013;40:190-5. doi: 10.1159/000351314
7. Bond G, Reyes J, Mazariegos G, Wu T, Schaefer N, Demetris J, et al. The impact of positive T-cell lymphocytotoxic crossmatch on intestinal allograft rejection and survival. Transplant Proc. 2000;32:1197-8. doi: 10.1016/S0041-1345(00)01181-7
8. Berger M, Zeevi A, Farmer DG, Abu-Elmagd KM. Immunologic challenges in small bowel transplantation. Am J Transplant. 2012;12(Suppl.4):S2-8. doi: 10.1111/j.1600-6143.2012.04332.x
9. Abu-Elmagd KM, Wu G, Costa G, Lunz J, Martin L, Koritsky DA, et al. Preformed and de novo donor specific antibodies in visceral transplantation: Long-term outcome with special reference to the liver. Am J Transplant. 2012;12:3047-60. doi: 10.1111/j.1600-6143.2012.04237.x
10. Wu GS, Cruz RJ Jr, Cai J-C. Acute antibody-mediated rejection after intestinal transplantation. World J Transplant. 2016;6:719-28. doi: 10.5500/wjt.v6.i4.719 11. Everly MJ, Everly JJ, Arend LJ, Brailey P, Susskind B, Govil A, et al. Reducing de novo donor-specific antibody levels during acute rejection diminishes renal allograft loss. Am J Transplant. 2009;9:1063-71. doi: 10.1111/j.1600-6143.2009.02577.x
12. Gerlach UA, Lachmann N, Sawitzki B, Arsenic R, Neuhaus P, Schoenemann C, et al. Clinical relevance of the de novo production of anti-HLA antibodies following intestinal and multivisceral transplantation. Transpl Int. 2014;27:280-9. doi: 10.1111/tri.12250
13. Tait BD, Süsal C, Gebel HM, Nickerson PW, Zachary A, Claas FHJ, et al. Consensus guidelines on the testing and clinical management issues associated with HLA and non-HLA antibodies in transplantation. Transplantation. 2013;95:19-47. doi: 10.1097/TP.0b013e31827a19cc
14. Riethmüller S, Ferrari-Lacraz S, Müller MK, Raptis DA, Hadaya K, Rüsi B, et al. Donor-specific antibody levels and three generations of crossmatches to predict antibody-mediated rejection in kidney transplantation. Transplantation. 2010;90:160-7. doi: 10.1097/ TP.0b013e3181e36e08
15. Kubal C, Mangus R, Saxena R, Lobashevsky A, Higgins N, Fridell J, et al. Prospective monitoring of donor- specific anti-HLA antibodies after intestine/ multivisceral transplantation: Significance of de novo antibodies. Transplantation. 2015;99:e49-56. doi: 10.1097/TP.0000000000000614
16. Gonzalez-Pinto IM, Tzakis AG, Tsai H-L, Chang J-W, Tryphonopoulos P, Nishida S, et al. Association between panel reactive antibodies and acute small bowel rejection: analysis of a series of 324 intestinal transplants. Transplant Proc. 2010;42:4269-71. doi: 10.1016/j.transproceed.2010.09.078
