Presentación de Cuatro Casos y Revisión del Tema
JAIME M, MD*; CANO F, MD**; WOLFF G, MD***; RESTREPO J, MD****; SANTOS C, MD*****
Palabras clave: injerto libre de yeyuno revascularizado, reconstrucción microquirúrgica de la hipofaringe y esófago cervical, autotrasplante yeyuno.
Resumen
Se presenta la experiencia de los autores con el autotrasplante de yeyuno en cuatro pacientes con lesiones severas de la hipofaringe y el esófago cervical secundarios a lesiones por arma de fuego, arma cortopunzante, accidente de tránsito y lesión iatrogénica después de cirugía de tiroides por cáncer papilar.
Se hace un recuento histórico de la cirugía reconstructiva del esófago cervical, se presentan los aspectos anatómicos y fisiológicos del mecanismo de la deglución y la descripción de los principales detalles técnicos del procedimiento quirúrgico.
Todos los pacientes desarrollaron en el posoperatorio algún grado de disfagia que fue cediendo gradualmente. Un paciente alimentado durante cinco años por sonda de gastrostomía, presentó una neumonía grave por broncoaspiración en el día veinte posoperatorio, la cual cedió con tratamiento médico. Un paciente con fístula externa a nivel de la anastomosis superior en las primeras 72 horas, en el séptimo día luego de la operación había cerrado la fístula. En un paciente fue necesario repetir dos veces la anastomosis venosa por trombosis sucesiva de ésta.
Durante el acto operatorio se evaluó la permeabilidad de las anastomosis microvasculares y la viabilidad del asa mediante observación del color, secreción y peristaltismo durante un período de 30 minutos.
En dos pacientes se exteriorizó un segmento del asa trasplantada para vigilancia de la viabilidad del asa yeyunal, que posteriormente fue resecada. La vía oral se inició en todos los pacientes a los ocho días después de practicarse un esofagograma. A los cuatro pacientes se le dio de alta tolerando dieta licuada y con la sonda de gastrostomía cerrada.
Por su pedículo vascular y su diámetro, el yeyuno es el injerto ideal para remplazos de hasta 20 cm de esófago cervical, y aunque funciona como un conducto pasivo, presenta una adaptación adecuada a la deglución sino hay compromiso neuromuscular importante en la hipofaringe.
El ascenso gástrico sigue siendo el método de elección cuando se practica una esofaguectomía total. El uso del colon se reserva para los casos que por cirugía previa o por quemadura extensa no se puede utilizar el estómago.
El manejo de estos pacientes debe ser multidisciplinario y debe incluir un cirujano con experiencia en microcirugía vascular.
Introducción
Un problema de la cirugía reconstructiva en nuestro medio, es el manejo del paciente con estenosis severa de la hipofaringe y el esófago cervical que no responde a las dilataciones. Estas lesiones, aunque no muy frecuentes, se presentan como secuela de trauma severo del cuello debido a accidentes de tránsito, lesiones por armas de fuego y armas cortopunzantes, después de múltiples intervenciones reconstructivas fallidas, iatrogenias y quemaduras localizadas por ingestión de ácido o álcalis.
Estos enfermos están confinados a alimentación mediante gastrostomía, imposibilitados indefinidamente para alimentarse en forma natural y, por supuesto, con un gran desequilibrio emocional que repercute en su actividad laboral y en su calidad de vida.
Historia
Muchas técnicas han sido utilizadas para la reconstrucción del esófago cervical a través de los años. Desde 1894 Bircher1 describió el tubo de piel antetorácico para el tratamiento de las secuelas en quemadura por lejía, con una alta incidencia de fístulas y estenosis; Wookey2 en 1942 describió un método de reconstrucción esofágica cervical utilizando un colgajo local de piel que incluía el platisma; éste fue una modificación del tubo de piel de Bircher, con iguales limitaciones, incluyendo la obligatoria alteración de integridad de los tejidos adyacentes para tomar el colgajo.
En 1965 Bakamjian3 introdujo el colgajo deltopectoral para la reconstrucción de lesiones extensas de la cabeza y el cuello. Este método fue enorme importancia porque introdujo la técnica del colgajo vascularizado arterial que había propuesto Esser4 en 1924. Este colgajo axial, basado en la circulación dada por las perforantes mediales de la arteria mamaria interna, era transpuesto al cuello y luego tubolizado para el remplazo del esófago. Por este método se resolvieron los problemas dimensionales, principalmente la longitud, de tanta trascendencia en la reparación del defecto esofágico; sin embargo, con frecuencia se requerían múltiples reinter-venciones para remodelar el colgajo, con un porcentaje muy alto de complicaciones como las fístulas persistentes, la retracción del colgajo y la fibrosis.
Los colgajos musculocutáneos fueron desarrollados en los años setenta después del redescubrimiento y la observación anatómica de que los vasos perforantes musculocutáneos suplían en forma fiable la circulación de la piel5. Es así como se optó por transponer el músculo pectoral mayor al cuello con una isla suficiente de piel, con la irrigación de los vasos toracoacromiales. Esta técnica desplaza al colgajo delto-pectoral por su fiabilidad, y fue popularizada por Ariyan y col.6 y utilizada en pacientes con grandes resecciones por carcinomas de orofaringe. Otro colgajo fasciocutáneo utilizado en la reconstrucción de lesiones extensas del cuello es el colgajo radial de antebrazo irrigado por la rama septocutánea de la arteria radial descrita inicialmente por Yang en 1981, y utilizado más que todo en la reconstrucción de la cavidad oral debido a la finura y flexibilidad de la piel de esta área y al largo pedículo disponible.
El uso de las porciones pediculadas del tracto gastrointestinal para la reconstrucción del esófago cervical precedió con mucho tiempo a los colgajos musculocutáneos. En 1895, Biondi ideó remplazar el esófago con el estómago a través del hiato esofágico. En 1933 Oshawa7 fue el primero en practicar una anastomosis esofagogástrica. En 1911, Kelling8 usó el colon trasverso y Vulliet9 el colon izquierdo en una ruta subcutánea ascendente para remplazo del esófago.
En 1958 Seidenberg y col.10 en el hospital de Montefiore de Nueva York, realizaron un estudio experimental en perros utilizando la técnica de revascularización de un segmento de yeyuno colocado en el cuello, culminando su estudio con una cirugía en un paciente, el cual murió de un accidente cerebrovascular en el séptimo día posoperatorio y cuya autopsia evidenció que la anastomosis vascular del segmento yeyunal se encontraba viable.
Roberts y Douglas11 en 1961 reportaron el remplazo exitoso del esófago cervical por un autotrasplante de yeyuno libre revascularizado en dos pacientes. Desde entonces, múltiples reportes por Nakayama12, Jurkiewicz13 y Peters y col.14 entre otros, confirmaron la validez clínica de este procedimiento.
El desarrollo de la microcirugía llevó a que se estan-darizara la técnica del colgajo libre de yeyuno para la reconstrucción de la hipofaringe y del esófago cervical. Los colgajos musculocutáneos, atractivos inicialmente porque se evitaban la laparotomía y la toracotomía, requerían múltiples reintervenciones y prolongado tiempo de hospitalización. Hoy su uso ha desaparecido en la reconstrucción del esófago cervical. El ascenso gástrico sigue siendo el método de elección cuando se requiere una esofaguectomía total.
El uso del colon para reconstruir el esófago se reserva para los casos en que por cirugía previa o por quemaduras extensa, no se puede utilizar el estómago.
Anatomía y Fisiología
La hipofaringe yace inferior al plano horizontal del hueso hioides y en su límite superior a nivel del cartílago cricoides. Es un tubo muscular compuesto por cinco pares de músculo estriado, con una estrechez inferior terminal, donde se continúa con el esófago cervical a nivel de la sexta vértebra cervical.
Los músculos constrictores superior, medio e inferior ocupan la capa externa circular; estas hojas musculares corren a lo largo de la pared posterior de la faringe para insertarse en el rafé central. Las contracciones sucesivas de los músculos constrictores ayudan a propeler la comida hacia el esófago.
La musculatura longitudinal está compuesta por el estilofaríngeo y el palatofaríngeo, los cuales se insertan en el borde posterior del cartílago tiroides; ellos actúan elevando la laringe y la faringe durante la deglución. El músculo cricofaríngeo, y las fibras más inferiores del constrictor inferior originados desde el cartílago cricoides rodean la salida de la faringe, actuando como un esfínter fisiológico y permitiendo la entrada de aire al esófago en el momento de la deglución.
El nervio vago provee la inervación motora a todos los músculos de la faringe excepto al estilofaríngeo, el cual es inervado por el nervio glosofaríngeo. Estos nervios también dan las fibras sensoriales a la pared de la faringe, el paladar blando, los arcos faríngeos y al tercio posterior de la lengua. Esta inervación sensorial es importante para la iniciación de la fase faríngea de la deglución.
La deglución es un proceso complejo que requiere la coordinación de numerosos y rápidos eventos. Durante la fase oral, la lengua mueve la comida hacia atrás al arco anterior de las fauces, iniciando inmediatamente el reflejo de la deglución. Los impulsos de los nervios aferentes viajan al fascículo solitario del tallo cerebral y luego al centro de la deglución en la médula.
Las señales eferentes del reflejo de deglución se originan en el núcleo motor de los nervios craneanos V, VII, IX, XI y XII, y en el núcleo ambiguo del X, nervios que dan la inervación a la faringe. Toda esta estimulación motora es coordinada y se traduce en cuatro estados o momentos que son secuenciales en la fase faríngea de la deglución:
1. Cierre del paladar blando.
2. Constricción peristáltica de los músculos constrictores de la faringe.
3. Elevación y cierre de la laringe.
4. Relajación del músculo cricofaríngeo.
La fisiología de la deglución era escasamente entendida hasta el desarrollo de la manofluorometría. Esta es una técnica que combina en forma sistematizada la manometría y la fluoroscopia, permitiendo el análisis detallado de los cambios de presión, las variaciones anatómicas y el tiempo del tránsito del bolo durante la fase faríngea de la deglución. Tradicionalmente la deglución ha sido estudiada mediante fluoroscopia con contraste de bario para la deglución. La manometría faríngea ha sido un examen técnicamente dispendioso debido a que los cambios de presión en la faringe son muy rápidos, suceden en un segundo y la baja rata de respuesta de frecuencia de los trasductores manométricos impide la evaluación de estos cambios de presión tan veloces. La combinación de la manometría y la fluoroscopia permite la verificación de la localización de los trasductores la visualización del bolo y la correlación con los cambios de presión.
Estudios hechos por McConnel y asociados15, y por Moreno-Osset16 y asociados, han demostrado que es la acción de la lengua la fuerza principal impulsora a través de la faringe y que los músculos constrictores de la faringe juegan un papel secundario en la deglución, concepto funcional que revolucionó la cirugía de reconstrucción faringoesofágica.
En los estudios de McConnel y col. en pacientes con ascenso gástrico e injerto libre de yeyuno, se demostró que los segmentos reconstruidos funcionan como un conducto pasivo. La disfagia reportada era el resultado de descoordinación de los movimientos de la lengua presentándose una obstrucción de tipo funcional. Además, la resección de la pared de la orofaringe e hipofaringe interfiere con la inervación sensorial responsable de la activación del reflejo de la deglución. La disfunción de la propulsión de la lengua se traduce en una pérdida del control del bolo y pérdida de la fuerza de conducción. Entre más largo sea el segmento reconstruido mayor es la resistencia para el manejo de la fuerza por la lengua.
Originalmente se pensó que el peristaltismo del yeyuno facilitaría el paso de los alimentos. Sin embargo, el yeyuno no es un órgano de tránsito rápido y tiene un predominio de las ondas tipo I o peristalsis mezcladora; éstas ondas pueden impedir o demorar el tránsito del bolo de alimento y aunque el segmento yeyunal responde a estímulos químicos, no contribuye a un tránsito digestivo efectivo.
El éxito de la reconstrucción de la hipofaringe depende de la extensión del defecto resecado y del método que se utilice para reconstituir la continuidad del tracto gastrointestinal.
Técnica Quirúrgica
La técnica que a continuación se describe es la que hemos empleado para la reconstrucción de la hipofaringe y del esófago cervical y puede ser utilizado para reconstruir defectos hasta de 20 cm de longitud.
La clave del éxito radica en la preparación minuciosa del paciente, lo cual incluye la recuperación nutricional de aquellos con pérdida severa de peso. Antes de empezar la cirugía es necesario confirmar el buen funcionamiento del microscopio operatorio y la disponibilidad del material microqui-rúrgico adecuado.
El abordaje se hace simultáneamente por dos equipos quirúrgicos, uno a nivel del cuello y el otro a nivel abdominal (figura 1).
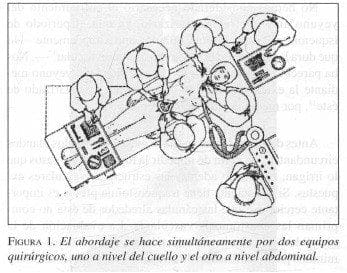
La disección de la hipofaringe y del esófago en el área estenosada se debe efectuar con sumo cuidado, puesto que la fibrosis predomina en el plano de la disección, teniendo especial cuidado en preservar la circulación venosa proximal que servirá de vaso receptor. En lo posible, la vena yugular externa, en su parte proximal debe ser disecada y respetada Mientras se completa la disección y se identifica el área que se debe resecar, el segundo equipo, del área abdominal, aborda la cavidad peritoneal por una incisión mediana, se visualiza el ligamento de Treitz y a 90 cm de éste se define el segmento de yeyuno para trasplante, teniendo en cuenta la longitud del defecto a corregir y respetando un margen amplio de 8 a 10 cm.
A continuación se procede a definir en el mesenterio, la arcada vascular radial del segmento seleccionado y, con una sutura, se marcan las márgenes proximal y distal del intestino para colocar posteriormente el segmento, en forma isoperistáltica; los vasos arterial y venoso de la arcada son escogidos, disecados y reparados, y el segmento de mesenterio que lo soporta es dividido usando ligadura de seda (figura 2).
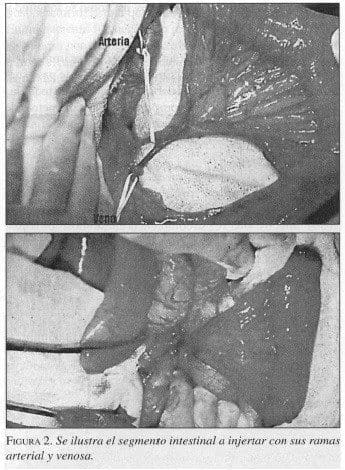
Este paso debe ser realizado con meticulosidad para evitar hematomas. Al finalizar esta etapa, el segmento de yeyuno sólo estará irrigado por el vaso arterial y venoso de la arcada; el segmento de intestino es seccionado entre dos clamps intestinales y es cubierto por una compresa húmeda, permitiendo la perfusión normal del segmento a trasplantar.
La continuidad del tracto gastrointestinal es restituida con una anastomosis intestinal con puntos interrumpidos de seda 3/0. En este momento en el área del cuello el segmento que va a ser resecado es calculado, y los vasos del cuello son identificados y preparados. El flujo arterial es comúnmente provisto por ramas de la carótida externa, la arteria cervical trasversa, la arteria tiroidea superior o la arteria lingual.
Es importante comparar y calcular el tamaño diametral de la arteria donante y receptora, así como la localización y el curso de los vasos. Cuando la luz de los vasos tiene una disparidad de 1.5: 1.0 es aconsejable realizar una anastomosis término lateral. Un puente vascular pocas veces es necesario, pero si hay duda en cuanto a la calidad de los vasos o la presencia de tensión, debe recurrirse a un injerto venoso. Si los vasos expuestos en el lado ipsilateral del cuello no son satisfactorios debido a extensa inflamación y fibrosis o a arteriosclerosis de los pequeños vasos, es necesario recurrir al lado contralateral. La arteria escogida es liberada y un segmento no calcificado es seleccionado para la anastomosis. Los vasos son pinzados y una vez estén ocluidos se remueven las pinzas microvasculares para verificar el flujo pulsátil arterial. A continuación se selecciona una vena en la misma región: vena yugular externa, facial o yugular interna, lo más alejada posible de la traqueostomía.
Es aconsejable marcar la cara anterior de la vena para asegurar que la anastomosis no quede rotada, y se deja completamente liberada y pinzada. En este momento se reasume el abordaje abdominal para comprobar la viabilidad del segmento intestinal seleccionado. Los vasos son seccionados y ligados en su parte distal. A continuación se trae el segmento yeyunal al cuello y se lo coloca en forma isoperistáltica; luego se evalúa la posición de los vasos, así como su longitud y diámetros.
El paso a seguir es la anastomosis proximal de la hipofaringe o del esófago proximal al yeyuno; este paso suele tener su grado de dificultad debido a la fibrosis de todas las estructuras vecinas y a la desproporción de los diámetros de la anastomosis, por lo cual es el sitio donde más fístulas posoperatorias suelen presentarse.
Si el diámetro de la boca receptora es muy amplio se puede abrir el yeyuno en forma longitudinal en su borde antimesentérico con el fin de asemejar los diámetros anastomóticos. Una vez se completa la anastomosis proximal se acerca el microscopio al campo operatorio y se practican las anastomosis vasculares venosa y arterial, iniciando con la venosa, con monofilamento 9/0 (figura 3).
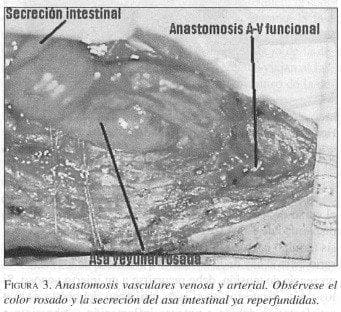
Si la arteria tiene placa ateromatosa, es importante incluirla en la sutura para evitar su desprendimiento. Los clamps son removidos, empezando primero por el venoso y luego el arterial. La perfusión debe aparecer inmediatamente: la pulsación de los vasos intestinales debe evidenciarse, así como el sangrado, el peristaltismo y la secreción de la mucosa.
En este momento la longitud del segmento intestinal es evaluada (lo usual es que sea largo y redundante), el segmento es recortado y se procede a realizar la anastomosis yeyunoesofágica distal con puntos separados de poliglactina 3/0. Antes de cerrar el abdomen, se sutura el defecto mesentérico preservando el catéter de gastrostomía previo.
No hemos considerado necesario el enfriamiento del yeyuno antes de revascularizarlo, ya que el período de isquemia es corto, sesenta minutos aproximadamente —lo que dura la práctica de la anastomosis microvascular17—. Nos ha parecido importante vigilar la viabilidad del yeyuno mediante la exteriorización de un segmento vascularizado de éste18, por medio de una incisión en la piel.
Antes de cerrar la piel se fija el meso a los tejidos blandos circundantes con el fin de impedir la torsión de los vasos que lo irrigan, cubriendo además las estructuras vasculares expuestas. Si el paciente tiene traqueostomía previa es importante cerciorarse que las cánulas alrededor de ésta no compriman las anastomosis vasculares. La evaluación de la viabilidad del colgajo se realiza durante los primeros treinta minutos por visualización directa de la anastomosis arterial y venosa, vigilando el color y el aspecto del asa testigo exteriorizada. En caso de signos de isquemia, se reexplorará y se revisarán las anastomosis vasculares. En todos los pacientes se inició alimentación por gastrostomía a las 72 horas de la operación y a los ocho días se practicó un esofagograma con bario, y si la integridad de la anastomosis era demostrada, se instauraba una dieta líquida y luego licuada.
* MARTINIANO JAIME CONTRERAS. Cirujano general, profesor Departamento de Cirugía, Universidad de Antioquia, Medellín, Colombia.
** FIDEL CANO RESTREPO. Cirujano general, cirujano vascular, profesor Departamento de Cirugía, Universidad de Antioquia, Medellín, Colombia.
*** GERMÁN WOLFF IDÁRRAGA. Cirujano plástico, profesor Departamento de Cirugía, Universidad de Antioquia, Medellín, Colombia.
**** JAIME RESTREPO ESPINAL. Cirujano plástico, profesor Departamento de Cirugía. Universidad de Antioquia, Medellín, Colombia.
***** CARLOS AUGUSTO SANTOS. Médico residente cirugía general, Universidad de Antioquia, Medellín, Colombia.
