Extensión de la Linfadenectomía para el Tratamiento Quirúrgico del Adenocarcinoma Gástrico en el Hospital Universitario San Ignacio: Cohorte Prospectiva con Análisis de Supervivencia
HENAO FJ, MD*; ROJAS OA, MD**; MEJÍA AF, MD**
Palabras clave: adenocarcinoma gástrico, gastrectomía, linfadenectomía, supervivencia.
Resumen
Introducción: en 1992 se creó el “Protocolo de Betania”, para el diagnóstico y tratamiento del cáncer gástrico en Colombia. A partir de ese momento, en el Hospital Universitario San Ignacio, el manejo de esta patología se ha realizado siguiendo los parámetros de dicho protocolo. El siguiente estudio presenta los resultados de una cohorte prospectiva que incluyó todos los pacientes operados por cáncer gástrico entre 1992 y 1998 en esta institución.
Materiales y métodos: cohorte prospectiva, observacional y descriptiva con análisis de supervivencia. Se incluyeron todos los pacientes con diagnóstico endoscópico e histológico de adenocarcinoma gástrico, operados en este hospital entre marzo de 1992 y diciembre de 1998. Se excluyeron del análisis los pacientes con tumores irresecables. Se analizaron entre otras las siguientes variables: demográficas, diagnóstico endoscópico e histológico, estadificación tumoral (TNM), tipo de cirugía, complicaciones posoperatorias y supervivencia.
Resultados: entre marzo de 1992 y diciembre de 1998 se realizaron 137 procedimientos quirúrgicos con diagnóstico de cáncer gástrico. 86 operaciones fueron consideradas con intención curativa, 18 fueron paliativas y las 33 restantes laparotomías no terapéuticas. Estos últimos 33 pacientes fueron excluidos del estudio. La supervivencia global actuarial fue de 54% a 5 años. Las principales variables que determinaron la supervivencia fueron el número de ganglios comprometidos y el estado tumoral. El nivel de disección ganglionar no tuvo impacto en la supervivencia y aumentó significativamente la morbilidad. El tratamiento adyuvante con quimioterapia tampoco afectó la supervivencia.
Conclusiones: los resultados del tratamiento quirúrgico del cáncer gástrico dependen del diagnóstico temprano de la enfermedad, del compromiso ganglionar y no de la extensión de la linfadenectomía.
Introducción
Al cáncer gástrico se le atribuyen más de medio millón de muertes por año en el mundo, cifra superada solamente por el carcinoma pulmonar1. Las tasas de más alta incidencia corresponden a Costa Rica, Japón, China y Colombia, entre otros2. En muchos países occidentales, la incidencia del cáncer gástrico ha descendido un las dos últimas décadas. La mayoría de los pacientes tiene más de 60 años en el momento del diagnóstico y se presenta con estados avanzados de la enfermedad, pues los estadios tempranos son generalmente indolentes. Estas dos características contribuyen a su mal pronóstico. En general la supervivencia a cinco años varía entre 10% y 25% en los países occidentales3. Durante las últimas dos décadas se ha presentado un aumento en la incidencia del cáncer gástrico de ubicación proximal (fondo y cardias), mientras que la incidencia del mismo en ubicación distal ha disminuido4. Varios estudios han mostrado que la colonización por Helicobacter pylori se relaciona con adenocarcinoma del tercio distal del estómago y no con el del tercio proximal5. En Estados Unidos 71% de los pacientes consultan en estadios tardíos de la enfermedad. En Japón, en cambio, el diagnóstico se hace en estadios tempranos hasta en 50% de los casos, gracias a los programas de tamizaje. Por otra parte, es importante resaltar que existen diferencias entre los criterios diagnósticos histológicos para adenocarcinoma del tipo intestinal entre patólogos japoneses y occidentales, lo cual en parte puede explicar la alta proporción de adenocarcinoma gástrico temprano en Japón y el mejor pronóstico del cáncer gástrico en este país al compararlo con el mundo occidental6.
Colombia presenta una de las mayores incidencias de cáncer gástrico en el mundo. El cáncer gástrico es la principal causa de muerte por neoplasia en hombres mayores de 40 años en este país7. La enfermedad se distribuye en nuestro país especialmente en dos áreas: la zona sur (incluye Nariño, Cauca y Valle del Cauca) y la zona del altiplano Cundiboyacense8. En nuestro país se han realizado varios trabajos sobre carcinoma gástrico y todos ellos demuestran que el diagnóstico se hace en estadios tardíos con pocas probabilidades de realizar procedimientos curativos y con muy pocos diagnósticos de estadios tempranos. Las tasas de supervivencia a 5 años son muy bajas9,10-13.
La cirugía es la única modalidad de tratamiento potencialmente curativo en la actualidad. La quimioterapia y la radioterapia no han tenido impacto en la supervivencia de los pacientes con cáncer gástrico. Existe controversia en cuanto al tipo de linfadenectomía que debe acompañar a la gastrectomía en el manejo quirúrgico del cáncer gástrico. En países orientales la linfadenectomía D2 ha mostrado resultados satisfactorios en la supervivencia de los pacientes al compararla con la linfadenectomía D1, pero la mayoría de trabajos son retrospectivos14, 15, 16, 17, 18. En Occidente, varios trabajos han mostrado que la linfadenectomía D2 no tiene impacto en la supervivencia de los pacientes y que sí aumenta la morbilidad19, 20-22.
Materiales y Métodos
Se incluyeron en el estudio los pacientes con diagnóstico endoscópico e histológico de adenocarcinoma gástrico que recibieran tratamiento quirúrgico en el Hospital Universitario San Ignacio entre marzo de 1992 y diciembre de 1998 siguiendo las recomendaciones establecidas en la reunión de consenso en el seminario taller de diagnóstico y manejo del cáncer gástrico en Betania, Huila, en 19927.
El “Protocolo de Betania” recomendaba básicamente realizar gastrectomías con linfadenectomías hasta la segunda estación ganglionar cuando el tumor se consideraba temprano, y realizar linfadenectomías hasta la tercera estación ganglionar cuando el tumor se consideraba avanzado.
El estudio es una cohorte prospectiva, observacional y descriptiva con análisis de supervivencia.
Resultados
Entre marzo de 1992 y diciembre de 1998 se realizaron 137 procedimientos quirúrgicos con diagnóstico de cáncer gástrico.
De estos 137 procedimientos, 86 fueron considerados con intención curativa, 18 fueron paliativos y los 33 restantes fueron laparotomías no terapéuticas. Los 33 casos de laparotomías no terapéuticas fueron excluidos del estudio (figura 1).
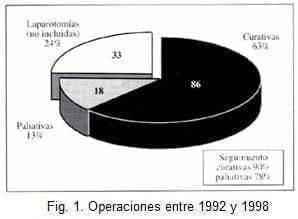
De las 86 operaciones con intención curativa realizadas, 78 (90%) tienen seguimiento hasta la actualidad. De las 18 operaciones paliativas, 14 (78%) tienen seguimiento hasta la muerte del paciente.
Los pacientes fueron distribuidos por rangos de edad en la siguiente forma: entre 21 y 40 años, entre 41 y 60 años, entre 61 y 80 años y mayores de 80 años. La mayoría de los pacientes se encontraba en el grupo de los 41 a los 60 años (45 pacientes, 43%), y en el de los 61 a los 80 años (46 pacientes, 44%).
En cuanto a la distribución por sexo, de los 104 pacientes incluidos en el estudio, 65,4% eran hombres (68 pacientes) y 34,6% eran mujeres (36 pacientes).
La localización endoscópica de las lesiones se muestra en el figura 2. La mayoría de las lesiones, 52,4% (54 pacientes) estaba ubicada en el antro. El resto de las lesiones tuvo localización media, 24,3% (25 pacientes); en la curvatura menor, 11,7% (12 pacientes); a nivel cardial, 7,8% (8 pacientes); y en la curvatura mayor, 3,8% (4 pacientes ); en uno de los 104 pacientes no apareció especificada la localización del tumor.

El diagnóstico histológico preoperatorio se dividió en los tipos intestinal, difuso, mixto y temprano y tuvo la siguiente distribución: intestinal bien diferenciado en 9 pacientes (8,7%), intestinal moderadamente diferenciado en 29 pacientes (27,9%), intestinal mal diferenciado en 26 pacientes (25%), difuso en 27 pacientes (26%), mixto en 4 pacientes (3,8%), y temprano en 9 pacientes (8,7%).
Los procedimientos quirúrgicos realizados fueron: gastrectomía subtotal en 71 pacientes (68,3%), gastrectomía total en 23 pacientes y en 10 pacientes (9,6%) no se hizo resección (figura 3).

Los procedimientos tuvieron los siguientes niveles de resección según las barreras ganglionares removidas: R0 en 13 pacientes (12,5%), R1 en 2 pacientes (1,9%), R2 en 74 pacientes (71,2%) y R3 en 15 pacientes (14,4%).
El número de ganglios resecados tuvo un promedio de 21,2 por operación, con un rango entre 3 y 74.
Las reconstrucciones realizadas fueron en su mayoría de tipo Billroth II (56 pacientes, 57,1%), seguida de esofagoyeyunostomía (20 pacientes, 20,4%), Y de Roux (11 pacientes, 11,2%) y gastroyeyunostomía (11 pacientes, 11,2%). Es de anotar que todas las esofagoyeyunostomías se reconstruyeron con una Y de Roux; no había datos en 6 pacientes.
En cuanto a invasión de la pared del estómago, en el análisis anatomopatológico se pudo establecer que el tumor llegaba hasta la serosa en más de la mitad de los casos (52 pacientes, 53,6%). Se encontró compromiso hasta la muscular en 20 pacientes (20,6%). Se encontraron 17 cánceres tempranos (17,5%) distribuidos en 11 pacientes con compromiso de mucosa y los otros 6 con compromiso de la submucosa. Se encontraron 6 pacientes (6,2%) con compromiso de órganos vecinos y 2 pacientes con compromiso de la subserosa.
No se encontró compromiso de los bordes de resección en 78 pacientes (77,2%); se encontró compromiso de los bordes en 13 pacientes (12,9%); no se hizo resección en 10 pacientes (9,6%) y no había dato en 3 pacientes.
La mayoría de pacientes se encontraba con estados avanzados de la enfermedad en el momento de la cirugía (26 pacientes en estado IIIA, 20 pacientes en estado IIIB y 15 pacientes en estado IV, para un 58,6%); 19 pacientes se encontraron en estado II (18,3%), 15 pacientes en estado IA (14,4%) y 9 pacientes en estado IB (8,7%).
El compromiso ganglionar encontrado en la revisión histopatológica de la pieza quirúrgica mostró la siguiente división por grupos: de 0 a 5 ganglios comprometidos en 62 pacientes (72,1%); de 6 a 10 ganglios comprometidos en 15 pacientes (17,4%); y más de 10 ganglios comprometidos en 9 pacientes (10,5%).
Se utilizó quimioterapia posoperatoria en 46 pacientes (49,5%).
La tasa de complicaciones posoperatorias fue de 27,2% (28 pacientes); a 12 (42,8%) pacientes de este grupo se les realizó gastrectomía total y a los 16 restantes (57,14%) gastrectomía subtotal. De estos 28 pacientes, 14 pacientes (50%) desarrollaron complicaciones infecciosas pulmonares, pero sólo 3 de ellas fueron mayores y requirieron intubación orotraqueal y manejo en cuidado intensivo; a estos 3 pacientes se les había realizado gastrectomía total.
La tasa de complicaciones cardiovasculares fue 5,7% (6 pacientes) del total de la serie (104 pacientes) y constituyó el 21% del total de las complicaciones posoperatorias. Tres pacientes sufrieron infarto agudo del miocardio, y sólo uno de ellos falleció. Los tres pacientes con complicaciones coronarias eran mayores de 70 años.
Se presentaron 5 casos de complicaciones mayores asociados a fallas de las diferentes anastomosis. Cuatro ocurrieron en pacientes sometidos a gastrectomía total que desarrollaron dehiscencia de la esofagoyeyunostomía; de éstos, dos fallecieron. En todos estos casos se utilizó sutura mecánica. Hubo un caso aislado de dehiscencia del muñón duodenal en una gastrectomía subtotal. Las otras complicaciones posoperatorias fueron infección de vías urinarias, hemorragia de vías digestivas altas sin compromiso hemodinámico, un evento cerebrovascular de tipo isquémico y neumonías aisladas sin alteración de la función respiratoria.
La tasa de complicaciones intraoperatorias fue 2,9% (3 pacientes); todos correspondieron a desgarro de la cápsula esplénica y requirieron esplenectomía. De estos tres pacientes, dos fueron sometidos a gastrectomía subtotal y 1 a gastrectomía total.
La mortalidad operatoria fue de 5 pacientes (4,8%), entre los cuales sólo hubo un caso de mortalidad intraoperatoria durante una reintervención.
Análisis de Supervivencia
Se realizó el análisis de supervivencia de 92 pacientes, incluyendo 78 gastrectomías con intención curativa y 14 procedimientos de tipo paliativo. Para tal propósito se empleó el programa estadístico “STATA”, y sólo los pacientes con seguimiento completo fueron incluidos en el análisis.
Es así como, independiente del tipo de cirugía, la tasa de supervivencia global a cinco años fue 54% (intervalo de confianza, IC, 42-65) (figura 4).

A continuación se presenta el análisis de las 78 operaciones realizadas con intención curativa y con seguimiento.
Al realizar el análisis de los pacientes por grupo de edad, se encontró una supervivencia del 66% a 5 años (IC 45-81) para los pacientes entre los 41 y los 60 años. Los pacientes entre los 61 y los 80 años tuvieron una supervivencia de 55% (IC 34-71). Esta diferencia fue estadísticamente significativa (P=0,0445) (figura 5).

Los pacientes sometidos a cirugía de tipo curativo tuvieron una supervivencia de 63% a cinco años (IC 49-74), en comparación con los pacientes que recibieron operaciones de tipo paliativo, cuya supervivencia media posoperatoria fue de 11 meses y ninguno vivió 5 años (figura 6).

La presencia de 6 o más metástasis ganglionares demostró ser una variable determinante de supervivencia, con una diferencia estadísticamente significativa al comparar los diferentes grupos. Los pacientes con 6 o más ganglios positivos tuvieron una supervivencia a cinco años de 16% (IC 3-38), mientras que los pacientes con 1 a 5 ganglios comprometidos sobrevivieron en un 73% (IC 49-87). Los pacientes sin compromiso ganglionar tuvieron una supervivencia a cinco años de 85% (IC 58-95) (figura 7).

El número de ganglios resecados, que varió entre 3 y 74 con un promedio de 21, no mostró correlación con el tiempo de supervivencia.
La clasificación por estadios TNM30 mostró cómo aquellos pacientes con estadios tempranos IA, IB y II tuvieron una mejor supervivencia que los casos de estadios más avanzados, IIIA y IIIB. La mortalidad a 5 años de este primer grupo fue 8%, mientras que en los pacientes con lesiones más avanzadas la mortalidad fue 77%. (p=0,0001) (figura 8). Las tasas de supervivencia a 5 años se distribuyeron así: estadio IA 92% (IC 54-99), IB 88% (IC 39-98), IIIA 43% (IC 18-67) y IIIB 28% (IC 9-50).

No se encontraron diferencias estadísticamente significativas en cuanto a supervivencia al comparar el nivel de resección ganglionar R2 o R3 (P=0,64). Los pacientes con resecciones de tipo R3 tuvieron una supervivencia a 5 años de 59% (IC 27-81), y los pacientes con resección ganglionar R2 tuvieron una tasa de supervivencia a cinco años de 64% (IC 48-76) (figura 9).

Se encontró que los pacientes con resecciones de tipo R3 tuvieron un mayor índice de complicaciones posoperatorias (61,5%), en comparación con las operaciones de tipo R2 (22,5%). Esta diferencia fue estadísticamente significativa (P=0,00503). El riesgo de presentar complicaciones posoperatorias es 2,7 veces mayor al someter un paciente a una resección ganglionar de tipo R3.
Finalmente, no se encontraron diferencias significativas en cuanto a supervivencia entre los pacientes con y sin quimioterapia.
Discusión
En la actualidad existe gran controversia en cuanto al tipo de linfadenectomía que debe acompañar a la gastrectomía en el manejo quirúrgico del adenocarcinoma gástrico. Varios estudios realizados en países occidentales19-22 muestran que la linfadenectomía extendida D2 no mejora la supervivencia de los pacientes y conlleva más complicaciones al compararla con la linfadenectomía D1. En países orientales los estudios han demostrado mejores resultados en aquellos pacientes sometidos a gastrectomía con linfadenectomía D2 que en pacientes con linfadenectomía D1; el estudio alemán de Siewert18 también demostró ventajas en la supervivencia de subgrupos de pacientes sometidos a linfadenectomía D2, al compararla con D1.
Tal vez el estudio más estructurado desde el punto de vista epidemiológico que se ha realizado hasta el momento es el del grupo holandés de van de Velde23. La principal conclusión de este estudio después de seguimiento de 5 años fue que la linfadenectomía D2 no mejoraba la supervivencia y sí aumentaba la morbilidad al compararla con la D1, por lo cual no recomiendan la linfadenectomía D2 como rutina. Sin embargo, en el último congreso nacional de cirugía que se realizó en Cartagena, el mismo autor mostró una actualización en cuanto a los resultados de su trabajo después de 7 años de seguimiento, donde el grupo de pacientes con N2 comprometido por tumor se beneficiaban de la linfadenectomía D2 con una mejor supervivencia que los pacientes sometidos a linfadenectomía D1. En la actualidad es imposible predecir preoperatoriamente el compromiso de los niveles ganglionares, por lo cual estaría indicado en todos los casos practicar linfadenectomía D2 en todas las gastrectomías en el manejo quirúrgico del adenocarcinoma gástrico.
En nuestro país, en un intento por mejorar la estrategia para enfrentar el flagelo del cáncer gástrico, en 1992 se creó el “Protocolo de Betania”. Los términos que se utilizaban en aquel entonces eran resección tipo R2 y R3 al hablar del tipo de linfadenectomía asociada a la gastrectomía.
La tasa de supervivencia global a cinco años en nuestro estudio fue 54%; es importante anotar que se habla de supervivencia actuarial en este caso y que la mayoría de los pacientes incluidos en el estudio fueron sometidos a cirugía con intención curativa y sólo 14 de ellos fueron sometidos a procedimientos paliativos. La supervivencia según grupos de edad fue mejor para los pacientes incluidos en el grupo entre los 41 y los 60 años, al compararlo con el grupo entre los 61 y los 80 años, más probablemente por enfermedades asociadas que contribuyeron a aumentar la morbimortalidad en el segundo grupo. Los pacientes sometidos a cirugía con intención curativa tuvieron una supervivencia (actuarial) a cinco años de 63%.
El compromiso ganglionar demostró ser la variable con mayor impacto en la supervivencia de los pacientes. Los pacientes con 6 o más ganglios comprometidos por tumor tuvieron una supervivencia a cinco años de 16%, mientras que los pacientes con 5 o menos ganglios comprometidos tuvieron una supervivencia de 73% y los pacientes sin compromiso ganglionar tuvieron una supervivencia de 85%. Al igual que en la mayoría de estudios prospectivos realizados hasta la actualidad, el factor que más impacto tiene en la supervivencia de los pacientes es el compromiso ganglionar. En el presente estudio los pacientes sometidos a disección tipo R3 no tuvieron diferencias en la supervivencia, pero sí tuvieron un mayor índice de complicaciones posoperatorias al compararlos con los pacientes sometidos a resección tipo R2. El uso de quimioterapia no tuvo impacto en la supervivencia.
Conclusiones
El presente estudio nos permite concluir que en nuestro hospital todavía tenemos un bajo índice de pacientes que se presentan con cáncer gástrico temprano (17,5%) y que la distribución por edad y sexo continúa siendo un poco mayor en hombres entre los cuarenta y los sesenta años.
A pesar de lo que aparece en otros informes de la literatura4,5, la localización cardial del cáncer gástrico todavía es infrecuente (7,8%) en nuestro hospital, y continúa siendo más frecuente la localización antral (52,4%).
Los pacientes sometidos a cirugía paliativa tienen una peor supervivencia que aquellos a los que se les practicó cirugía con criterio curativo.
Los pacientes que presentan cinco o menos ganglios comprometidos por tumor tienen una supervivencia mayor que aquellos que tienen más de seis.
Cuando el paciente tiene un estado clínico del tumor menor o igual a II según la clasificación TNM26, tiene una mayor posibilidad de supervivencia.
El nivel de resección R3 no mejoró la supervivencia y sí produjo mayor número de complicaciones (riesgo 2,7 veces mayor). El tratamiento con quimioterapia no mostró cambios en la supervivencia de nuestros pacientes.
Abstract
Several Colombian groups interested in the management of gastric cancer met in Betania, Huila, in 1992, with the purpose of developing guidelines (known nationally as the “Protocolo de Betania”) for the management of gastric cancer. Following the publication of the guidelines, a prospective study was initiated at Hospital Universitario San Ignacio in Bogotá. The present study includes all patients with the diagnosis of gastric cancer previously documented that underwent surgical treatment based on such guidelines at our hospital between March 1992 and December 1998. The study is a prospective cohort with survival rates; patients with unresectable tumors were excluded from the study.
Between March 1992 and December 1998, 137 surgical procedures were performed on subjects with diagnosis of gastric carcinoma; 86 of the patients had curative procedures and 18 palliative procedures; the remaining 33 patients had unresectable tumors and were excluded from the study.
The level of lymphadenectomy had no impact on the five-year survival of these patients, and the more radical dissections were associated with higher number of complications. The number of lymph nodes affected by tumor was the most significant prognostic factor.
Referencias
1. Inambar N.: Gastric Cancer. Surg Oncol Clin North Am 1993; 2(3): 333-345.
2. Correa P.: Etiopatogenia del Cáncer gástrico. Tribuna médica, 89 (6)1994; 261-262.
3. Van de Velde C.: Gastric Cancer Staging and Surgical Treatment of Gastric Cancer. 1992; 7-103.
4. Brenes F, Correa P.: Pathology of gastric cancer. Surg Oncol Clin North Am 1993; 2(3): 347-360.
5. Siewert J, Fink U, Sendler A et al.: Gastric Cancer, Curr Probl Surg 1997; 34(11): 837-852.
6. Schlemper R, Itabashi M, Kato Y, et al.: Differences in diagnostic criteria for gastric carcinoma between Japanese and Western Pathologists. Lancet 1997; 349: 1725-29.
7. Liévano G.: Diagnóstico y manejo del cáncer gástrico, Editora Láser Impresores, Neiva, Colombia, 1992.
8. Henao F, Jiménez H.: Cáncer gástrico. Manual de cirugía Pontificia Universidad Javeriana, Editorial CEJA, Bogotá, 1999; págs. 289-293.
9. Segura J, Gaitán M, Lozano L, Montañez P.: Cáncer gástrico: estudio sobre 205 casos en el Instituto Nacional de Cancerología, Temas escogidos de gastroenterología, t. VI. Bogotá, 1962; págs. 41-62.
10. Higuera D, Escobar J, Argüello M.: Carcinoma gástrico. Temas escogidos de gastroenterología, t. XIX, Bogotá, 1976, págs. 69-78.
11. Liévano G, Peñaloza F, Argüello M, Camargo H.: Cáncer en estómago operado por lesión benigna. Temas escogidos de gastroenterología, t. XX, Bogotá, 1978, págs. 85-97.
12. Segura J, Olarte H, Martínez A. Tratamiento quirúrgico radical y paliativo del cáncer gástrico 1961-1970. Instituto Nacional de Cancerología. Temas escogidos de gastroenterología, t. XXI. Bogotá, 1980, págs 49-67.
13. Pineda R. Cáncer gástrico en el Hospital San Rafael de Tunja. Temas escogidos de gastroenterología, t. XXVI, Bogotá, 1991, págs. 19-40.
14. Maehara Y, Orita H, Okuyama T, et al.: Predictors of lymph node metastasis in early gastric cancer. Brit J Surg 1992; 79 (March): 245-247.
15. Maruyama K, Sasako M, Kinoshita T, et al.: Pancreas-preserving total gastrectomy for proximal gastric cancer. World J Surg 1995; 10: 532-536.
16. Okayima K, Isozaki H.: Splenectomy for the treatment of gastric cancer: Japanese experience. World J Surg 1995; 19: 537-540.
17. Siewert J, Maruyama K. What’s new on gastric cancer. World J Surg 1995; 19: 483.
18. Siewert J, Bottcher K, Roder J, et al.: Prognostic relevance of systematic lymph node dissection in gastric carcinoma. Br J Surg 1993; 80: 1015-1018.
19. Roder J, Bonenkamp J, Craven J. Lymphadenectomy for gastric cancer in clinical trials: Update. World J Surg 1995; 19: 546-553.
20. Dent DM, Madden MV.: Randomized comparison of R1 and R2 gastrectomy for gastric cancer. Brit J Surg 1988; 75: 110,1988.
21. Robertson CS, Chung SCS, Woods SDS.: A prospective randomized trial comparing R1 subtotal gastrectomy with R3 total gastrectomy for antral cancer. Ann Surg 1994; 220: 176,1994.
22. Pacelli F, Doglietto G, Bellantone R.: Extensive versus limited lymph node dissection for gastric cancer: A comparative study of 320 patients. Brit J Surg 1993; 80: 1153-1156.
23. Bonenkamp JJ, van de Velde CJH, Sasako M.: Extended lymph node dissection for gastric cancer. N Engl J Med 1999; 340: 908-914.
