Estudios Analíticos
l. BAENE, MD, SCC
Palabras clave: Resistencia bacteriana, Enfermedades infecciosas, Bacterias patógenas, Moléculas antibacterianas, Antibióticos.
Introducción
Uno de los problemas de morbilidad y mortalidad en los centros hospitalarios es la resistencia bacteriana. Esta se presenta cuando el médico requiere combatir las enfermedades infecciosas producidas por bacterias y ellas no responden al tratamiento de antibióticos. A principios de los años 40 surgió el uso de la penicilina para combatir estas enfermedades; al poco tiempo de emplear esta droga empezaron a surgir bacterias resistentes con lo cual no fue posible combatirlas. Con el pasar del tiempo, las compañías farmacéuticas han desarrollado un gran número de moléculas antibacterianas para inhibir el crecimiento de los agentes causantes de las enfermedades infecciosas; estos medicamentos han requerido de grandes inversiones económicas y largos períodos de investigación. Desafortunadamente para la humanidad, pero no así para las bacterias, éstas han logrado generar diferentes alternativas para evadir el efecto letal de los antibióticos convirtiéndose en cepas resistentes. Para entender la habilidad de las bacterias patógenas para defenderse de los antimicrobianos es necesario conocer el desarrollo evolutivo de la vida en el planeta; ellas aparecieron hace 3.5 billones de años, los mamíferos hace 250 millones, nuestros humanoides hace 2.5 millones, el Horno Sapiens hace 125.000 años y los antibióticos solo fueron desarrollados para el uso del hombre hace 54 años. He aquí el porqué todavía estamos como en las cavernas con relación al dominio de las mismas (1,23).
Definición de Resistencia Bacteriana
Se puede definir la resistencia bacteriana como la disminución de la sensibilidad de un germen a la acción nociva de un agente quimioterápico determinado. En un principio se creía que la resistencia se debía a una modificación en la bacteria, posterior al contacto con un determinado antibiótico, algo así como en la reacción alérgica en que los síntomas se presentan recién cuando el sujeto sufre una segunda exposición al alergeno. Hoy se sabe que hay muchos mecanismos en juego, pero el más importante, es la modificación de la información genética de las bacterias. Esto puede llevar a que algunas pierdan la pared celular y se transformen en resistentes a antibióticos que destruyen la pared; otras, modifican su metabolismo o su síntesis proteica al alterar sus sistemas enzimáticos, lo que anula la acción del antibiótico; o producen enzimas que alteran la molécula antibiótica como es el caso de las betalactamasas en el Staphylococcus áureas (2).
Clasificación de la Resistencia Bacteriana
La resistencia bacteriana puede clasificarse de varias formas:
1. Por su origen, puede ser natural, adquirida o trasmitida.
Natural, también llamada primaria, cuando se presenta en los casos en que no hubo contacto previo con el antibiótico en uso. Adquirida o secundaria. Cuando hay antecedentes de utilización del mismo antibiótico en un individuo en tratamiento. Trasmitida, cuando se produce por transferencia de un germen a otro, no necesariamente similares, de factores extracromosómicos. Es lo que se conoce como resistencia mediada por plásmidos, segmentos de DNA que migran de una bacteria a otra, confiriendo resistencia al microorganismo que hasta ese momento era sensible al antibiótico en estudio. Esta transferencia también la pueden dar los virus e igualmente se puede dar el material genético producido por muerte bacteriana. Cuando la información genética de resistencia bacteriana es embebida en pequeñas cantidades de DNA, ya sea en cromosomas o en plásmidos. Se les da el nombre de trasposomas. y cuando la información es tomada por toda una bacteria se le denomina integrón.
2. Otra forma puede ser directa o cruzada, según el antibiótico objeto de resistencia, y estaría dentro de la resistencia adquirida. Si en el segundo contacto el antibiótico es el mismo, es directa; pero si éste es otro diferente, es cruzada o indirecta, pues para que este segundo tipo pueda producirse, ambos deben estar químicamente emparentados; por ejemplo, la primera vez penicilina y el segundo contacto cefalosporina.
3. Según la rapidez conque el microorganismo se hace resistente, la forma puede ser lenta o muy rápida. En el caso del estafilococo y las micobacterias el proceso es lento, mientras que es muy rápido con cepas de E. coli (1,3).
Mecanismos Generales de Resistencia
Tres son los mecanismos básicos mediante los cuales las bacterias se hacen resistentes a los antibióticos: por inactivación del antibiótico; por alteración del sitio blanco del antibiótico; o por disminución del transporte del antibiótico al interior de la célula.
Inactivación del antibiótico
El antibiótico puede inactivarse por hidrólisis o por modificación enzimática.
La hidrólisis enzimática, compromete a los antibióticos betalactámicos y a la eritromicina.
Antibióticos betalactámicos. Fueron los primeros antibióticos que se intrudujeron para el tratamiento de infecciones comunes y para los cuales se conoce con gran precisión el mecanismo de la resistencia. Así mismo, son los de mayor empleo y los más conocidos. Actúan inhibiendo las enzimas D-alanil-Dalanincarboxipeptidasas, también conocidas como PBPs( proteínas que se unen a penicilina), responsables de la síntesis de la pared celular, provocando filamentación y lisis celular.
Los betalactámicos, representados por las penicilinas y cefalosporinas, son antibióticos efectivos contra bacterias Gram positivas y Gram negativas, aeróbicas ‘f anaeróbias, algunos de ellos. Las enzimas responsables de proporcionar resistencia contra estos antibióticos son las betalactamasas que hidrolizan el enlace amida del anillo penicilánico o cefalosporánico produciendo derivados ácidos sin propiedades antibacterianas. Pueden ser de dos clases, penicilinasas y cefalosporinasas, según que actúen sobre penicilinas o sobre cefalosporinas. También pueden diferenciarse por su localización en las células, propiedades fisicoquímicas o su codificación genética (plásmidos o cromosómicas). Las betalactamasas Gram positivas son mediadas por plásmidos y están en la superficie celular; las betalactamasas Gram negativas son codificadas unas cromosómicamente, otras por plásmidos y otras trasmitidas por conjugación. La enzima TEM-I es la betalactamasa Gram negativa más común.
Eritromicina. Este antibiótico, del grupo de los macrólidos, inhibe la síntesis de proteínas bacterianas, uniéndose reversiblemente a la subunidad ribosomal50S, bloqueando la translocación e impidiendo la extensión de la cadena polipeptídica. El mecanismo común de resistencia es la producción de eritromicina esterasa que catalisa la hidrólisis del anillo lactona del antibiótico. Para las eritromicinas esterasas han sido estudiados dos genes con relativa profundidad, ereA y ereB, obtenidos de aislamientos clinicos de E. coli y parece que son resultado de una evolución convergente.
La modificación enzimática de antibióticos, compromete a los aminoglucósidos y al cloramfenico1.
Aminoglucósidos. Ejercen su acción interfiriendo en la síntesis de proteínas bacterianas, por unión al ribosoma 30S. Entre este grupo se encuentran la estreptomicina, gentamicina, tobramicina, netilmicina, neomicina, amikacina ampliamente usados contra gérmenes Gram negativos. Las bacterias inactivan estos antibióticos sintetizando enzimas modificadoras codificadas en plásmidos. Predominan dos tipos de modificación: nacetilación de grupos amino y o-fosforilación de grupos hidroxilo.Entre las principales enzimas responsables de catalizar la modificación, están la acetiltransferasa (AAC), fosfatidiltransferasa (APH) y adeniltransferasa (AAD). Existen asimismo otros mecanismos de resistencia a aminoglucósidos, como el bloqueo del transporte del antibiótico al sitio de acción y la modificación de ribosomas.
Cloramfenicol. Este antibiótico penetra a la célula por difusión facilitada y se une a la subunidad 50S del ribosoma, causando inhibición de la síntesis de proteínas. La resistencia al cloramfenicol se debe a la presencia de una enzima intracelular, cloramfenicolacetiltransferasa (CAT) existente tanto en Gram positivos como en Gram negativos. Esta enzima acetila los dos grupos hidroxilo y previene la unión del c1oramfenicol al ribosoma 50S (3-6).
Alteración del blanco de acción del antibiótico
Pared celular. Los antibióticos betalactámicos actúan sobre las proteínas de la pared celular PBPs (unidoras de penicilina). Las mutaciones en estas proteínas, tanto en bacterias Gram positivas como en Gram negativas, disminuyen la afinidad por los antibióticos betalactámicos, permitiendo la formación de la pared celular. Estos microorganismos son refractarios a cualquier tipo de derivado betalactámico.
Ribosomas. La resistencia a antibióticos que se presenta debido a la alteración de ribosomas, puede involucrar componentes de las subunidades 50S que incluye fundamentalmente a macrólidos y lincomicinas 30S que involucra ami noglucósidos o al RNA ribosoma123S ó 16S que tienen que ver con la estreptomicina.
Proteínas relacionadas con síntesis y funcionamiento de ácidos nucleicos
DNA girasa. Las quinolonas son fármacos antimicrobianos derivados del ácido nalidíxico, con una alta actividad contra gérmenes Gram negativos. La introducción de un átomo de flúor a la molécula de quinolona produjo un grupo de antibióticos como la ofloxacina, pefloxacina, enoxacina, norfloxacina y ciprofloxacina.
La DNA giras a es una enzima topoisomerasa tipo 11 involucrada en los procesos de replicación, transcripción y recombinación del DNA. Está compuesta por dos subunidades A codificadas por el gen gyrA y dos subunidades B codificadas por el gen gyrB. Produce superenrollamiento negativo sobre DNA circular, y separa reversiblemente DNA concatenado, procesos que requieren ATP. La enzima causa el rompimiento de las dos cadenas de DNA y, posteriormente, las reunifica. Las quinolonas actúan sobre el DNAgirasa inhibiendo su actividad.
Hasta ahora no se han descrito enzimas bacterianas capaces de hidrolizar o inactivar quinolonas; en cambio, se han descrito mutaciones en los genes gyrA y gyrB que producen resistencia al ácido nalidíxico, así como también que las mutaciones sobre el gen gyr A confieren resistencia a las nuevas quinolonas. Las mutaciones que confieren resistencia a quinolonas se presentan en el cromosoma bacteriano y nunca en plásmidos.
RNA polimerasa. Rifampicina. Este antibiótico actúa sobre la subunidad 13 de la RNApolimerasa, inhibiendo la extensión del RNA durante su síntesis. Esta resistencia es común en enterobacterias y puede desarrollarse también en estafilococos, N.meningitidis y H.influenzae (5-9).
Alteraciones en la permeabilidad o transporte
Modificación de la membrana externa. Esto hace referencia a betalactámicos y aminoglucósidos.
En organismos Gram negativos, la membrana externa es de gran importancia en la resistencia intrínseca a diversos antimicrobianos. La permeabilidad se ve directamente afectada por el tamaño, carga, número y naturaleza hidrofóbica tanto del antibiótico como de las porinas (poros en la membrana). La resistencia con los aminoglucósidos no solamente es por permeabilidad disminuida sino también por falta de transporte.
Modificaciones en sistemas de transporte. Para la penetración de un antibiótico dentro de un microorganismo, se necesita del sistema de transporte de la bacteria. La resistencia bacteriana por este mecanismo es baja y puede vencerse aumentando la dosis del antibiótico; pero cuando esta resistencia está acompañada por otros mecanismos también de resistencia, el aumentar la dosis no es garantía para vencerla.
Tetraciclina. La actividad antibacteriana de las tetraciclinas se basa en su capacidad para alcanzar una concentración crítica capaz de bloquear la unión del complejo aminoacil-tRNAGTP- factor de extensión Tu, con el sitio del receptor en la subunidad 30S del ribosoma inhibiendo así la síntesis de proteínas. Este grupo de antibióticos posee un amplio espectro de actividad antimicrobiana y una baja toxicidad, por lo cual se han utlizado tanto en animales como en humanos en una gama amplia de enfermedades; como consecuencia del abuso en su prescripción, su eficacia se ha visto reducida por el aumento progresivo de la resistencia bacteriana (5,6,8,9).
Mecanismos de Resistencia de Patógenos Específicos
En los hospitales y especialmente en las UCI hay gérmenes que ocasionan mucha morbilidad y mortalidad y que elevan los costos tanto para los centros hospitalarios como para las empresas y las familias de los pacientes infectados.
Debido a su importancia creo que es necesario enumerarlos y describir algunas de sus características más notorias.
Estafilococo coagulasa negativo
Las dos especies más frecuentes son el S. Epidermidis y el S. Haemolyticus, que son gérmenes resistentes a múltiples ~atibióticos. El primero se consideraba anteriormente como germen contaminante de la piel pues hace parte de la f10ra normal de la misma.
Las infecciones ocasionadas por este germen tienen que ver con cuerpos extraños como las relacionadas con catéteres, prótesis, injertos vasculares y válvulas; shunts para hemodiálisis, diálisis peritoneales y fluidos cerebroespinales.
La resistencia es transmitida fundamentalmente por plásmidos y se hace casi con la totalidad de los antibióticos actuales especialmente penicilina, eritromicina, clindamicina, tetraciclina, cloramfenicol, TMP/SXT, cefalosporinas y aminoglucósidos, donde puede estar por encima de 50%.
La meticilino resistencia en estos gérmenes es igual a la MRSA de S.aureus.
Estafilococo aureus
Este germen es el más fuerte de los microorganismos no productores de esporas pues es capaz de sobrevivir en condiciones ambientales no favorables.
Coloniza sobre todo a pacientes comprometidos inmunológicamente y es la causa más común en la infección de la herida y en la neumonía nosocomial.
La resistencia intrínseca también llamada meticilino-resistencia. es cromosómica. Por la producción de penicilinasa hace resistencia rápidamente a la penicilina pero últimamente se ha visto que también ha hecho a las quinolonas y a la vancomicina.
Enterococo
Poco se conoce la forma como ocasiona infección. No es tan virulento como el estafilococo o el estreptococo. En pacientes debilitados y comprometidos inmunológica y nutricionalmente, con facilidad coloniza las válvulas cardíacas produciendo endocarditis, y el epitelio renal ocasionando infección urinaria.
La resistencia es cromosómica. Todos son intrínsecamente resistentes, relativamente a los antibióticos betalactámicos y aminoglucósidos; pero esta resistencia se puede vencer si durante el tratamiento se combina un antibiótico que actúe sobre la pared celular y un aminoglucósido, así que podría combinarse un betalactámico o vancomicina más aminoglucósido.
Desde 1980 se ha reportado resistencia del enterococo a la vancomicina y se ha visto que es de tres tipos: VanA,VanB y VanC cuya característica es que sea alta, moderada o baja a la misma.
Klebsiella pneumoniae y Escherichia Coli
Se consideran juntas porque tienen mecanismos de resistencia con características similares.
La resistencia es mediada por plásmidos y fundamentalmente los que codifican betalactamasas de espectro extendido (ESBL); por eso su resistencia es a un grupo amplio de antibióticos como carbenicilina, ampicilina, aminoglucósidos, cefalosporinas, ceftazidima, aztreonam, ceftriaxone y cefoxitin. Parece que el imipenem todavía permanece activo contra estos gérmenes, además de amikacina, cefmicina y los inhibidores de betalactamasas como piperalizinaftazobactam, antibióticos ausentes en nuestro país. Están asociadas a infecciones de la herida, tracto urinario y biliar; pero, K. Pneumoniae produce fundamentalmente una neumonía lobar que generalmente aparece en pacientes inmunosuprimidos y debilitados llamándose por esto infección oportunista.
Organismos SPACE
Esta es una sigla en inglés que significa: S (serratia spp), P (P aeruginosa), A (A. baumanii), C (Citrobacter spp), E (Enterobacter spp).
Son bacilos Gram negati vos asociados a infección nosocomial especialmente del tracto respiratorio inferior en pacientes con ventilador e inmunocomprometidos.
Presentan resistencia mediada por cromosomas. La producción de betalactamasas es inducida por dos mecanismos, ya sea mediante la exposición de un inductor que puede ser cefoxitin, imipenem, ceftazidime o acido clavulánico, o por mutación espontánea.
A causa de que son organismos que rápidamente hacen resistencia, es conveniente, para tratar infecciones producidas por estos gérmenes, combinar una cefalosporina de tercera o cuarta generación o penicilina antiseudomona con aminoglucósido y tluorquinolona (l 0-16,23).
Prevención de la Resistencia Bacteriana
La prevención se puede fundamentar sobre tres pilares: vigilancia epidemiológica, uso racional de antibióticos y control de la infección intrahospitalaria.
Vigilancia epidemiológica
Es de primordial importancia la creación de un Comité para la vigilancia epidemiólogica o Comité de infecciones, pues dará información sobre la frecuencia, magnitud, tipo de infección, por sitio y por servicios. Además, proporciona información requerida para romper el ciclo de usar antibióticos cuando no se conoce bien su eficacia. Es bastante frecuente encontrar formulación hospitalaria sin ningún control y bajo el capricho del conocimiento científico que el facultativo cree tener bien sea por información bibliográfica o traída de protocolos de otros centros hospitalarios. El laboratorio microbiológico es de suma importancia, pues dará información de la flora hospitalaria, tanto interna como externa, y así se puede conocer la eficacia del medicamento antimicrobiano utilizado para determinado germen. El frotis, cultivo y antibiograma es una trilogía indispensable.
Uso racional de antibióticos
Implica educación médica permanente. Conocer la farmacología y farmacodinamia de la droga así como la flora endógena normal y la patógena.
Por lo general, los antibióticos ·se usan erróneamente ya se por mala eJt:¡cción, uso excesivo en profilaxis quirúrgica o localmente. Es condición indispensable el diagnóstico preciso y el conocimiento de las indicaciones y dosis del antibiótico elegido.
En las Tablas 1 y 2, se muestra la susceptibilidad antimicrobiana en la Clínica Universitaria San Rafael de Santafé de Bogotá, durante los años 1996 y 1997.

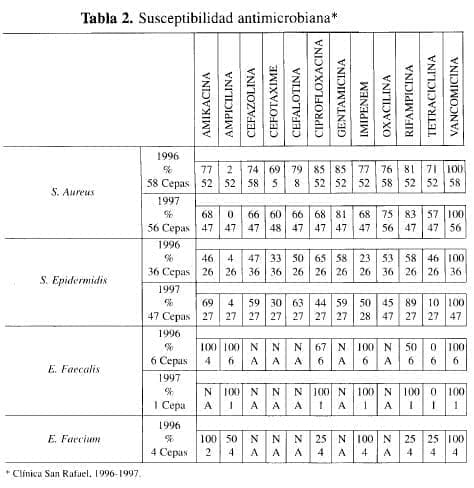
Se podrá apreciar claramente cómo cambia la eficacia de la droga de un año a otro y cómo aumenta la resistencia en el mismo centro hospitalario. La eficacia de las cefalosporinas no es la misma, a pesar de ser de primera, segunda o tercera generación; lo mismo puede decirse para los aminoglucósidos. La vancomicina, afortunadamente no muestra resistencia para los estafilococos dorados (aureus) y epidermidis, aunque comparados estos dos gérmenes, el S. Epidermidis muestra más resistencia. El E. faecalis es muy sensible a varios antimicrobianos en la muestra examinada. La Ps. Auriginosa y la Serratia marcescens son demasiado resistentes (22).
Es aconsejable, entonces, que en cada centro hospitalario, se constituya un Comité de Infecciones con buen respaldo por las directivas y el personal científico, así como un laboratorio de microbiología con respaldo científico, para que se conozca la flora hospitalaria y se pueda dictar dentro del Comité una política racional para la selección de antibióticos a fin de no dejar que caprichosamente se prescriban antimicrobianos según el criterio caprichoso de cada médico.
Control de la Infección Hospitalaria
Se basa en la prevención
Cada vez cobra más importancia la infección por estafilococo aureus meticilino resistente (MRSA), estafilococo epidermidis meticilino resistente (MRSE) y el enterococo vancomicina resitente (EVR), sobre todo en las unidades de cuidados intensivos para pacientes quirúrgicos.
El aseo cuidadoso de las habitaciones, salas de cirugía, unidades de cuidado intensivo y urgencias para limpiar las superficies que han estado en contacto con el paciente infectado, debe hacerse con sustancias que sean efectivas contra estos gérmenes como el hipoclorito de sodio, alcohol isopropílico o los compuestos yodados. El lavado de manos, medida tan sencilla, ha sido y seguirá siendo pilar fundalmental del control de la infección hospitalaria. Esta medida debe realizarse antes y después de tener algún contacto con cualquier paciente pero en especial con el paciente infectado para evitar la infección cruzada y la transmisión múltiple de la misma.
El aislamiento adecuado del paciente contagioso así como el manejo de pacientes inmunosuprimidos, mejorará mucho el control de la infección y contribuirá a no aumentar la resistencia bacteriana (17-22).
Referencias
1. Levy SB: Antibiotic resistence. Microbial adaptation and evolution. New York Plenum Press; 1992
2. Infectología y microbiología clínica; 1994
3. Bryan LE: General mechanism 01′ resistence to antibiotics. J.Antimicrob Chemother. 1989; 22 :1-15
4. Medeiros AA: Lactamasas. Br Med Bull 1984; 40:18-25
5. Kelly JA , Dideberg O, et al: On the origen 01′ bacterial resistence to penicillin. Science 1986; 231: 1429-31
6. Mayer KH: Review 01′ epidemie aminoglucoside resistence world wide. Am J Med 1981; 80:56-64
7. Cozarelli R: DNA gyrasa and the supercoiling 01′ DNA. Science 1980; 207:953-60
8. Fisher L, Lawrence J, et al: Ciprofloxacin and the fluoroquinolons. J Med 1989; 87:25-85
9. Kunin CM : Resistence to antimicrobial drugs. Ann Inter Med 1993; 118:557-61
10. Murray BE: Can antibiotic resistence be controlled? N Engl J Med 1994; 330: 1229-30
11. Goldmann DA, Weinstein RA. et al. Strategies to prevent and control the emergence and spread 01′ antimicrobial resistence microoganisms in hospitals. Jama 1996; 275:234-40
12. Hirschman SZ, Meyers BR, et al: Use 01′ antimicrobial agents in a university teaching hospital. Arch Int Med 1988; 148:2001-7
13. Lesar TS. Briceland LL, et al: Medication prescribing errors in a teaching hospital. Jama 1990; 263:2329-34
14. Leibovici L, Konisberger H, et al: Patients at risk for inapropriate antibiotic treatment 01′ bacteremia. J Int Med 1992; 231 :371-4
15. Wunderink RG: Mortalility and ventilation associated pneumonia. Chest 1993; 104:993-5
16. Neu HC : The crisis in antibiotic resistence. Science 1992; 257: 1064-73
17. Wenzel RP, Nettleman. et al: MRSA: implications for the 1990s and effective control measures. Am J Med 1991; 91(3B):22Is-7s
18. Holzheimer R. Werner H. et al: The challenge ofpostoperative infections.lnfControl Hosp Epid 1997; 18:449-56
19. Weber D, Rutala W: Role 01′ environmental contamination in the transmission 01′ Vancomycin Resistant Enterocci. Inf Control Hosp Epid 1997; 18:306-9
20. Saurina G, Landuan D, et al: Activity 01′ disinfectants against Vancomycin resistant enteroccus faecium. Inf Control Hosp Epid 1997; 18:345-7
21. Shannon T, Edgar P. et al: Much ado abaut nothing :MRSA. J Burn Care Rehab 1997; 18:326-31
22. Boletín del Comité de Infecciones. ClínicaUniversitaria San Rafael. 1996 y 1997
23. Jenkins S: Mechanisms ofbacterial antibiotic resistenee. New Horizons 1996; 4(3 ):321- 31.
Correspondencia:
Doctor Iván Baene. Hospital Clínica San Rafael. Santa Fe de Bogotá, D.C.
Doctor Ivan Baene Férez, Prof de Cirug., Univ. Nueva Granada; Jefe de Cirug. Gral., Hosp. Universo Clínica San Rafael; Santafé de Bogotá, D.C., Colombia.

La resistencia de las bacterias a los antibióticos es un peligro potencial para todos
Como Odontólogo haré hincapié en tres puntos específicos que en mi opinión profesional merecen atención:
1) La responsabilidad del profesional al momento de prescribir un antibiótico, ya que la resistencia a los mismos es causada tanto por un uso deficitario como un uso excesivo del mismo, y en esto tenemos mucho que contribuir los profesionales y las instituciones
2) La responsabilidad del ciudadano en países como el mío, Venezuela, donde aún en algunas farmacias los antibióticos son de libre venta al público y hay personas que aún los adquieren para supuestamente curar una gripe.
Allí los profesionales y las instituciones también tenemos mucho que contribuir, tanto en la parte cultural de la sociedad, como en presionar para que hayan nuevas leyes que estrictamente indiquen que los antibióticos únicamente se pueden adquirir con prescripción
3) La responsabilidad industrial por así decir, el uso desmesurado e irresponsable de antibióticos en animales de cría también ha contribuido en mucho a causar la resistencia que hoy padecemos
Aprendí mucho con este artículo, gracias por compartirlo
Saludos desde Caracas