A. LECHTER, MD, scc; J.D. NAAR, MD; o. ANDRADE, MD.
Palabras claves: Paraganglioma, Compresión neurovascular, Arteriografía carotídea, Disección subadventicia, Bifurcación carotídea ensanchada.
Los tumores del cuerpo carotídeo (paragangliomas, quimiodectomas), se originan en el tejido paragangliónico de la bifurcación carotídea; son lesiones de lenta evolución que aumentan gradualmente en el curso de los años y pueden comprimir las estructuras neurovasculares del cuello; su transformación maligna es rara. La lesión, a menudo asintomática, puede aparecer en la tercera o cuarta décadas de la vida y es más frecuente en personas que viven a grandes alturas, y en pacientes con enfermedad pulmonar obstructiva crónica (EPOC).
El propósito de este estudio es enfatizar los beneficios de nuestra técnica quirúrgica, ya que con ella hemos obtenido excelentes resultados.
Vale destacar la utilidad de la angiografia carotídea bilateral en el estudio y tratamiento de esta patología. En nuestros pacientes tratados quirúrgicamente no se presentó ninguna complicación definitiva, y la única morbilidad fue una paresia de la rama mandibular del nervio facial y otra del hipogloso; tampoco hubo mortalidad.
Introducción
El tumor del cuerpo carotídeo es el tumor de la región de la cabeza y el cuello que más controversia ha generado en todas las épocas, debido a su potencial maligno y a las diferencias de opinión en su estudio y tratamiento (1). Desde que se descubrió, se le confundió con otros tumores; Von Haller describió la estructura anatómica del cuerpo carotídeo en 1743 (2).
Félix Jacobo Merchán, un patólogo de Berlin, describió en 1881 la estructura histopatológica de este tumor (2). Kohn en 1903 lo clasificó como un paraganglioma cromafín pensando que era de origen simpático (3). En 1949 Lattes y Waltner lo denominaron paraganglioma no cromafín, reconociendo que su función endocrina era dudosa (4). En 1950 Mulligan lo denominó quimiodectoma (5).
El cuerpo carotídeo tiene funciones quimiorreceptoras íntimamente relacionadas con sus ramas nerviosas aferentes, mediadas por varias clases de células epiteliales, a saber: a) tipo 11, en las cuales se han demostrado gránulos de catecolaminas que pueden originar neoplasias funcionantes como los feocromocitomas (6-8); b) tipo 1, a las cuales no se les han demostrado gránulos de adrenalina, nora drenalina y otras sustancias vasoactivas por microscopía electrónica. Se cree que los tumores del cuerpo carotídeo no son funcionales debido a que se originan en las células tipo 1, las cuales en el período embrionario nacen en la cresta neural y emigran paralelamente con las células del sistema nervioso autónomo; esta es la razón por la cual a estas neoplasias se les da también nombre de paragangliomas (9,10).
Algunos autores han encontrado tumores del tejido quimiorreceptor productores de catecolaminas (11-13).
El propósito de este trabajo es hacer un análisis de la literatura y enfatizar sobre los beneficios de nuestra técnica quirúrgica, con la cual hemos obtenido una morbimortalidad de cero.
Material y metodos
Durante el período comprendido entre 1982 a 1990 estudiamos 23 casos de paragangliomas del cuerpo carotídeo en el servicio de Cirugía Vascular del Hospital Militar Central de Bogotá. Se revisaron las historias clínicas de los pacientes, se determinó el sitio del tumor por examen físico y por imágenes diagnósticas y se confirmó el diagnóstico por exámenes histopatológicos. Se analizó la edad, sexo, antecedentes, características clínicas, estudios diagnósticos, tratamiento, presencia de malignidad, recurrencias, complicaciones y morbimortalidad.
La edad de los pacientes osciló entre 28 y 84 años, con un promedio de 59.5 años. De los 23 pacientes, 16 fueron mujeres y 7 hombres.
Se diagnosticaron enfermedades concomitantes como hipertensión arterial (48%), EPOC (17%), diabetes 17% y tabaquismo (13%).
Las manifestaciones clínicas fueron, masa (100%), inmovilidad del tumor en sentido vertical (100%), ausencia de soplo (100%) y signo de la esponja (80%).
Se utilizaron métodos paraclínicos de diagnóstico como arteriografía carotídea (74%), pool carotídeo (57%) y escanografía (22%).
Los tratamientos empleados fueron, resección (74%) y observación (26%).
Sólo se presentaron complicaciones neurológicas temporales, tipo paresia de la rama mandibular del facial y del hipogloso.
No hubo morbilidad defmitiva ni mortalidad.
Discusión
Los tumores del cuerpo carotídeo se presentan desde la infancia hasta las edades más avanzadas, con una incidencia mayor en la quinta década de la vida (14). Son funcionales en menos del 2% de los casos, malignos en el 10% y multicéntricos o bilaterales en el 15% (15). No se encontraron estas características en ninguno de nuestros casos. Los parangliomas pueden ocurrir en el oído medio, laringe, nervio vago, arco aórtico y dentro de las vísceras abdominales (hígado, vejiga y duodeno) (16). El cuerpo carotídeo se deriva de elementos mesodérmicos del tercer .’ arco branquial y de elementos neurales originados del ectodermo de la cresta neural. El cuerpo carotídeo es una pequeña masa ovoide de color rosado grisáceo, que está localizado en la bifurcación de la arteria carótida primitiva; su diámetro mayor mide en promedio 0.5 cm y es la colección más grande de células quimiorreceptoras que existe en el organismo. Su irrigación sanguínea esta dada principalmente por ramas de la carótiaa externa, y su retorno venoso pasa a las venas laringofaríngeas o linguales; la inervación es sensorial y llega por el nervio gloso faríngeo. El control químico de la respiración tiene elementos centrales y periféricos, siendo el principal de estos últimos, el cuerpo carotídeo; estructura muy sensible que incrementa su actividad ante la hipercapnia, hipoxemia y la acidosis. Es el órgano que posee el más alto Oujo del organismo (cerca de 2.000 mL/100 grde tejido/ minuto).
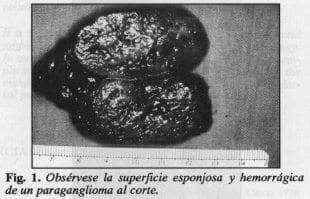
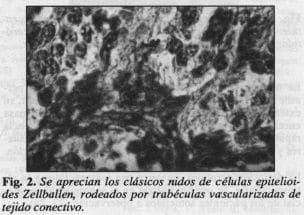
Los paragangliomas son tumores bien circunscritos, homogéneos y al corte son hemorrágicos y esponjosos (Fig. 1). Su tamaño es variable y algunos logran grandes dimensiones antes de ser diagnosticados. En nuestra serie el tumor de mayor tamaño midió 10x5x4 cm. Microscópicamente están compuestos por nidos de células epitelioides Zellballen, con citoplasma eosinófl1o granular y trabéculas vascularizadas de tejido conectivo (Fig. 2) (17). Aunque son tumores bien circunscritos, no tienen cápsula (18). Los criterios patológicos de malignidad están basados en el grado de atipia celular y mitosis, invasión local y diseminación a distancia. Los tumores del cuerpo carotídeo pueden crecer inexorablemente si no se resecan, y se ha informado una tasa de mortalidad del 8% en los casos no tratados (19). La morbilidad que se asocia a los tumores que no se resecan es significativa e incluye parálisis progresiva de los nervios craneanos, disfagia, oclusión de la vía aérea, extensión a la base del cráneo con inmtración del sistema nervioso central y sintomatología originada en el centro barorreceptor como mareo, vértigo y lipotimia (20). Nunca se ha informado un caso de regresión espontánea (1). La supervivencia a largo plazo de los pacientes a quienes se les reseca el tumor es la misma que para la población general.
Estos tumores ocurren usualmente como masas asintomáticas en el cuello; sin embargo, pueden presentarse con dolor, cefalea, vértigo, diaforesis, cambios visuales y, hasta en un 20%, con parálisis de los nervios craneanos (IX, X, XI y XII) (1, 2).
Con la compresión de la masa el tumor tiende a disminuir de tamaño (signo de la esponja); clásicamente estas neoplasias son móviles lateralmente pero no verticalmente. Cualquier masa con estas características en la región lateral del cuello debe ser sometida a una angiografía cerebral bilateral por vía transfemoral ya que confirma el diagn6stico y permite la evaluación de enfermedad arterioesclerótica oclusiva coexistente y determina la irrigación sanguínea del tumor (15).
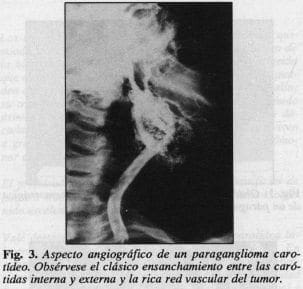
Es importantísima la demostraci6n de circulación cruzada en el cerebro para la posibilidad eventual de un pinzamiento carotídeo; la presencia de una masa oval que ensancha el ángulo de la bifurcaci6n de la car6tida primitiva y desplaza a las car6tidas interna y externa, es patognomónica de este tumor (Fig. 3).
La escanografía con medio de contraste endovenoso permite apreciar las extensiones medial y lateral del tumor, su extensión a la base del cráneo y el compromiso de la masa encefálica (21). La escanografía dinámica o de secuencia rápida, mejora la resoluci6n entre las estructuras vasculares y podría ser en el futuro el estudio de primera elección.
La perfusi6n carotídea dinámica con radionúclidos y la ultrasonografía, se pueden utilizar en el seguimiento secuencial de los pacientes sometidos a observación (23, 24).
El Duplex scaning permite evaluar la presencia de placas ateromatosas en la luz del vaso y confirmar el tumor.
La base del tratamiento de los tumores del cuerpo carotídeo es la resección quirúrgica completa, pero en pacientes ancianos o con enfermedades graves concomitantes, se puede adoptar una conducta expectante, si no hay síntomas y si el tumor es de crecimiento lento (25).
El tratamiento quirúrgico de estos tumores ha generado una gran controversia, desde que Reigner en 1880 llevara a cabo el primer intento de resección quirúrgica; en el acto operatorio fue necesario seccionar y ligar la arteria carótida, la vena yugular y los nervios vago, hipogloso y simpático.
Scudder en 1903, resecó exitosamente y sin ninguna complicación un paraganglioma carotídeo en Estados Unidos. La frecuencia de ligadura de los vasos carotídeos ha disminuido a través de los años; entre 1928 y 1939 la incidencia de ligadura fue del 82%, mientras que en la década de los 40’s s610 se practicó ligadura en el 25% de los casos; concomitantemente la mortalidad también descendió del 50% en los años 30’s a 25% a finales de la década de los 50’s. Gordon Taylor, el famoso cirujano británico, describe en 1941 la “línea blanca”, un plano de disección en el cual la pared de los vasos permanecía estructuralmente respetada por el tumor (26).
Lahey y Warren describen en 1949 la disecci6n subadventicia en la cual la resección del tumor conlleva a la extracción de la adventicia (13). Crile en 1951 lleva a cabo la resección de un paraganglioma junto con la arteria carótida y realiza la interposici6n de un injerto heterólogico(27).
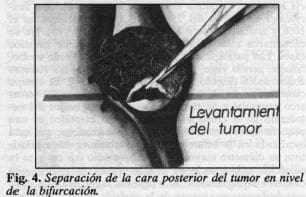
La técnica quirúrgica que empleamos de rutina utiliza una vía de acceso estético por medio de una incisión transversa sobre la parte media de la masa tumoral; se exponen adecuadamente la carótida interna, la carótida común y la bifurcación carotídea; las venas que drenan el tumor se seccionan y ligan, y se separa la masa de los tejidos adyacentes; se inicia luego la separaci6n del tumor de la adventicia de la carótida común, debido a que la irrigaci6n del tumor proviene de la bifurcaci6n carotídea y de la carótida externa; la disecci6n se hace primero en estos sitios, donde usualmente hay un plano de disecci6n areolar entre el tumor y la arteria, excepto en su uni6n subadventicia en la pared posterior de la bifurcación; nuestra técnica acomete directamente, luego de hacer el plano de divaje en la carótida común, la unión de las carótidas interna y externa levantando este punto crucial del tumor de la bifurcaci6n carotídea. Una vez separado el tumor de la bifurcación, éste es fácilmente resecable traccionándolo hacia afuera o hacia adentro (Fig. 4). Esta maniobra constante nos ha permitido conservar los vasos y nos ha facilitado la disección; ésta debe efectuarse pegada a la pared de las arterias para disminuir el riesgo de lesionar el nervio laríngeo superior y el recurrente. Actualmente la incidencia de lesión de los nervios craneanos permanece en el 40%; una explicación parcial a este problema es que los pacientes ya tienen compromiso de los pares craneanos antes de la cirugía; sin embargo, la lesión es temporal en el 50% de estos pacientes (15); en nuestra casuística no tuvimos ningún caso de lesión definitiva de los pares craneanos. En un caso hubo necesidad de ligar la arteria carótida externa, y este paciente desarrolló un síndrome de Horner temporal, que se resolvió en forma espontánea; de rutina no sacrificamos este vaso para facilitar el control del aporte vascular y la movilización del tumor, como lo recomienda el grupo de San Francisco (28).
Con esta técnica no hemos tenido morbilidad definitiva ni ha habido recurrencias.
Abstract
Carotid body tumors (paragangliomata, chemodectomas) originate at the paraganglionic tissues of the carotid bifurcation. They are slowly-evolving lesions which show a gradual increase in size during the years and may eventually compress the neurovascular structures in the neck; they rarely become malignant. The lesion, which is ofien asymptomatic, may appear during the third or fourth decade of life and is found more frequently in people living at high altitudes and in patients with chronic obstructive pulmonary disease (COPD).
The purpose of this study is to stress the benefits of our surgical technique with which we have obtained excellent results.
It is important to stress the usefulness of bilateral carotid angiography in the study and treatment of this pathology. In our surgically treated patients there were no final complications and the only morbidity was a paresis of the mandibular branch of the facial nerve and one hypoglossal paresis. There were no deaths.
Referencias
1. Reese H E, Lucas R N, Besgman P A: Malignanl carolid body tumor. Ano Surg 1963; 157 (2):232-4
2. Lahey F H, Warren K W: A long lerm appraisal of carolid body lumors wilh remarks on lheir removal. Surg Gynecol Obslel 1951; 92: 481
3. Kohn A: Die paraganglien. Arch Miks Anal 1903; 62:263 (Javid Hoshang Arch Surg 1976; 11I:44)
4. Lanes R, Waltner J G: Nonchromafin paraganglioma of lhe middle ear (carolid body like tumor glomus jugulare). Cancer 1949; 2:447-68
5. Mulligan R M: Chemodectoma in lhe dogo Aro J Palhol 1950; 26:680
6. Coslero 1: Slruclure of lhe carolid lumors. J Palhol 1961; 38:127
7. Nelson W R: Carolid body lumors: Surgery 1962; 51:326
8. Tollen R S: Terminology of carolid body lumors: confusion al lhe cross roods. Hum Palhol, a Clinical Quarlerly 1973; 4:454
9. Javid Hushab: Maslery of surgery. Nyhus-Baker. Boston, Toronlo, Linle Brown and company; 1 Ed, 1984
10. Irons B J Jr: Paraganglionares del cuello. Análisis clínico e hislopalológico de 116 casos. Clin Quir Norte Aro 1977; 57: 573
11. Gopalakrishnan R el al: Cardiac paragangli.ma (chemodectoma). A case report and review of lhe lileralure. J Thorac Cardiovasc Surg 1978; 76 (2):183-9
12. Pelers J L 1:1 al: Diagnosis of carolid body chemodecloma wilh dynamic radionuc1ide perfusion scanning. Aro J Surg 1979; 137 (5):661-4
13. Ward P H el al: Diagnosis and lrealmenl of carolid body lumors. Ann 0101 Rhinol Laringol 1978; 87:614-21
14. Mc Ilralh D C, ReMine W H: Carolid body tumors. Surg Clin Norlh Aro 1963; 43:1135-44
15. Meyer F B, Thoral M S, Pearson B W: Carolid body tumors. J Neurosurg 1981; 64: 377-85
16. RUlherford R B: Vascular Surgery. Third Edilion, W. B. Saunders, 1989
17. Robbins S L, Colran R S: Palologic basis of diseasse. Second Edilion, Philadelphia. W.B. Saunders. 1979; 1406-7
18. Harringlon S W, Clagen O T, Docklery M B: Tumors of lbe caro lid body. Clinical and palhological consideralions of lwenly lumors affecling nineleen palienls (one bilaleral). Ann Surg 1941; 114: 820-33
19. Lees C D, Levinell L, Beven E G Tucker H M: Tumors of lbe carolid body. Aro J Surg 1981; 142: 362
20. Denl T L, Thompson N W, Fry W J: Caroolid body lumors. Surgery 1976; 80: 365-72
21. Rangwala A F el al: Soft lissue melaslasis of a chemodecloma: a case reporl and review of lhe lileralure. Cancer 1978; 42 (6): 2865
22. Sbugar M A, Mafee M F: Diagnosis of carolid body lumors by dynamic compularized lomography. Head Neck Surg 1982; 4: 518-21
23. Goioding G A W: Gray-scale ultrasound deleclion of carolid body tumors. Report of two cases. Radiology 1979; 132: 409
24. Pelers J L el al: Diagnosis of a carolid body cbemodecloma wilb dynamic radionuclide perfussion scanning. Aro J Surg 1979; 137 (5): 661-4
25. Weil J V el al: Hypoxic venlilalory drive in normal mano J Clin Invesl 1970; 49: 1061
26. OIarle F, Sabogal E: Paragangliomas del cuerpo carolídeo. En: OIarle F, Arislizábal H, Bolero M, Reslrepo J, eds.: Cirugía, 18 , Tomo 11; Medellín, U. de A., 1983, pp. 833-9
27. Miginiac G: Mem de l’Acad de Chir 1937; 63: 165-6
28. Meyer F B, Sundl and Pearson. Carolid Body lumors: a subjecl review and suggesled surgical approach. J Neurosurg 1986; 64: 377-85
29. Jaramillo Z, Valencia J: Tumor del cuerpo carolídeo. Med Caldas 1982 sep; 4 (1): 14-21
30. Fonseca E: Tumores del cuerpo carolídeo. Rev Col Cirug 1986 dic; 1 (3): 146-8
Doctores: Abraham Letcher, Prof. U. Mil. “Nueva Granada”, Jefe del Dpto. de Cirug. y del Servo de Cirug. Vascular y Angiologia; Julio David Naar, R-N de Cirug. Gral.; Oscar Andrade, R-N de Cirug. Gral., Hosp. Militar Central, Bogotá, D.C., Colombia.