Para estudiar la influencia del tejido heterogéneo en formación de arritmias, se diseñó un juego de simulaciones que representa un corte transmural del ventrículo izquierdo de 300×150 células (34) en presencia de una lesión semicircular isquémica regional en la parte medial a partir del epicardio.
Este diseño de aglomerados circulares de células del medio miocardio corresponden con datos experimentales tomados de Yan y colaboradores, junto con los datos más modernos de Poelzing para datos de inmunoetiqueta de Conexin 43 en corazón canino (35;36).
Para el tejido virtual diseñado la zona correspondiente con el endocardio, modelado en la parte izquierda, representando un 45% del área total, una zona epicárdica con el 20% del área total y dos isletas en forma circular que representa la distribución de las células M (37).
La heterogeneidad cardiaca es incluida en el modelo por medio de la corriente transitoria de salida Ito (38) y la componente lenta del rectificador de potasio IKs (39) con una relación de 23:7:15 entre las células del epicardio: medio miocardio: endocardio respectivamente. Los valores de conductancia se alteraron con base en el trabajo de simulación de Clayton (40). (Lea también: Comportamiento Antiarrítmico de la Hipoxia en Simulaciones de Pared Transmural Cardíaca en Presencia de Isquemia Sub-Epicárdica)
Modelo de Electrograma
La actividad eléctrica cardiaca involucra la forma del potencial de acción y su propagación a través del corazón. Esta actividad eléctrica determina las fuentes bioeléctricas. Cambios en el volumen conductor son a menudo extra cardiacos y se reflejan en el electrocardiograma (ECG). A partir del modelo de fuentes doble capa Geselowitz mostró que el ECG, calculado a partir de (6), puede dar información diagnostica sobre eventos acaecidos en el corazón (41).

Corrientes de lesión. Lesiones ocasionadas por isquemia en diferentes regiones de la pared cardiaca conllevan cambios en la forma, duración y propagación del potencial. Variaciones de la línea base y deflexiones del segmento ST son ejemplo de estas corrientes de lesión (42).
Defectos de conducción. Enfermedad de alguna estructura que comprometa el sistema de conducción o presencia de caminos accesorios anormales, ocasionan alteración en la velocidad de conducción. Potenciales dobles en ECG son índice de bloqueos de conducción (43).
Efectos iónicos. El potencial de acción depende de concentraciones extracelulares y corrientes únicas a través de la membrana. Alteraciones en corrientes iónicas inscriben la onda J, la onda T, y la onda U del ECG (44;45). Un programa en matlab (The Markwors inc) calcula el electrograma con base en una versión discreta de la ecuación (6) suponiendo un electrodo situado a 1 mm en el centro de la zona lesionada.
Resultados
Este trabajo al ser una simulación matemática con la que se quiere comprender el fenómeno de la hipoxia subepicárdica en simulaciones de pared transmural en presencia de isquemia, son innecesarias metodologías estadísticas para comprender y simular el fenómeno.
Influencia de las componentes de isquemia
La influencia en la repolarización ocasionada por las células M, en tejido comprometido con lesiones isquémicas, se convierte en un nuevo componente que altera el delicado balance energético del tejido volviéndolo mas vulnerable a iniciar eventos reentrantes.
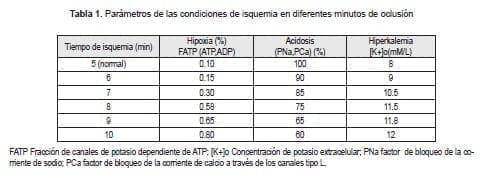
La Figura 4 muestra la simulación en pared transmural de isquemia regional con los tres principales componentes de la isquemia modelados en tejido heterogéneo. En la izquierda de la figura se muestra la distribución geométrica de las tres componentes celulares de la pared. Las condiciones de isquemia bajo las cuales se caracterizan las diferentes componentes son mostradas en la tabla 1 y corresponden al minuto ocho desde el comienzo de isquemia de cero flujo.
El primer fotograma (80 ms) muestra el frente de onda casi plano del potencial, los círculos que se observan corresponde con la despolarización de las células M diseñadas.
El segundo fotograma muestra la pronta repolarización de la zona isquémica. El tercer fotograma (240 ms) muestra el impulso prematuro aplicado con un intervalo de acople (CI) de 175 ms. En el fotograma 3 se observa el bloqueo del estímulo prematuro en la parte correspondiente a endocardio, a su vez, el frente de onda llega a la zona lesionada del tejido para bloquearse de forma unidireccional en epicardio isquémico.
El fotograma 4 muestra el frente elíptico, que se forma después del bloqueo y se propaga por todo el tejido hasta que la onda de potencial reversa su sentido de propagación en la parte distal de la lesión (fotograma 5) para finalmente bloquearse completamente de manera bidireccional y desaparecer como se muestra en los fotogramas posteriores.

