Estamos interesados en estudiar la influencia de la heterogeneidad de la pared cardiaca (funcional y lesionada por isquemia) y sus mecanismos iónicos como generadores de patrones reentrantes en isquemia aguda. Las diferentes alteraciones bioquímicas producidas por la isquemia (hipoxia, acidosis e hiperkalemia) han sido modeladas e incluidas en la descripción cinética de iones a través de la membrana desarrollada por Luo-Rudy (19-21). El modelo incluye 16 diferentes corrientes iónicas a través de la sarcolema (incluyendo diferentes corrientes de Na+, K+, y Ca2+, así como también bombas electrogénicas e intercambiadores), el vaciado de Ca2+ inducido por Ca2+ y almacenes de Ca2+ intracelular. La estructura matemática básica de una célula cardiaca del modelo es:
![]() donde Im es la corriente a través de la membrana, Cm es la capacitancia de la membrana celular, es el potencial, Iion es la suma de las corrientes por unidad de área en la descripción de Luo-Rudy, y Iapp es el estímulo de corriente aplicado. El formalismo de Hodgkin-Huxley para la dinámica de las compuertas iónicas que describen el canal y la especificidad matemática con la que se puede modelar cada corriente iónica en el modelo fueron descritas en Henao (22).
donde Im es la corriente a través de la membrana, Cm es la capacitancia de la membrana celular, es el potencial, Iion es la suma de las corrientes por unidad de área en la descripción de Luo-Rudy, y Iapp es el estímulo de corriente aplicado. El formalismo de Hodgkin-Huxley para la dinámica de las compuertas iónicas que describen el canal y la especificidad matemática con la que se puede modelar cada corriente iónica en el modelo fueron descritas en Henao (22).
![]()
Si el tejido cardiaco se asume como un syncitium funcional (conglomerado de células que actúan como una unidad funcional), entonces se puede describir mediante la ecuación del cable, desarrollada por Wiedmann (23). Una extensión de dicha ecuación para un tejido bidimensional espacialmente extendido se suscribe como:
donde es el operador de Laplace, y D es el tensor difusión del voltaje a través del medio, en modelos isotrópicos el tensor se convierte en una cantidad escalar. La estructura del tejido 2D modelado se muestra en la parte A de la Figura 3. En el tejido virtual modelado (30×15 mm2), cada célula interna (sin fronteras) se toma como un nodo con cuatro puntos adyacentes conectados por resistencia lineales. Algunos estudios recientes (24;25) dan soporte a dicho modelo, y por lo tanto cada conexión longitudinal y transversal puede ser programada individualmente, así la anisotropía lineal para el tejido puede ser introducida en modelo. Es de aclarar que en el tejido cardiaco se define un tensor de conductividad anisotrópica que depende de las propiedades materiales de la fibra cardiaca. Al tomarse una anisotropía lineal en el tejido se define una conductividad extracelular como infinita y la conductividad longitudinal es un 40% mayor que la transversal.
En nuestras simulaciones, se consideró un tejido representando una porción rectangular de pared transmural cardiaca sujeto a isquemia regional, como el representado en la parte B de la Figura 3. La naturaleza microscópica de la estructura del ventrículo es ignorada y así el tejido es tratado como un sistema continuo modelado por una ecuación de reacción-difusión:
 donde Sv es el cociente entre superficie y volumen celular, x y y son las resistividades en la dirección transversal y longitudinal respectivamente. Por propósitos computacionales, el tejido fue discretizado en porciones de 100×100 mm. La ecuación (3) fue resuelta utilizando el método numérico de operador partido. La parte de difusión de la ecuación se resolvió utilizando el esquema implícito de dirección alternante, mientras que el término de reacción se utilizo un método de Euler implícito. Un paso de tiempo de 18 ms fue escogido para evitar artefactos numéricos y la no convergencia del método numérico. Se utilizaron condiciones de no flujo en la frontera y los valores de resistividades celulares fueron escogidos de tal forma que la velocidad de conducción en dirección longitudinal fue de 50 cms-1 y en dirección trasversal fue de 13 cms-1 con un cociente anisotrópico en la velocidad de aproximadamente 4:1(26).
donde Sv es el cociente entre superficie y volumen celular, x y y son las resistividades en la dirección transversal y longitudinal respectivamente. Por propósitos computacionales, el tejido fue discretizado en porciones de 100×100 mm. La ecuación (3) fue resuelta utilizando el método numérico de operador partido. La parte de difusión de la ecuación se resolvió utilizando el esquema implícito de dirección alternante, mientras que el término de reacción se utilizo un método de Euler implícito. Un paso de tiempo de 18 ms fue escogido para evitar artefactos numéricos y la no convergencia del método numérico. Se utilizaron condiciones de no flujo en la frontera y los valores de resistividades celulares fueron escogidos de tal forma que la velocidad de conducción en dirección longitudinal fue de 50 cms-1 y en dirección trasversal fue de 13 cms-1 con un cociente anisotrópico en la velocidad de aproximadamente 4:1(26).
Protocolo de estimulación
El protocolo para estimular el tejido consistió de dos pulsos rectangulares (protocolo S1-S2). La amplitud del pulso de corriente aplicado es dos veces el umbral diastólico y su duración es de 2 ms (27). El primer pulso (diastólico) se aplica en la parte superior del tejido 50 ms después de comenzado el tiempo de simulación para efectos de estabilización de las variables independientes del modelo en la dirección longitudinal de la fibra cardiaca. El segundo estímulo (prematuro) se aplica al tejido en la misma parte con un intervalo de acople (CI) variable entre 170 y 220 ms de tal forma que puede formar en el tejido propagación total, colisión total, bloqueo bidireccional, o bloqueo unidireccional y finalmente un patrón reentrante.
Modelo de isquemia regional aguda
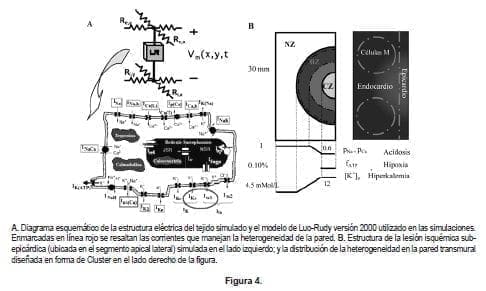
La parte B de la Figura 3 muestra la estructura electrofisiológica del tejido modelado (correspondiente al minuto ocho después del comienzo de la isquemia), en el cual existen diferentes zonas representando los cambios generados por la isquemia (28;29). El tamaño de estas zonas, así como los valores relevantes de los parámetros del modelo y sus gradientes espaciales han sido tomados de datos experimentales revisados por Coronel (30). Una zona central (CZ) de forma (semicircular) representando isquemia sub-epicárdica con su respectiva zona de borde (BZ) en la cual los parámetros relevantes para el modelo de isquemia cambian espacialmente y una zona normal de tejido epicárdico (NZ) rodeando la zona de borde. Los valores de los parámetros  que modelan la acidosis y la hiperkalemia en la lesión isquémica fueron descritos anteriormente por Ferrero (31). Es sabido que en hipoxia decrece pO2 después de la oclusión de la arteria coronaria llevando a disminuir la concentración intracelular de ATP y aumenta la concentración de ADP. Estos cambios afectan la activación de la corriente de potasio dependiente de ATP (IKATP), la cual permanece casi inactiva en miocardio normal. Usamos nuestro modelo de IKATP el cual considera que la corriente depende de las concentraciones de ATP, ADP, Mg+ intracelulares y de la concentración extracelular de K+, como también de la dependencia de los canales respecto del voltaje de membrana (32). La corriente y la fracción de canales abiertos considerados por el modelo se suscriben como:
que modelan la acidosis y la hiperkalemia en la lesión isquémica fueron descritos anteriormente por Ferrero (31). Es sabido que en hipoxia decrece pO2 después de la oclusión de la arteria coronaria llevando a disminuir la concentración intracelular de ATP y aumenta la concentración de ADP. Estos cambios afectan la activación de la corriente de potasio dependiente de ATP (IKATP), la cual permanece casi inactiva en miocardio normal. Usamos nuestro modelo de IKATP el cual considera que la corriente depende de las concentraciones de ATP, ADP, Mg+ intracelulares y de la concentración extracelular de K+, como también de la dependencia de los canales respecto del voltaje de membrana (32). La corriente y la fracción de canales abiertos considerados por el modelo se suscriben como:
Los niveles de ATP y ADP proporcionan una fracción de canales dada por fatp = 0.1% y fatp = 0.8% en la NZ y la CZ respectivamente (33). En la parte superior, el tejido es estimulado con diferentes intervalos de acople para caracterizar la reentrada y los electrogramas del tejido virtual. Se estudiaron los diferentes parámetros de isquemia descritos en la tabla 1.

