Lo más importante de esta entidad es el diagnóstico temprano con el fin de evitar secuelas a corto plazo; manifestaciones de hiperandrogenismo como procesos de virilización, macrogenitosomía precoz, talla baja, hirsutismo, acné, y a largo plazo infertilidad, enfermedad cardiovascular (ECV), diabetes, etc.
Los niños con HAC-NC deben ser cuidadosamente tratados, utilizando dosis de acuerdo al peso con el fin de evitar sub o sobre-tratamientos.
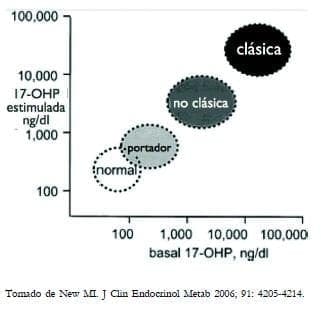
Figura 7.
Los objetivos del tratamiento son: 1) frenar la hipersecreción de ACTH, 2) mantener una homeostasis normal de energía y glucosa, 3) prevenir los signos y síntomas del exceso de andrógenos, 4) promover crecimiento normal, 5) mantener una adecuada maduración sexual y función gonadal durante la adolescencia y edad adulta, y 6) asegurar su fertilidad.
El médico quien trata estas pacientes debe tener buena preparación sobre el tema, debe hacer un buen empalme entre el médico pediatra y el médico de adultos con el fin de continuar el manejo de los pacientes en forma adecuada12.
El tratamiento debe manejar las manifestaciones del hiperandrogenismo y evitar el uso de dosis suprafisiológicas de esteroides para no caer en el hipercortisolismo y por lo tanto en las alteraciones a nivel de la mineralización ósea y los trastornos de la función gonadal, o la utilización de dosis muy bajas que no regulen adecuadamente el sistema endocrino y puedan evitar las complicaciones.
Las pacientes con diagnóstico de HAC-clásica se deben tratar durante toda la vida, haciendo ajustes de acuerdo a las condiciones de salud, estrés, obesidad, etc. Los pacientes con diagnóstico de HAC-NC se tratan hasta cuando hayan revertido los síntomas, a veces por variosaños. Se puede suspender periódicamente el tratamiento y reiniciarlo una vez se reactiven los síntomas, principalmente en los estados de estrés o enfermedad.
Se utiliza siempre la mínima dosis efectiva de los medicamentos más utilizados, los cuales son: hidrocortisona (Solucortef ®) 10-15 mg/ m2/día; prednisona (Meticortén ®) 10-15 mg/ m2/día o 5-7.5 mg/día por vía oral en dos dosis: 1/3 en la mañana y 2/3 en la tarde; o dexametasona (Deltafluorene ®) 0.6 mg/m2, 0.02 mg por kg/día o 0.25-0.375 mg/día o en forma interdiaria (un día sí otro no), administrado en las horas de la noche. En las pacientes con HAC-clásica de la variedad perdedora de sal se administra fluorohidrocortisona (Astonin ®), 0.05-0.1 mg/día por vía oral.
Cuando la terapia con esteroides a dosis fisiológica no logra su objetivo de disminuir la actividad androgénica suprarrenal y el hirsutismo y el acné son manifestaciones clínicas progresivas y refractarias al uso único de esteroides, es necesario utilizar otros medicamentos antiandrogénicos, o cuando al incrementar la dosis se corre el peligro de producir manifestaciones de hipercortisolismo, es necesario asociar medicaciones que controlen los síntomas de hiperandrogenismo y permitan los objetivos propuestos tales como acetato de ciproterona 2 mg mezclado con etinilestradiol 0.035 mg (Diane ®) o adicionando al tratamiento anterior (Androcur ®) 10 – 50 mg los primeros 14 días que se tome dicha mezcla, o espironolactona (Aldactone ®) 50 – 200 mg/día. Se debe analizar en el futuro si hay riesgo con la administración de drosperinona, debido a que es progestágeno antiandrogénico y con actividad antimineralocorticoide, lo que pudiera tener algún problema en el caso de presentar algún grado de alteración en los mineralocorticoides. En los pacientes prepúberes o púberes con diagnóstico de retardo en el crecimiento se puede agregar también hormona del crecimiento sola o en combinación con agonistas de la GnRH (GnRHa).
Recientemente se vienen utilizando en forma experimental nuevos esquemas de manejo, especialmente en aquellos casos de pubertad precoz, para retardar la pubarquia y la maduración ósea precoz, tal como la asociación de hidrocortisona (glucocorticoide), fludrocortisona (Astonin ®) (mineralocorticoide), flutamida (Eulexin ®), 10 mg/ kg/día, dividido en tres dosis, alrededor de 250 mg/día, finasteride (Propecia ®) 5-7.5 mg/día como antiandrógeno y testolactona (Teslac ®) en dosis de 40 mg/kg/día, como inhibidor de la aromatasa para disminuir la acción estrogénica. Experimentalmente se están utilizando en los casos de HAC-clásica los antagonistas de CRH, la adrenalectomía y la terapia génica13.
Infertilidad
En los casos de infertilidad cuando las pacientes sean refractarias a la hidrocortisona o dexametasona para la inducción de la ovulación debido a que los andrógenos cuando actúan por largo tiempo producen una alteración del eje hipotálamo-hipófisis-ovario, es necesario agregar a muchas de las pacientes, además de los corticoides, citrato de clomifeno para la inducción de la ovulación. Durante el embarazo se puede mantener la hidrocortisona en dosis de 20 a 30 mg/día. Sin embargo, esto es controvertido en la HAC-NC. Existen trabajos donde se trata y donde no se trata a las pacientes durante el embarazo. Algunos investigadores recomiendan tratar previamente al embarazo y suspender el tratamiento durante la gestación.
Feldman et al.14, en 53 pacientes con diagnósticode HAC-NC, estudiaron 30 pacientes, aquienes dividieron en dos grupos, las que se embarazaron y no se embarazaron, y determinaron las diferentes concentraciones de testosterona y androstendiona; pudieron apreciar cómo todos los valores eran mayores que los niveles normales, indiferentemente del grupo de estudio (Figura 8). Cuando evaluaron las pacientes de acuerdo a la concentración 17-hidroxiprogesterona, todas ellas estaban en niveles por encima de 5 nmol/L, la mayor parte por encima de 10 nmol/L y al hacerles la prueba de estímulo con ACTH alcanzaron una media arriba de 100 nmol/L (Figura 9).
En estas mismas 30 pacientes con diagnóstico de HAC-NC se evaluó la historia obstétrica y se pudo apreciar cómo 10 de las mujeres se embarazaron antes de ser estudiadas y tratadas, a las cuales se les confirmó un 30% de antecedentes de abortos, a diferencia de las 20 mujeres restantes que se embarazaron una vez se les diagnosticó y trató el trastorno endocrino, lográndose embara zos a término y sin ningún aborto. Es posible que la mayor frecuencia de abortos en este grupo de pacientes no tratadas sea la consecuencia de una mala ovulación o placentación (Tabla 4).
Figura 8. Concentraciones de andrógenos en pacientes con diagnóstico de hiperplasia adrenal congénita no clásica.
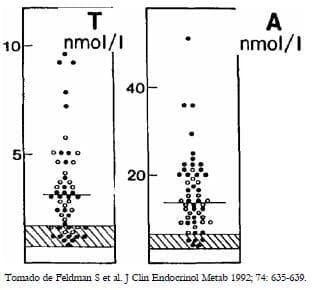
Figura 9. Niveles de 17-hidroxiprogesterona basal y cuando se hace la prueba de estímulo con ACTH en pacientes con hiperplasia adrenal no clásica.
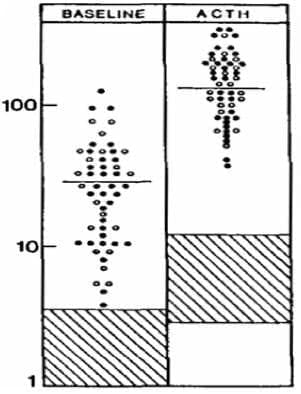
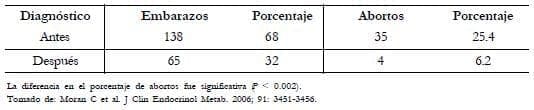
En este mismo orden de ideas Morán et al.15 estudiaron 203 embarazos en 101 mujeres con HAC y apreciaron el mismo resultado. En 138 embarazos que ocurrieron antes del diagnósticohubo un 25.4% de abortos, cifra más alta que el 6.2% de abortos que hubo en los 65 embarazos después del diagnóstico y tratamiento, con una diferencia que es estadísticamente significativa, cuatro veces menos que las pacientes no tratadas. Cabe hacer notar que en este trabajo no se administraron glucocorticoides a todas las pacientes durante el embarazo. Esto sugiere que el aborto puede ser causado por alteraciones en la ovulación o en la implantación ovular (Tabla 5).
Diagnosis prenatal y tratamiento
El diagnóstico prenatal y el tratamiento de la HAC se han efectuado en los últimos años en familias que tienen varios miembros afectados por esta entidad. En estos casos es muy importante el diagnóstico endocrino y genético del padre. El tratamiento preventivo durante la gestación se hace a base de dexametasona debido a que atraviesa la barrera placentaria y llega a la circulación fetal. Se administra a la dosis de 20 ug/kg/día, dividida en tres dosis; idealmente antes de la semana 7 de gestación, debido a que la formación del seno urogenital se inicia alrededor de la novena semana de gestación. En ocasiones el tratamiento se inicia desde el momento en que se hace el diagnóstico con miras a prevenir la virilización en mujeres afectadas con el problema. Se debe realizar el estudio del DNA fetal para lo cual se requiere muestras de vellosidades coriales tomadas aproximadamente a la novena semana de gestación o el estudio del líquido amniótico alrededor de la semana 16 a 20. Si se determina que es un feto masculino o femenino no afectado se suspende el tratamiento, de otra forma se continúa hasta llegar a término. Con las dosis recomendadas se disminuyen las complicaciones maternas como edema, estrías, ganancia de peso o abortos espontáneos. Este sería el primer desorden metabólico que es posible tratarlo en la vida intrauterina y no requiere que se le practique al recién nacido cirugía correctiva al nacimiento16.
Tabla 4. Resultados de la fertilidad en mujeres con diagnóstico de HAC-NC debido a deficiencia de 21 -hidroxilasa.
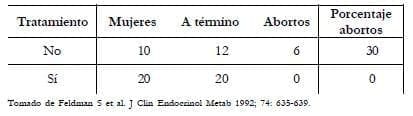
Tabla 5. Resultados gestacionales en 203 embarazos de 101 mujeres, antes o después del diagnóstico
y tratamiento de HAC-NC por deficiencia 21-hidroxilasa.
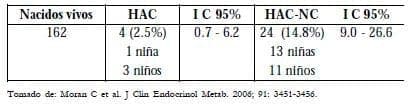
En la misma investigación de Morán et al.15 se describen las características hormonales y genéticas en algunos de los 162 recién nacidos que se pudieron estudiar; se encontró que 134 (82.7%) nacieron normales, 24 (14,8%) tuvieron el diagnóstico de HAC-NC y cuatro (2,5%) diagnóstico de HAC clásica (Tabla 6).
Complicaciones
Estas pacientes con HAC-NC pueden sufrir problemas recurrentes, enfermedades crónicas y en ocasiones de presentar mucho estrés, enfermedades severas. Tienen muy baja respuesta al estrés quirúrgico y mayor riesgo de infección, por lo que requieren que se les aumente la dosis de esteroides de 3 a 20 veces de la comúnmente utilizada. En los casos de enfermedades moderadas o leves no se requiere incrementar la dosis17.
Las manifestaciones clínicas de la HAC-NC tales como acné, hirsutismo, anovulación y obe obesidad pueden ocultar complicaciones frecuentes y futuras de la pacientes que padecen esta entidad como la resistencia a la insulina con todas sus complicaciones inherentes tales como adiposidad visceral, hiperandrogenismo, alteración de la curva de tolerancia a la glucosa, hiperleptinemia y finalmente ECV, hipertensión arterial y diabetes mellitus; sin embargo no hay aún estudios en la literatura médica que confirmen tales hipótesis, con excepción de Saygili et al.18 en 18 mujeres con diagnóstico de HAC-NC, comparadas con un grupo control de 26 mujeres sanas, donde apreciaron hiperinsulinemia y resistencia a la insulina asociada a hiperandrogenismo y niveles de leptina normales que no difieren del grupo control. No hay informes del comportamiento de esta entidad en el climaterio. Solo hay algunos casos reportados de presentación después de los 49 años7. Falta más investigación al respecto.
Es necesario que el médico tenga una visión universal a cerca del diagnóstico y manejo de todas aquellas personas que consultan por diferentes manifestaciones de hiperandrogenismo para que sean estudiadas exhaustivamente, establecer programas de prevención para futuras complicaciones, como también preparar a la paciente para su futuro obstétrico, antes de instaurar tratamientos empíricos o sintomáticos que en nada la benefician.
Tabla 6. Resultados de nacidos vivos de mujeres con HACNC por deficiencia 21-hidroxilasa.
El manejo de esta patología requiere de un equipo interdisciplinario de expertos en este grupo de pacientes de acuerdo al grado de compromiso tal como médicos generales, internistas, endocrinólogos, ginecólogos, especialistas en fertilidad, dietistas, terapistas sexuales, que les brinden apoyo psicológico, orientación genética, y un permanente control médico con el fin de evaluar los antecedentes y alteraciones endocrinas, resolver sus problemas androgénicos, planear su futuro reproductivo y evitar complicaciones posteriores.
Referencias
1. New MI. Nonclassical 21-hydroxylase deficiency. J Clin Endocrinol Metab 2006; 91: 4205-4214.
2. Speiser PW, White PC. Congenital Adrenal Hyperplasia. N Engl J Med 2003; 349: 776-788.
3. Jaimes H. Comunicación personal.
4. Morán C, Tapia MC, Hernández E, Vázquez G, García-Hernández E, Bermúdez JA. Etiological review of hirsutism in 250 patients. Arch Med Res 1994; 25: 311-314.
5. Azziz R, Sanchez LA, Knochenhauer ES, Moran C, Lazenby J, Stephens KC, Taylor K, Boots LR. Androgen excess in women: experience with over 1000 consecutive patients. J Clin Endocrinol Metab 2004; 89: 453-462.
6. Carmina E, Rosato F, Janni A, Rizzo M, Longo RA. Relative Prevalence of Different Androgen Excess Disorders in 950 Women Referred because of Clinical Hyperandrogenism. J Clin Endocrinol Metab 2006; 91: 2-6.
7. Moran C, Azziz R, Carmina E, Dewailly D, Fruzzetti F, Ibañez L, Knochenhauer ES, Marcondes JA, Mendonca BB, Pignatelli D, Pugeat M, Rohmer V, Speiser PW, Witchel SF. 21–Hydroxylase-deficient nonclassic adrenal hyperplasia is a progressive disorder: a multicenter study. Am J Obstet Gynecol 2000; 183:1468-1474.
8. Forest MG. Recent advances in the diagnosis and management of congenital adrenal hyperplasia due to 21-hydroxylase deficiency. Human Reprod Update 2004; 10: 469-485.
9. Moran C, Knochenhauer ES, Azziz R. Nonclassic adrenal hyperplasia in hyperandrogenism: a reappraisal. J Endocrinol Invest 1998; 21: 707-720.
10. Charmandari E, Brook CGD, Hindmarsh PC. Classic congenital adrenal hyperplasia and puberty. Europ Endocrinol 2004; 151 suppl 3: U77-82.
11. Azziz R, Hincapie LA, Knochenhauer ES, Dewailly D, Fox L, Boots LR. Screening for 21-hydroxylase-deficient nonclassic adrenal hyperplasia among hyperandrogenic women: a prospective study. Fertil Steril 1999; 72: 915-925.
12. Kruse B, Riepe FG, Krone N, Bosinski HAG, Kloehn S, Partsch CJ, Sippell WG, Monig H.
Congenital adrenal hyperplasia. How to improve the transition from adolescence to adult life. Exp Clin Endocrinol Diabetes 2004; 112: 343-355.
13. Merke DP. Future directions in the study and management of congenital adrenal hiperplasia due to 21-hydroxylase deficiency. Ann Int Med 2002; 136: 320-334.
14. Feldman S, Billaud L, Thalabard JC, Raux- Demay MC, Mowszowicz I, Kuttenn F, Mauvais-Jarvis P. Fertility in women with late-onset adrenal hyperplasia due to 21- hydroxylase deficiency. J Clin Endocrinol Metab 1992; 74: 635-639.
15. Moran C, Azziz R, Weintrob N, Witchel SF, Rohmer V, Dewailly D, Marcondes JA, Pugeat M, Speiser PW, Pignatelli D, Mendonca BB, Bachega TA, Escobar-Morreale HF, Carmina E, Fruzzetti F, Kelestimur F. Reproductive outcome of women with 21-hydroxylasedeficient nonclassic adrenal hyperplasia. J Clin Endocrinol Metab 2006; 91: 3451-3456.
16. New MI. An update of congenital adrenal hyperplasia. Ann NY Acad Sci 2004; 1038: 14-43.
17. Deaton MA, Glorioso JE, McLean DB. Congenital adrenal hyperplasia: not really a zebra. Am Fam Physician 1999; 59: 1190-1196.
18. Saygili F, Oge A, Yilmaz C. Hyperinsulinemia and insulin insensitivity in women with nonclassical congenital adrenal hyperplasia due to 21- hydroxylase deficiency: the relationship between serum leptin levels and chronic hyperinsulinemia. Horm Res 2005; 63: 270-274.
