Tratamiento de la Enfermedad de Graves Basedow: Mixedema Pretibial
Mixedema pretibial:
El mixedema localizado, o dermopatía tiroidea (DT), es una manifestación infrecuente de la EGB, su característica clínica principal es el engrosamiento localizado de la piel, localizado especialmente en el área pretibial –de ahí que sea más conocido como mixedema pretibial–. La característica histológica principal es la acumulación de GAG en la dermis reticular, con una exagerada concentración de ácido hialurónico, lo cual ocurre como consecuencia de la estimulación de fibroblastos, aunque el motivo de su estimulación y su origen autoinmune no es totalmente entendido, en especial el por qué afecta casi predominantemente el área pretibial, quizás por la estasis venosa y la mayor probabilidad de micro traumas en miembros inferiores induce un mayor depósito de mucina, o bien porque los fibroblastos de la economía corporal tienen diversos patrones de mecanismos de regulación, otra opción es el edema local, que puede aumentar la secreción de citoquinas que empeoran la concentración de GAG (49). Varias modalidades terapéuticas han sido empleadas, desde vendas compresivas y aplicaciones tópicas de esteroides hasta terapia sistémica con esteroides y aplicaciones intradérmicas. La DT puede tener característicamente cuatro formas de presentación:
a) La forma edematosa, indurada, sin fóvea, que se acompaña con cambios en la coloración de la piel.
b) La forma de presentación en “placas”.
c) La forma nodular.
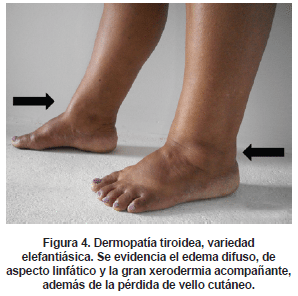
d) La forma elefantiásica.
El tratamiento de la DT es sintomático; en general, la forma edematosa y en placas puede serleve y no molesta para el paciente, la mayor partede las veces no requiere tratamiento, pero cuando se decide manejo específico, el uso de esteroides tópicos es suficiente (50,51). Las formas nodular y elefantiásica responden al manejo con vendas compresivas nocturnas (en sitios de afección en el área del tobillo o rodilla, las vendas deportivas, con una presión de compresión de 20-40 mm Hg pueden ser útiles (ver figura 4); en otras áreas de presentación, el uso de vendas de compresión media ayudan al manejo) y los esteroides tópicos (por ejemplo, acetato de triamcinolona al 0.05-0,1% en crema (52,53).
El acetónido de fluocinolona y el propionato de clobetasol también se han utilizado en algunos protocolos) con una frecuencia de aplicación de tres veces al día, acompañado de un vendaje suave con papel plástico en el área afectada, en protocolos de seguimiento entre 4-8 semanas tienen buena respuesta, con mejoría notoria en los hallazgos cutáneos de la DT (en casos selectos, la terapia con dicho protocolo puede mantenerse durante otras semanas, incluso meses, teniendo en cuenta que, al prolongar la terapia se corre el riesgo de presentar telangiectasias, equimosis y atrofia cutánea). El uso de esteroides intralesión puede causar degeneración nodular de la piel debido a la atrofia del tejido graso cuando se utilizan agujas estándar, aunque es probable que el uso de agujas de menor calibre (como las utilizadas en “mesoterapia”) no origine los resultados desfavorables descritos con las agujas normales; en general, el uso de esteroides intra-lesión y los sistémicos van perdiendo más adeptos cada día, tanto por los resultados desfavorables, como por el impacto local y sistémico de los mismos; el uso de terapias inmunomoduladoras como octreótide,azatioprina y ciclosporina, entre otros, no tienen aún una evidencia real que apoye su utilización. La cirugía para DT es poco utilizada, de hecho el trauma quirúrgico predispone a la recurrencia de la misma, por lo que sólo para casos con presentaciones estéticamente “inaceptables” podría estar indicada, junto al uso de terapia tópica con esteroides (54,55).
Como decíamos, los temas de fisiopatología y diagnóstico han sido materia de otro artículo (56).
REFERENCIAS
1. Cooper DS. Antithyroid Drugs. N Engl J Med. 2005; 352:905-917.
2. Nygaard B. Hyperthyroidism (primary). ClinEvid (Online). 2010 Jul 19; 2010. pii: 0611.
3. Abraham P, Acharya S. Current and emerging treatment options for Graves’ Hyperthyroidism. Therap Clin Risk Manag. 2010; 6:29-40.
4. Bartalena L, Tanda ML, Bogazzi F, Piantanida E, Lai A, Martino E. An update on the pharmacological management of hyperthyroidism due to Graves’ disease. Expert Opin Pharmacother. 2005; 6:851-861.
5. Abraham P, Avenell A, McGeoch SC, Clark LF, Bevan JS. Antithyroid drug regimen for treating Graves’ hyperthyroidism. Cochrane Database of Systematic Reviews 2010, Issue 1. Art. No.: CD003420. DOI: 10.1002/14651858.CD003420.pub4.
6. Iagaru A, McDougall IR. Treatment of Thyrotoxicosis. J Nucl Med. 2007; 48:379-389.
7. Andre`s E, Maloisel F, Zimmer J. The role of haematopoietic growth factors granulocyte colony-stimulating factor and granulocyte-macrophage colony-stimulating factor in the management of drug-induced agranulocytosis. Brit J Haematol. 2010; 150:3-8.
8. Watanabe N,Narimatsu H, Noh JY, Yamaguchi T, Kobayashi K, Kami M, Kunii Y,Mukasa K, Ito K, Ito K. Antithyroid Drug-Induced Hematopoietic Damage: A Retrospective Cohort Study of Agranulocytosis and Pancytopenia Involving 50,385 Patients with Graves’ Disease. J Clin Endocrinol Metab. 2012; 97:E49-E53.
9. Sun MT, Tsai CH, Shih KC. Antithyroid drug-induced agranulocytosis. J Chin Med Assoc. 2009; 72:438-441.
10. Nwatsock JF, Taieb D, Tessonnier L, Mancini J, Dong- A-Zok F, Mundler O. Radioiodine thyroid ablation in Grave’s Hyperthyroidism: Merits and pitfalls. World J Nucl Med. 2012; 11:7-11.
11. Ross DS. Radioiodine Therapy for Hyperthyroidism. N Engl J Med 2011; 364:542-550.
12. Jarløv AE, Hegedüs L, Kristensen LO, Nygaard B, Hansen JM. Is calculation of the dose in radioiodine therapy of hyperthyroidism worthwhile? Clin Endocrinol (Oxf). 1995; 43:325-329.
13. Van Isselt JW, de Klerk JMH, Lips CJM. Radioiodine treatment of hyperthyroidism: fixed or calculated doses; intelligent design or science? Eur J Nucl Med Mol Imaging. 2007; 34:1883-1884.
14. Howarth D, Epstein M, Lan L, Tan P, Booker J. Determination of the optimal minimum radioiodine dose in patients with Graves’ disease: a clinical outcome study. Eur J Nucl Med 2001; 28:1489-1495.
15. Grosso M, Traino A, Boni G, Banti E, Della Porta M, Manca G, et al. Comparison of different thyroid committed doses in radioiodine therapy for Graves’ hyperthyroidism. Cancer Biother Radiopharm. 2005; 20:218-223.
16. Oszukowska L, Knapska-Kucharska M, Lewiski A. Effects of drugs on the efficacy of radioiodine (131I) therapy in hyperthyroid patients. Arch Med Sci. 2010; 6(1):4-10.
17. deRooij A, Vandenbroucke JP, Smit JWA, Stokkel MPM, Dekkers OM. Clinical outcomes after estimated versus calculated activity of radioiodine for the treatment of hyperthyroidism: systematic review and meta-analysis. European Journal of Endocrinology. 2009; 161:771-777.
18. Bonnema SJ, Hegedüs L. Radioiodine therapy in benign thyroid diseases: effects, side effects, and factors affecting therapeutic outcome. Endocr Rev. 2012; 33(6):920-980.
19. Metso S, Auvinen A, Huhtala H, Salmi J, Oksala H, Jaatinen P. Increased Cancer Incidence After Radioiodine Treatment for Hyperthyroidism.CANCER. 2007;109(10):1972-1979.
20. Angusti T, Codegone A, Pellerito R, Favero A. Thyroid cancer prevalence after radioiodine treatment of hyperthyroidism. J Nucl Med.2000; 41:1006-1009.
21. Thyroid Function after Subtotal Thyroidectomy in Patients with Graves’ Hyperthyroidism. E. J. Limonard EJ, Bisschop PH, Fliers E, Nieveen van Dijkum EJ. Scient World J. Volume 2012, Article ID 548796, doi:10.1100/2012/548796.
22. Palit TK, Miller CC 3rd, Miltenburg DM. The efficacy of thyroidectomy for Graves’ disease: A meta-analysis. J Surg Res. 2000; 90:161-165.
23. Kaplan EL, Angelos P. Surgery of the Thyroid Gland. Thyroid Disease Manager. Available at: www.thyroidmanager. org/Chapter21/21-frame.htm.
24. Stalberg P, Svensson A, Hessman O, Akerstrom GA, Hellman P, “Surgical treatment of Graves’ disease: evidence based approach,” World J Surg.2008;32(7):1269-1277.
25. Sugino K, Ito K, Nagahama M, Kitagawa W, ShibuyaH, Ito K. “Surgical management of Graves’ disease— 10-year prospective trial at a single institution,” Endocrine Journal. 2008; 55(1):161-167.
26. Lal G, Ituarte P, Kebebew E, Siperstein A, Duh QY, Clark OH, “Should total thyroidectomy become the preferred procedure for surgical management of Graves’ Disease?” Thyroid.2005; 15(6):569-574.
27. Bahn RS, Burch HB, Cooper DS, Garber JR, Greenlee MC, Klein I, et al. “Hyperthyroidism and other causes of thyrotoxicosis: management guidelines of the American Thyroid Association and American Association of Clinical Endocrinologists”. Thyroid.2011; 21(6):593-646.
28. Genovese BM, Noureldine SI, Gleeson EM, TufanoRP, Kandil E. What is the best definitive treatment for Graves’ disease? A systematic review of the existing literature. Ann Surg Oncol. 2012 DOI 10.1245/ s10434-012-2606-x.
29. Marx H, Amin P, Lazarus JH. PREGNANCY PLUS. Hyperthyroidism and pregnancy. Brit Med J. 2008; 336: 663-667.
30. Laurberg P, Bournaud C, Karmisholt J, Orgiazzi J. Management of Graves’ hyperthyroidism in pregnancy: focus on both maternal and foetal thyroid function, and caution against surgical thyroidectomy in pregnancy.
Europ J Endocrinol. 2009;160:1-8.
31. Abalovich M, Amino N, Barbour LA, Cobin RH, DeGroot LJ, Glinoer D, et al. Management of thyroid dysfunction during pregnancy and postpartum: an Endocrine Society clinical practice guideline. J Clin Endocrinol Metab.2007; 92(8) Suppl: S1-47.
32. Chan GW, Mandel SJ. Therapy insight: management of Graves’ disease during pregnancy. Nat Clin Pract Endocrinol Metab.2007; 3:470-478.
33. Luton D, Le Gac I, Vuillard E, Castanet M, Guibourdenche J, Noel M, et al. Management of Graves’ Disease during Pregnancy: The Key Role of Fetal Thyroid Gland Monitoring. J Clin Endocrinol Metab.2005; 90:6093-6098.
34. Bahn RS. Graves’ ophthalmopathy. New Engl J Med.2010; 362:726-738.
35. Soeters MR, van Zeijl CJJ, BoelenA, Kloos R, Saeed P, Vriesendorp TM, Mourits P. Optimal management of Graves’s orbitopathy: a multidisciplinary approach. Netherl J Med. 2011; 69(7/8):302-308.
36. Regensburg NI, Wiersinga WM, Berendschot TT, Potgieser P, Mourits MP. Do subtypes of Graves’ orbitopathy exist? Ophthalmol. 2011; 118(1):191-196.
37. Khalilzadeh O, Noshad S, Rashidi A, Amirzargar A. Graves’ ophthalmopathy: a review of immunogenetics. Curr Genomics. 2011; 12(8):564-575.
38. Maheshwari R, Weis E. Thyroid associated orbitopathy. Indian J Ophthalmol. 2012; 60(2):87-93.
39. Bartalena L, Pinchera A, Marcocci C. Management of Graves’ ophthalmopathy: Reality and perspectives. Endocr Rev. 2000; 21:168-199.
40. Bartalena L. Prevention of Graves’ ophthalmopathy. Best Pract Res Clin Endocrinol Metab. 2012; 26(3):371-379.
41. Hegedüs L, Bonnema SJ, Smith TJ, Brix TH. Treating the thyroid in the presence of Graves’ ophthalmopathy. Best Pract Res Clin Endocrinol Metab. 2012 26(3):313-324.
42. Marcocci C, Marinò M. Treatment of mild, moderateto- severe and very severe Graves’ orbitopathy. Best Pract Res Clin Endocrinol Metab. 2012; 26(3):325-337.
43. Müller-Forell W, Kahaly GJ. Neuroimaging of Graves’ orbitopathy. Best Pract Res Clin Endocrinol Metab. 2012; 26(3):259-271.
44. Kirsch E, Hammer B, von Arx G. Graves’ orbitopathy: current imaging procedures.Swiss Med Wkly. 2009; 139(43/44):618-623.
45. Yang M, PerrosP. Management plan and delivery of care in Graves’ ophthalmopathy patients. Best Pract Res Clin Endocrinol Metab. 2012; 26(3):303-311.
46. Dolman PJ. Evaluating Graves’ orbitopathy. Best Pract Res Clin Endocrinol Metab. 2012 Jun; 26(3):229-248.
47. Rajendram R, Bunce C, Lee RW, Morley AM. Orbital radiotherapy for adult thyroid eye disease. Cochrane Database Syst Rev. 2012 Jul 11; 7:CD007114. doi: 10.1002/14651858.CD007114.pub2.
48. Sabih DE, Inayatullah M. Managing thyroid dysfunction in selected special situations. Thyroid Res. 2013; 6:2 doi: 10.1186/1756-6614-6-2.
49. Li H, Want T. The autoimmunity in Graves’disease. Front Biosci.2013; 1(18):782-787.
50. Fatourechi V, Pajouhi M, Fransway AF. Dermopathy of Graves disease (pretibial myxedema). Review of 150 cases. Medicine (Baltimore) 1994; 73:1-7.
51. Fatourechi V. Thyroid dermopathy and acropachy. Best Pract Res Clin Endocrinol Metab. 2012; 26(4):553-565.
52. Fatourechi V. options. Am J Clin Dermatol. 2005; 6(5):295-309.
53. Reddy SV, Gupta SK, Jain M. Dermopathy of Graves’ disease: Clinico-pathological correlation. Indian Med J 2012; 16(3):460-462.
54. Vannucchi G, Campi I, Covelli D, Forzenigo L, Beck- Peccoz P, Salvi M. Treatment of pretibial myxedema with dexamethasone injected subcutaneously by mesotherapy needles. Thyroid. 2013 Feb 11. [Epubahead of print].
55. Schwartz KM, Fatourechi V, Ahmed DD, Pond GR. Dermopathy of Graves’ disease (Pretibial myxedema): Long-term outcome. J Clin Endocrinol Metab. 2002; 87:438-446.
56. Vargas-Uricoechea H, Sierra-Torres CH, Meza-Cabrera I: Enfermedad de Graves Basedow, Fisiopatología y Diagnóstico. Medicina 2013; 35(1): 41-66 .
Fecha de recibido: Febrero 20 de 2013
Fecha de aprobado: Marzo 4 de 2013
Dirección para correspondencia:
Hernando Vargas U.
hernandovargasu10@yahoo.com
CLIC AQUÍ Y DÉJANOS TU COMENTARIO