La Disfunción Tiroidea es frecuente en la mujer
Ginecología Endocrina
*Arturo Zárate T., Lourdes Basurto; Unidad de Investigación Médica en
Enfermedades Endocrinas, Hospital de Especialidades, Centro Médico
Nacional, Instituto Mexicano del Seguro Social, México DF. México
Resumen
Los trastornos tiroideos tienen una prevalencia elevada en la mujer y esta preponderancia se ha relacionado con mayor susceptibilidad a alteraciones de la autoinmunidad. Los trastornos tiroideos presentan como características su aparición insidiosa y manifestaciones proteiformes. Por ello, se recomienda sospechar patología tiroidea en caso de depresión posparto, alteraciones menstruales, síndrome de amenorrea con galactorrea, pubertad precoz o retardada, esterilidad inexplicable o aborto de repetición. La dificultad en el diagnóstico clínico es compensada por la accesibilidad y relativa facilidad del diagnóstico bioquímico mediante las pruebas de función tiroidea, principalmente la medición de TSH y FT4, por lo que es útil considerar a estas pruebas en el estudio de los trastornos ginecológicos.
Un diagnóstico precoz y oportuno resolverá en las mejores condiciones los trastornos ginecológicos originados por el mal funcionamiento de la glándula tiroides.
Palabras clave: Hipotiroidismo, hipertiroidismo, tiroides, autoinmunidad.
Summary
The prevalence of thyroid dysfunctions is high in women, this female preponderance has been related with a bigger susceptibility to autoimmune abnormalities. Clinical features of thyroid disease have poor specificity and insidious onset. It is recommended to suspect thyroid pathology in the event of postpartum depression, menstrual abnormalities, amenorrhea, galactorrhea, precocious or delayed sexual development, inexplicable sterility or habitual abortion. The difficulty in the clinical diagnosis is compensated by the accessibility and relative easiness of the biological diagnosis by means of the of thyroid function tests, mainly the measurements of TSH and FT4 levels; thus, gynecological evaluations should be completed by obtaining thyroid function tests. An opportune diagnosis of thyroid illness will solve under the best conditions the gynecological dysfunctions.
Key words: hypothyroidism, hyperthyroidism, thyroid disease, autoimmunity.
Se ignora por qué los trastornos tiroideos son más frecuentes en las mujeres que en los hombres, aunque se ha supuesto que es debido a la mayor susceptibilidad para desarrollar procesos de autoinmunidad y se sabe que estos tienen cierta preferencia en la glándula tiroides1. Otra observación es, que en etapas particulares en las que ocurren cambios hormonales como la pubertad, el embarazo, el puerperio y la menopausia, se presentan modificaciones fisiológicas de la función tiroidea; además el sistema inmunológico se modifica.
Desde hace mucho tiempo se sabe que las anormalidades en la función tiroidea se acompañan frecuentemente de alteraciones del ciclo menstrual y de esterilidad, por lo cual era tradicional utilizar de manera empírica terapéuticas tiroideas. El avance en los métodos diagnósticos y la disponibilidad de pruebas bioquímicas más precisas así como muy sensibles ha permitido un manejo más apropiado de los trastornos tiroideos en la mujer.
Fisiología tiroidea
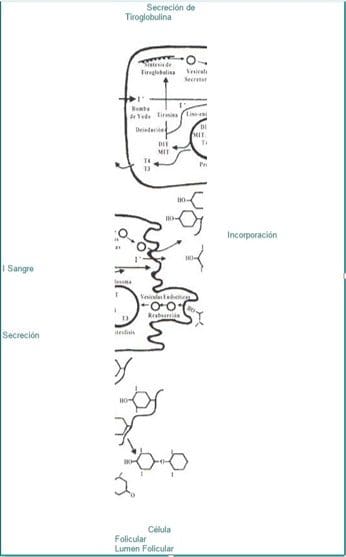
Para la síntesis de las hormonas tiroideas es necesario un aporte suficiente de yodo en la dieta, el que se absorbe en el intestino delgado y alcanza rápidamente la tiroides bajo el efecto de la tirotropina (TSH). Dentro de la glándula tiroides; de inmediato se oxida el yoduro para convertirse en yodo elemental y así se une a la tirosina. Las moléculas de monoiodotirosina y diyodotirosina se combinan para formar tiroxina (T4) y triyodotironina (T3), las cuales quedan almacenadas dentro de una molécula de tiroglobulina en el interior del folículo tiroideo (Fig.1).
Fig. 1. La tiroglobulina es la precursora de las hormonas tiroideas, su yodación se efectúa en el
lumen del folículo tiroideo; los residuos de tirosina yodados forman la monoiodotirosina (MIT) y la
diyodotirosina (DIT); una DIT se acopla con otra DIT para formar la tiroxina y una MIT con una DIT
para formar triyodotironina. Al reincorporarse la tiroglobulina al interior de la célula folicular,
sufre proteólisis, permitiendo la liberación de las hormonas tiroideas a la circulación.
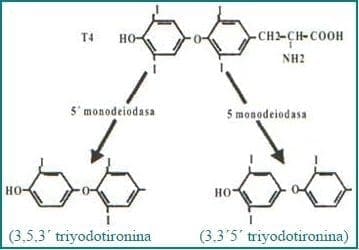
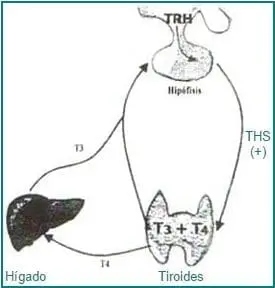
Bajo el efecto de la TSH se produce una proteólisis y al descomponerse la tiroglobulina las hormonas tiroideas salen a la circulación. La remoción de un átomo de yodo del anillo fenólico de la T4 da origen a T3, mientras que la remoción del yodo del anillo no fenólico origina la T3 reversa (rT3) (Fig. 2). Principalmente en el hígado y el riñón, una tercera parte de T4 se convierte en T3 y aproximadamente el 40% se convierte en rT3 la que es inactiva biológicamente; por lo tanto, cerca del 80% de T3 circulante proviene de la conversión periférica de T4, y por ser la T3 cinco veces más activa que la T4, se puede decir que la función de ésta es a través de T3. La T4 se puede considerar como una prehormona de T3 y la gran actividad de esta última, es debida a la enorme afinidad por el receptor nuclear. Cerca del 70% de las hormonas tiroideas circulantes se transportan unidas a la globulina transportadora de tiroxina (TBG) y el restante 30% se une a prealbúmina y a la albúmina; la T4 tiene mayor afinidad por la TBG y así la T3 puede movilizarse más fácilmente. Los estrógenos incrementan la producción de TBG en el hígado y por ello, cambios en la concentración de estrógenos modifican la cantidad de hormonas tiroideas circulantes. En situaciones que cursan con una tasa metabólica reducida, se presenta una reducción de T3 con un incremento simultáneo de la rT3 como un mecanismo para conservar energía. A su vez la síntesis y secreción de TSH está regulada por el hipotálamo y la neurohormona que lleva su nombre del inglés (TRH) por “thyroid releasing hormone”, tripéptido que estimula la producción de TSH; por otra parte, la somatostatina y la dopamina, también de origen hipotalámico, ejercen el efecto contrario. La T4 se convierte en T3 dentro de la adenohipófisis y de esta manera inhibe adicionalmente la síntesis y secreción de TSH (Fig.3).
Fig. 2. La conversión periférica de la tiroxina (T4) se realiza por acción de las monodeiodasas, por la pérdida del Yodo en posición 5′ se origina la triyodotironina (T3) y en la posición 5 a la T3 reversa (rT3).
Los estrógenos tienen la capacidad de aumentar la síntesis de receptores de TRH en la hipófisis y de esta manera pueden incrementar la secreción de TSH como ocurre durante el embarazo y la terapia estrogénica. Durante la menopausia y senescencia disminuyen los receptores de TRH, coincidiendo con una menor conversión de T4 a T3 y como resultado se incrementa la concentración de TSH al removerse el freno que ejerce la T32-3
Pruebas de Función Tiroidea
Existen varias pruebas que permiten evaluar con gran certeza el grado de funcionamiento de la tiroides, y éstas han mejorado la oportunidad y precisión en el diagnóstico de los trastornos tiroideos, aún en condiciones que cursan con variaciones en el nivel circulante de estrógenos. La tiroxina total (TT4) mide la T4 tanto libre como unida a TBG, teniendo cierta limitación diagnóstica; por lo que se prefiere medir la T4 libre (FT4). La cuantificación del índice de T4 libre se utilizó ampliamente, pero debido a que requiere la realización de dos técnicas analíticas, de reducida precisión, se utiliza poco. Esto mismo ocurre con los ensayos de T3 total y rT3, por lo tanto, se prefieren las determinaciones de FT4 y TSH. La técnica de TSH tiene gran sensibilidad, utilizando anticuerpos monoclonales contra sus dos cadenas polipeptídicas, por lo que se ha convertido en la prueba diagnóstica estelar. La medición de TSH también permite conocer en forma indirecta el efecto de la T4 sobre la hipófisis4, por lo que cambios mínimos en la concentración de T4 se reflejan en el nivel de TSH. En suma, una concentración de TSH dentro de los límites normales permite excluir razonablemente la sospecha clínica tanto de hipo como de hipertiroidismo; por otra parte, una elevación de TSH, es sospechosa de hipotiroidismo, y éste se puede confirmar al demostrar un nivel bajo de FT4.
Hipotiroidismo
El hipotiroidismo es más frecuente en la mujer y aumenta con la edad, siendo en la mayor parte de los casos asintomático o subclínico, por lo que es conveniente realizar una determinación de TSH en toda mujer a partir de los 40 años y después repetirla cada 5 años hasta los 60, y después de esta edad en forma bianual. Anteriormente se creía que el hipotiroidismo se acompañaba de trastornos menstruales en la mitad de los casos, pero estadísticas recientes han mostrado una frecuencia aproximada del 30%. Muchas mujeres pueden presentar sólo síntomas de depresión, sensación de frío, letargia y pérdida de energía, debilidad o confusión mental. Por tal motivo en estos casos, se debe efectuar una prueba de detección con TSH. Se cree que en la mayoría de los casos, el hipotiroidismo es consecuencia de una tiroiditis de Hashimoto 6. En la edad reproductiva aparecen irregularidades menstruales e infertilidad, pero es raro que el hipotiroidismo se asocie con aborto habitual (Tabla 1).
Tabla 1. Principales manifestaciones del hipotiroidismo
La presencia de niveles elevados de colesterol total, concomitante con obesidad orienta a la búsqueda de hipotiroidismo; asimismo una elevación de TSH superior a 10 mU/L, aún coincidiendo con niveles normales de FT4, amerita que se realicen pruebas periódicas de la función tiroidea. Ante la presencia de niveles muy elevados de TSH y un cuadro clínico confuso, pero sospechoso de hipotiroidismo, se debe iniciar la administración de la medicación tiroidea, porque de lo contrario se puede desarrollar un bocio. El tratamiento del hipotiroidismo es la medicación sustitutiva y aunque se ha insistido en la ventaja de recurrir a un fármaco que sólo contenga T4, la experiencia ha mostrado que en muchos casos, tiene mayor aceptación la combinación de T4/T3.
El control del tratamiento tiroideo, se realiza con la medición anual de TSH, y esto permite hacer ajustes en cuanto a la dosis. Si ocurre un embarazo, de inmediato se incrementa la dosis tiroidea y se hacen mediciones trimestrales tanto de TSH como de FT4 para control durante la gestación. Después del parto se repiten las pruebas al mes y se reduce la dosis de la medicación tiroidea.
Hipertiroidismo
El hipertiroidismo es más frecuente en la mujer que en el hombre en una razón de 5 a 1, debido a que las enfermedades autoinmunes predominan en el sexo femenino y por existir cierta tendencia familiar por una probable herencia en la vulnerabilidad inmunológica. La variedad más frecuente de hipertiroidismo es la ocasionada por la enfermedad de Graves-Basedow que se manifiesta por tirotoxicosis, exoftalmos y bocio; el cuadro clínico característico es la pérdida de peso, taquicardia, sudoración excesiva, fatiga, disnea, temblor digital, piel fina e hipertérmica, edema pretibial y nerviosismo. En la mujer posmenopáusica, el hipertiroidismo se presenta en forma diferente y puede aparecer un cuadro subclínico en el que predomina la taquicardia y la arritmia cardiaca. (Tabla 2).
Tabla 2. Manifestaciones clínicas del hipertiroidismo
El diagnóstico de hipertiroidismo se confirma al obtener una cifra mínima de TSH asociada a una elevación de FT4; la determinación de anticuerpos antitiroideos sólo es útil para el seguimiento de algunos casos, pero no conviene de rutina. La gamagrafía tiroidea sólo es de utilidad para descartar la posibilidad de tiroiditis; en este caso el cuadro de hipertiroidismo es transitorio y la captación de yodo por la glándula está disminuida o ausente.El hipertiroidismo durante el embarazo, se puede asociar con aborto, hiperemesis, preeclampsia, retraso del desarrollo fetal, óbito y peso bajo al nacimiento7. En la enfermedad de Graves-Basedow circulan anticuerpos con acción biológica semejante a la TSH y como atraviesan la barrera placentaria originan hipertiroidismo fetal y neonatal. El hipertiroidismo tanto por un nódulo único como por el multinodular es menos frecuente, en estos casos no existen las manifestaciones autoinmunes como es el exoftalmos8.
En general el tratamiento de la enfermedad de Graves-Basedow se basa en drogas antitiroideas como el metimazol que suprime la síntesis de las hormonas tiroideas y la conversión de T4 a T3; adicionalmente posee un efecto modulador de la inmunidad. La efectividad de este tratamiento alcanza entre 50 y 70%, pero requiere suministrarlo cuando menos durante un año; en caso de recurrencia de la enfermedad es recomendable la administración de una dosis terapéutica de yodo radiactivo (I131) para producir un hipotiroidismo iatrógeno. Hay quien prefiere el yodo radiactivo como una manera inicial de tratamiento, a pesar del hipotiroidismo y la consecuente posibilidad de deterioro del exoftalmos. Existe discusión en cuanto a la utilidad de la asociación del metimazol con hormonas tiroideas para reducir el tamaño del bocio y el exoftalmos, siendo los resultados contradictorios. Hasta ahora, el exoftalmos se ha tratado con glucocorticoides y mediante cirugía oftalmológica para reducir el tejido retro-orbitario y corregir trastornos de los párpados. Durante la gestación sólo se usa el metimazol asociado o no con la medicación tiroidea. Los agentes b-bloqueadores se dan de rutina en el periodo inicial, dos a cuatro semanas, para aliviar las manifestaciones de hiperactividad del sistema adrenérgico. Los nódulos tiroideos hiperfuncionantes se tratan mediante cirugía o con la administración de yodo radiactivo9.
Nódulo Tiroideo
El nódulo tiroideo único es benigno en el 90 % de los casos; pero es necesario realizar el diagnóstico diferencial con el carcinoma que se inicia también como un nódulo único10. En la mujer existen datos clínicos que pueden indicar la malignidad, como son la aparición del nódulo en edad mayor a 60 años, la presencia de ganglios, y una tiroides de consistencia dura y fija a tejidos vecinos, así como datos compresivos que incluyen disfonía y disfagia. En la gamagrafía se observa un área sin captación del isótopo radiactivo (“nódulo frío”). Se recomienda realizar la biopsia con “aguja fina” y su análisis citológico por citólogo con experiencia. El tipo y extensión de la cirugía para el cáncer de tiroides dependen de la variedad histológica; posteriormente se administra una dosis elevada de yodo radiactivo para destruir el resto de la glándula, seguido de la medicación tiroidea con el fin de suprimir la secreción de TSH. En los casos de nódulo benigno, aún se encuentra en discusión la conveniencia de dar tratamiento supresivo con hormonas tiroideas por un tiempo prolongado. Si un año después no se ha reducido el nódulo, está indicada su extirpación quirúrgica. El bocio multinodular de grandes proporciones es quirúrgico11.
Tiroiditis Postparto
Durante el embarazo se suprimen los procesos inmunológicos maternos; por ello al término de la gestación puede aparecer de manera brusca una tiroiditis, la que puede haber estado silente durante la gestación. Se manifiesta clínicamente en el posparto con dolor en el cuello y datos de hipertiroidismo, pero más frecuentemente aparece un síndrome de depresión (conocido anteriormente como “tristeza postparto”). Se cree que la tiroiditis postparto es más frecuente de lo anticipado y por ello es conveniente realizar una determinación de TSH en las puérperas con depresión12. El diagnóstico diferencial con una tirotoxicosis de Graves-Basedow se realiza con un gammagrama de tiroides el que muestra ausencia de captación de yodo baja o nula en la tiroiditis.
Embarazo
En la gestación ocurren cambios en la función tiroidea de la madre con el fin de ajustarse a los requerimientos fetales y a la misma función tiroidea del feto, la cual hasta cierto grado es independiente. Desde las primeras semanas de gestación en la madre se incrementa la depuración renal de yodo y esto hace que se requiera de un aporte mayor porque el feto necesita ese yodo para sintetizar sus propias hormonas tiroideas. Por esta razón se supone que un aporte insuficiente de yodo a las embarazadas puede determinar la aparición de bocio materno, pero el riesgo mayor es para el feto.
En la embarazada se produce una mayor cantidad de T4 la cual pasa a la circulación fetal para darle al feto los requerimientos iniciales, mientras el feto sintetiza importantes cantidades de TSH para estimular la formación de sus propias hormonas a partir de la semana 10. Con base en estas observaciones se justifica incrementar la dosis de medicación tiroidea en toda mujer hipotiroidea que apenas inicia su embarazo. El paso de hormonas tiroideas hacia el feto es importante, ya que de esta manera se explica el por qué los fetos con ausencia de tiroides tienen un desarrollo normal incluso a nivel neurológico. Por otra parte, el hipotiroidismo del recién nacido es asintomático y sólo se puede diagnosticar de manera bioquímica con cuantificación de TSH y T4 libre; cuando se corrige precozmente se pueden evitar todos los problemas neurológicos que ocasionan retraso mental. Este trastorno mental es el único que se puede prevenir y es por ello que se ha propuesto implementar las pruebas de detección universal de hipotiroidismo en los recién nacidos; una vez confirmado el diagnóstico de hipotiroidismo neonatal se debe establecer la terapéutica correspondiente.
Bocio en la adolescente
El bocio simple que aparece en la adolescente habitualmente cursa sin alteración de la función tiroidea y el tamaño es de poca magnitud. Se piensa que el bocio se presenta por la demanda adicional de hormonas tiroideas que se requieren durante la pubertad, y en consecuencia hay una mayor secreción de TSH que finalmente determina en forma compensatoria el crecimiento de la glándula tiroides. El tratamiento consiste en administrar hormonas tiroideas, con lo cual se logra la reducción del bocio y se alivia la molestia cosmética.
Conclusión
La mujer es especialmente vulnerable a padecer trastornos tiroideos, por lo que es necesario su diagnóstico oportuno ya que frecuentemente pasan inadvertidos y se pueden confundir con otros problemas. En casos de esterilidad inexplicable, trastornos menstruales, aborto repetido, preeclampsia, taquicardia y arritmia cardiaca, exoftalmos, depresión, síndrome de amenorrea con galactorrea y pubertad precoz se debe realizar un estudio de la función tiroidea, iniciando mediciones de TSH y FT4, y de acuerdo con el resultado se procede en concordancia.
Referencias
1. Gaches F, Delaire L, Nadalon S, Loustaud-Ratti V, Vidal E. Frequency of autoimmune diseases in 218 patients with autoimmune thyroid pathologies. Rev Med Intern 1998; 19: 173-79.
2. Rallisonn ML, Dobyns BM, Meikle AW, et al. Natural history of thyroid abnormalities: prevalence, incidence, and regression of thyroid diseases in adolescents and young adults. Am J Med 1991; 91: 363-9.
3. Samuels MH. Subclinical thyroid disease in the elderly. Thyroid 1998; 8: 803-13.
4. Madjlessi A, Pariel-Madjlessi S, Belmin J. Clinical usefulness of screening for dysthyroidism with an ultrasensitive thyroid-stimulating hormone (TSH) assay in patients hospitalized in geriatric units. Press Med 1999; 28: 1743-47.
5. Kudson TM, Meuleman E. Managing menopause. Am Fam Phys 2000; 61: 1391-440.
6. Davies TF. The thyroid immunology of the postpartum period. Thyroid 1999; 9: 675-84.
7. Burrow GN, Fisher DA, Larson PR. Maternal and fetal thyroid function. N Engl J Med 1994; 331: 1072-78.
8. Weetman P. Thyroid-associated eye disease pathophysiology. Lancet 1991; 338: 25-28.
9. Kraimps JL, Bouin-Pineau MH, Marechaud R, Barbier J. Basedow’s disease and thyroid nodules. A common association. Ann Chir 1998; 52: 449-51.
10. Chao TC, Lin JD, Jeng LB, Chen MF. Thyroid cancer with concurrent hyperthyroidism. Arch Surg 1999; 134: 130-34.
11. Sandrock D, Olbricht T, Emrich D, Benker G, Reinwein D. Long-term follow-up in patients with autonomous thyroid adenoma. Acta Endocrinol (Copenh) 1993; 128: 51-55.
12. Weetman P. Autoimmune thyroiditis: predisposition and pathogenesis. Clin Endocrinol 1992; 36: 307-23.


CLIC AQUÍ Y DÉJANOS TU COMENTARIO