Fisiología del Hueso
La fisiología del hueso está determinada por el metabolismo fosfocálcico que está regulado por la actividad hormonal sistémica y por mediadores locales como prostaglandinas, leucotrienos, IGF, TGFß (factor de crecimiento transformante beta); TNF (factor de necrosis tumoral). El calcio ionizado está regulado por tres órganos: riñón, hueso e intestino.
La calcemia está determinada por los flujos de calcio existentes entre el líquido extracelular, la sangre y órganos como riñón, hueso e intestino.
Las hormonas reguladoras del metabolismo óseo son la PTH, calcitonina, vitamina D, estrógenos, hormonas tiroideas, esteroides, factores de crecimiento, osteoprotegerina y leptina, las cuales serán tratadas con más profundidad en un próximo artículo.
Paratohormona PTH
Es la hormona más importante del metabolismo fosfocálcico. Ante la disminución de la calcemia se produce aumento de la resorción ósea promoviendo la movilización de calcio. Además reduce los niveles circulantes de fosfato e incrementa su excreción en la orina.
La PTH aumenta la producción renal de 1,25 (OH)2 colecalciferol, lo cual produce un aumento en la absorción intestinal de calcio. Además controla la reabsorción de calcio en la porción distal de la nefrona.
1,25 Dihidroxivitamina D
Aumenta la absorción intestinal de calcio. Su producción es estimulada ante la hipocalcemia. A diferencia de la PTH que su regulación se realiza en minutos, la vitamina D requiere de horas a días. Su activación se inicia en la piel por acción del sol, produciendo colecalciferol el cual en el hígado es transformado a 25(OH)D3 (calcidiol). El calcidiol en riñón por acción de la 1a hidroxilasa se convierte a 1,25 (OH)2 D3 o calcitriol.
La vitamina D tiene acciones inmunomoduladoras estimulando la unidad formadora de colonias de fibroblastos lo cual lleva a la producción de células mesenquimatosas que se transformarán en osteoblastos. De igual manera, acciones pro-mineralización mediadas por prostaglandinas. Además se detectan receptores para vitamina D en la fibra muscular estriada, interviniendo en la mejoría del tono muscular lo cual a su vez contribuye a disminuir el riesgo de caída2,12.
Calcitonina
Se libera cuando la calcemia ha aumentado en un 10% con una respuesta rápida. Disminuye los niveles de calcio y fosfato en sangre. Inhibe la osteolisis y aumenta la excreción renal de calcio. Este mecanismo fisiológico es poco relevante en humanos.
Osteoprotegerina
Es una proteína inhibidora del reclutamiento y activación de los osteoclastos. Actúa uniéndose al receptor transmembránico RANK (Receptor para la activación del factor nuclear Kappa ß) localizado en la pared de los osteoclastos, impidiendo la unión a su ligando RANKL, ligando o activador del receptor para la activación del factor nuclear Kappa ß, expresado en la superficie osteoblástica.
Estrógenos
Las acciones sobre los procesos de resorción y formación ósea se basan en: inhibición del reclutamiento de los osteoclastos, mediado por la osteoprotegerina; aumento del número de osteoblastos. Producción de colágeno por parte de los osteoblastos. Aumento del RNA mensajero del TGF-ß y acciones genómicas y no genómicas.
Leptina
Es una de las últimas hormonas que ha sido incluida entre los reguladores de la fisiología ósea. Su acción se encuentra en estrecha relación con la PTH. El principal mecanismo de acción es una estimulación directa sobre la actividad osteoblástica promoviendo la síntesis de colágeno y una estimulación antiosteoclastogénica de la osteoprotegerina, promoviendo la mineralización ósea.
Unidad de remodelado óseo (URO)
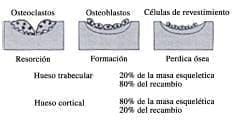
En condiciones normales el esqueleto se remodela continuamente. Un ciclo de remodelación ósea dura de tres a nueve meses y se completa cada diez años. El remodelado óseo es más activo a nivel del hueso trabecular, presentando un recambio anual del 40%, mientras que este fenómeno solo ocurre en un 10% del hueso cortical.
El equilibrio o acoplamiento entre los procesos de formación y resorción ósea asegura la preservación de la masa ósea por un proceso complejo controlado por los osteoclastos, osteoblastos y osteocitos (Figura 7).
La unidad de remodelado óseo es una estructura temporal multicelular de 1-2mm x 0.2-0.4 mm ligada al proceso de formación y resorción. Un adulto normal tiene en funcionamiento 3 a 4 millones de URO cada año y en cualquier momento hay un millón de dichas unidades en funcionamiento. El ciclo vital de la URO es superior al ciclo vital de las células participantes, lo cual indica que hay una actividad continua de incorporación celular para mantener el proceso hasta su terminación.
Proceso de remodelado óseo
Un ciclo de remodelación se inicia con la activación de un grupo de pre-osteoclastos llevada a cabo por el factor de crecimiento decolonias macrófagos (M-CSF) y citoquinas.
Figura 7. Remodelamiento óseo.
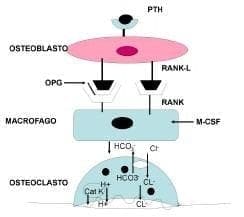
Las citoquinas estimulan la expresión en el osteoblasto y en células del estroma de la molécula RANK-L miembro de la familia de las citoquinas del Factor de Necrosis Tumoral (TNF), la cual se une al RANK ubicado en la superficie del osteoclasto y lo activa (Figura 8).
El osteoclasto una vez activado produce la solubilización de la matriz ósea, liberando cistein-aminoproteinasas y metaloproteinasas además de la catepsina K la cual rompe la triple hélice del colágeno en múltiples puntos13-15. Al activarse el osteoclasto libera iones hidrógeno y lactato produciendo un ambiente ácido. La resorción ósea la completan los osteoclastos entre 4 y 12 días. En esta fase puede interferir la osteoprotegerina producida por los osteoblastos y unirse al RANK en vez del RANK-L e impedir la activación del osteoclasto o inducir su apoptosis16. A continuación un grupo de células mononucleadas emparejan la superficie horadada. Los siguientes siete a diez días la cavidad se rellena de un material pobre en colágeno y rico en proteoglicanos, glicoproteínas y fosfatasa ácida (Figura 8).
Figura 8. Interacciones entre osteoblasto y osteoclasto. Ante estímulos como la PTH las células del estroma y los osteoblastos expresan M-CSF y al RANK-L el cual se une al RANK estimulando la osteoclastogénesis. La osteoprotegerina (OPG) bloquea los efectos del RANKL sobre el RANK de los macrófagos. El osteoclasto maduro produce diferentes proteinasas implicadas en la resorción ósea, entre las que se destaca la catepsina K (Cat K). Modificado de Teitelbaum SL. Science 2000; 289: 1504-1508.
Posteriormente los osteoblastos se desplazan al sitio de remodelación influenciados por factores hormonales y factores de crecimiento y van recubriendo la superficie de la cavidad del hueso resorbido, depositando matriz osteoide y otras proteínas (fase de acoplamiento y formación). La matriz recién sintetizada, formada en un 90% por colágeno tipo 1, es posteriormente mineralizada con cristales de hidroxiapatita bajo la influencia de la vitamina D17-18. El grado de mineralización es una propiedad importante para el hueso; cuanto mayor es el contenido mineral, mayor será la rigidez y el estrés máximo que tolerará el hueso. Sin embargo, la resistencia del hueso disminuye cuando el contenido mineral excede al 65%.
En el proceso de formación ósea en la URO el osteoblasto se podría considerar un fibroblasto más evolucionado; todos los genes de los fibroblastos son comunes con los osteoblastos, tan solo se ha identificado un factor de transcripción específico, Cbfa-1, (core binding factor a1) el cual codifica la expresión de osteocalcina6-8.
En el control de la diferenciación de los osteoblastos se ha implicado a las principales familias de factores de crecimiento, varias proteínas morfogenéticas óseas (BMPs) capaces de inducir la expresión de Cbfa-1, la cual a su vez activa los genes específicos de la osteopontina, sialoproteína ósea, colágeno tipo 1 y osteocalcina.
Estas actividades de síntesis son precedidas por la expresión de la fosfatasa alcalina como un marcador precoz de los preosteoblastos. Otros factores que estimulan la diferenciación de los osteoblastos incluyen el factor de crecimiento transformante (TGFß), factor de crecimiento derivado de las plaquetas (PDGF), factores de crecimiento insulínico (IGFs) y la familia de factores de crecimiento de fibroblastos (FGF).
CLIC AQUÍ Y DÉJANOS TU COMENTARIO