Hiperplasia Adrenal Congénita
Revisión de Tema
*Jáner Sepúlveda Agudelo
**Lucy Sanguino Abril
***Hermes Jaimes Carvajal
Resumen
La hiperplasia adrenal congénita es el desorden adrenal más común en niños y niñas; la causa más frecuente de ambigüedad sexual.
La deficiencia de la enzima 21 hidroxilasa es la causa más común de hiperplasia suprarrenal congénita, ocurre entre un 90 y 95% de los casos; su diagnóstico inicial se realiza midiendo los niveles de 17 hidroxiprogesterona; se puede realizar diagnóstico prenatal de esta patología. El tratamiento se realiza básicamente con glucocorticoides; éstos también pueden ser aplicados prenatalmente a la madre para tratamiento.
La deficiencia de 11 beta hidroxilasa produce el 5-8% de casos de hiperplasia adrenal congénita.
Los otros casos son producidos por la deficiencia de 3 beta hidroxiesteroide deshidrogenasa/delta 5-delta 4 isomerasa, 17 alfa hidroxilasa, 20 hidroxilasa, 18 hidroxiesteroide deshidrogenasa, 18 hidroxilasa y la 17,20 desmolasa.
Se realizó una revisión de los tópicos más relevantes de la hiperplasia suprarrenal congénita haciendo énfasis en la deficiencia de la 21 hidroxilasa por ser la más frecuente.
PALABRAS CLAVE: Hiperplasia adrenal congénita, hormona corticotrópica, 21 Hidroxilasa, 17 Hidroxiprogesterona, diagnóstico prenatal.
Summary
Congenital adrenal hyperplasia is the most common adrenal disorder in childhood and the most frequent cause of sexual ambiguity.
21 hydroxylase deficiency is the most common form of congenital adrenal hyperplasia, and accounts for approximately 90-95% of patients. The initial diagnosis of 21-hidroxylase deficiency is made by plasma levels 17 hydroxiprogesterone and the diagnosis can be done in pregnancy. The medical treatment is mainly glucocorticoid therapy; also treatment can be performed in pregnancy.
11 beta hydroxylase deficiency accounts for 5-8% of congenital adrenal hyperplasia.
The congenital adrenal hyperplasia is caused too by deficient activity of 3 beta-hydroxysteroids dehydrogenase /delta 5-delta, 4 isomerase, 17 alpha hydroxylase, 20 hydroxylase, 18 hydroxyesteroids dehydrogenase, 18 hydroxylase and 17,20 desmolase.
An overview of the main aspects of congenital adrenal hyperplasia is made, emphasis is done in 21 hydroxylase deficiency.
KEY WORDS: Congenital adrenal hyperplasia, adrenocorticotropic hormone, 21 hydroxylase, 17 hydroxyprogesterone, prenatal diagnosis.
Introducción
La hiperplasia adrenal congénita es una familia de desórdenes hereditarios de la esteroidogénesis adrenal, transmitido por un gen autosómico recesivo que codifica una de las enzimas esenciales para la síntesis de cortisol1-3. Es el desorden adrenal más común en niños y niñas4. El resultado de la deficiencia de estas enzimas, es la disminución en la producción de cortisol, el cual incrementa la secreción de hormona corticotrópica (ACTH) por un mecanismo de retroalimentación negativo1,3. El exceso de ACTH estimula la corteza adrenal causando hiperplasia y superproducción de precursores esteroides para cortisol por defectos enzimáticos y superproducción de otros esteroides adrenales que son sintetizados independientemente de la actividad enzimática deficiente1,3. La fisiopatología de la hiperplasia adrenal congénita (HSC) se inicia desde la vida fetal temprana y da como resultado hiperplasia adrenocortical1. Es una enfermedad que debe sospecharse e investigarse en todo niño que nazca con ambigüedad sexual.
Además de la deficiencia de cortisol, la deficiencia de enzimas esteroidogénicas activas en la corteza adrenal causa disminución o superproducción de andrógenos adrenales y mineralocorticoides dependiendo de la enzima que afecten. La alteración en la síntesis de hormonas sexuales, causa virilización, pérdida de sal o no, o desórdenes hipertensivos5. Estudios han identificado las formas clínicas leves a severas de HSC reflejadas por el grado de deficiencia enzimática en Cortisol, Aldosterona o ambas, y la secuela de exceso o deficiencia de la producción de andrógenos. La forma severa se presenta en la vida prenatal y la leve o no clásica se manifiesta después del nacimiento. Recientes avances han permitido codificar los genes de las enzimas esteroidogénicas1. Los genes para la 21 hidroxilasa son el CYP 21B (gen activo) y otro el CYP 21 A (gen inactivo). Los de la 3 beta hidroxiesteroide deshidrogenasa / delta 5 delta 4 isomerasa son el 3 beta HSD tipo I y tipo II ambos localizados en el cromosoma Ip. Para la 11 beta hidroxilasa se han encontrado dos genes el CYP 11B1 y CYEP 11B2 localizados en el cromosoma 8q22, los de la 17 alfa hidroxilasa están codificados en el cromosoma 10.
En la práctica, la evaluación de los niveles en suero de esteroides y sus metabolitos urinarios y la relación entre precursores y productos localiza el defecto enzimático1.
Fisiopatología
Las principales enzimas comprometidas como causantes de hiperplasia adrenal congénita son:
- 3 beta-hidroxiesteroide deshidrogenasa / delta 5 delta 4 isomerasa (3 beta OHeDHasa).
- 17 alfa hidroxilasa (17alfaOHasa); en la actualidad se llama citocromo P450c17*
- 21 hidroxilasa (21 OHasa); en la actualidad se llama citocromo P450c21*
- 11 beta hidroxilasa (11 betaOHasa); en la actualidad se llama citocromo P450c11*
- 20 hidroxilasa o 20,22 desmolasa, en la actualidad se llama citocromo P450SCC* (SCC significa en inglés: side chain cleavage que es desdoblamiento de una cadena lateral)
- 18 hidroxiesteroide deshidrogenasa (18 OHeDHasa).
- También pueden comprometerse la 18 hidroxilasa (18 OHasa) y la 17,20 desmolasa.
* Las enzimas denominadas citocromo P450 son llamadas así por ser oxidasas del citocromo P450 cuya característica es la de absorber luz a 450 nm cuando son reducidas con monóxido de carbono.
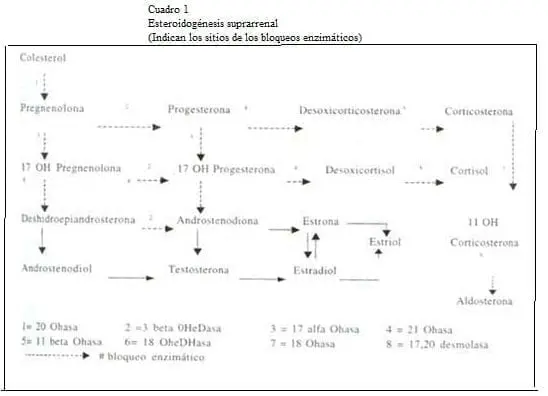
Para comprender mejor la fisiopatología de esta enfermedad debemos repasar los procesos metabólicos de la esteroidogénesis adrenal. Los esteroides son lípidos y se derivan del colesterol.
En el cuadro 1 se simplifica la vía suprarrenal y se señalan los posibles bloqueos enzimáticos que se pueden presentar.
Deficiencia de la enzima 21 hidroxilasa:
La deficiencia de la enzima 21 hidroxilasa es la causa más común de genitales ambiguos en los neonatos, la causa endocrina más frecuente de muerte neonatal y la causa más común de hiperplasia suprarrenal congénita6-7. Ocurre en un 90 -95% de los casos3, con una incidencia aproximada de 1 caso en 14.000 – 15.000 nacidos vivos en su forma clásica7-10 y 1:1000 en su forma no clásica11; este trastorno se hereda como un rasgo autosómico recesivo ligado al complejo mayor de histocompatibilidad (HLA) situado sobre el brazo corto del cromosoma 6; por lo tanto los hermanos con deficiencia de 21 hidroxilasa suelen tener tipos de HLA idénticos8. Es decir los padres de un niño afectado tienen al menos un haplotipo para el defecto dando la posibilidad de que su descendiente tenga una probabilidad de un 25% de presentar la enfermedad y un 50% de ser portador.
Una persona afectada produce un 100% de portadores si su pareja no está afectada. Si su pareja es portadora los hijos tienen una posibilidad de un 50% de presentar la enfermedad y un 50% ser portadores10.
El exceso de la estimulación de la ACTH en la deficiencia de 21 hidroxilasa, resulta en exceso de progesterona (P) y 17 hidroxiprogesterona (17 OHP) los cuales son precursores de Aldosterona y Cortisol1,11-13 porque está bloqueada la conversión de P en desoxicorticosterona (DOCA) y 17 OHP en desoxicortisol8,14.
Es clasificada en dos grandes grupos, la forma clásica y no clásica. La primera comprende dos categorías: la perdedora de sal y la virilizante simple1,7-8 . La forma no clásica se asocia con HLA B 14, DR1. La perdedora de sal se asocia con los haplotipos HLA A3, BW 47, DR7 y HLA BW60 y la virilizante simple con HLA B5.
Otra forma de clasificación es de acuerdo al grado de pérdida de sal y se divide en cuatro grupos14:
– No perdedora de sal.
– Perdedora de sal.
– Ligeramente perdedora de sal.
– Potencialmente perdedora de sal.
La forma clásica perdedora de sal es la más severa, ocupa el 75% de los casos de la forma clásica1,3,8-9 y resulta en deficiencia de Cortisol y Aldosterona, exceso en la producción de andrógenos adrenales desde la vida fetal, virilización de genitales externos en los recién nacidos de sexo femenino y alteraciones por deficiencia de Aldosterona.
La inhabilidad para retener sodio y excretar potasio de los túbulos renales por la deficiencia de Aldosterona resulta en hiponatremia, hiperkalemia, acidosis metabólica1,3 y en algunos casos hipoglicemia por deficiencia de Cortisol1.
Los síntomas y signos en los recién nacidos incluyen inapetencia, letargia, vómito, diarrea, deshidratación, hipotensión y pérdida de peso; en los no tratados colapso circulatorio y muerte13-14; como el control de líquidos y electrolitos en el feto es mantenido por la placenta, esta “crisis perdedora de sal” se desarrolla sólo después del nacimiento, usualmente durante la primera a la cuarta semana de vida1,14; la acumulación de altas concentraciones de 17 OHP la cual tiene leves propiedades natriuréticas puede exacerbar la pérdida de sal1.
La deficiencia de 21 OHasa causa hipocortisolismo fetal que estimula la producción de ACTH resultando en crecimiento adrenal y acumulación de 17 OHP y otros esteroides adrenales, los cuales en ausencia de 21 OHasa son convertidos a androstenodiona en la glándula adrenal y luego a testosterona. Esta testosterona adicional no trae consecuencias para los fetos masculinos pero significante virilización de fetos femeninos. Dependiendo de la cantidad de testosterona producida y el tiempo de exposición fetal el resultado puede ser clítoromegalia con o sin fusión posterior de los pliegues labiales a una fusión completa13-14. Al nacimiento, las niñas conservan ovarios, trompas y útero normales1,8 y los genitales externos son ambiguos o pueden ser lo suficientemente virilizadas y parecer de sexo masculino con testículos sin descender, resultando en errores de asignación de sexo13. El hecho que no se afecten los genitales internos es debido a que estos están completamente formados a la semana 10 de gestación y la corteza adrenal no es completamente funcional a esta edad gestacional15.
Los hombres afectados no presentan anormalidades genitales al nacimiento, de no ser tratados presentan virilización progresiva, crecimiento anormalmente acelerado del pene, pubarquia prematura, crecimiento corporal acelerado y fusión precoz de la epífisis, lo cual lleva finalmente a una estatura definitiva menor1,14; Los testículos en cambio generalmente permanecen pequeños y sin capacidad de desarrollarse ni ser funcionales1,14.
En las mujeres suele ser manifiesta desde el nacimiento la hiperproducción de andrógenos por la ambigüedad sexual, si no se suprimen tales hormonas, progresa la clítoromegalia (se debe sospechar clítoromegalia con un tamaño del clítoris mayor a 2 cm), se presenta pubarquia temprana y crecimiento corporal acelerado, fusión precoz de la epífisis y menor estatura. Más adelante, hipotrofia mamaria, hay apariencia masculina, amenorrea e incluso vello facial masculino, en casos exagerados calvicie temporal y cambio de la voz1, 14.
Finalmente uno de los productos secundarios de la ACTH es la hormona melanocito estimulante (MSH); si no se frena la secreción de ACTH habrá también secreción excesiva de MSH por lo cual se produce hiperpigmentación cutánea7.
La forma clásica virilizante simple ocupa el 25% de este grupo. El exceso de producción de andrógenos desde la vida fetal temprana causa virilización en genitales externos femeninos. La síntesis de Aldosterona no está significantemente afectada, hay un adecuado mantenimiento de sodio renal, pero la actividad de la renina está aumentada si no son diagnosticados. El exceso de andrógenos causa clítoromegalia o agrandamiento del pene con crecimiento acelerado, pubarquia temprana y posteriormente pubertad precoz y baja estatura final por cierre prematuro de las epífisis oseas1. Los fetos masculinos no son afectados1.
La forma tardía o no clásica resulta en bajo grado de deficiencia de Cortisol y exceso en la producción de andrógenos adrenales, secreción normal de Aldosterona, no hay pérdida de sal y los genitales externos en recién nacidos son normales. Es usualmente diagnosticada cuando los síntomas o signos de andrógenos ocurren durante la niñez o la vida adulta tales como pubarquia temprana, crecimiento corporal acelerado y clítoromegalia; durante la adolescencia o la vida adulta presenta síntomas que incluyen hirsutismo, acné, desordenes menstruales e infertilidad1, 3, 7, 11, 13, 16.
La infertilidad se presenta en el 50% de los casos17 y la complicación con ovarios poliquísticos en un 39 – 44%3, 17. El hirsutismo aislado en un 39%3.
La HSC también se ha relacionado como causa de hiperandrogenismo en la vida tardía especialmente en la sexta década de la vida y está se asociada a incidentalomas de la glándula adrenal, llamados de esta manera por su hallazgo incidental o inexplicable cuando se realizan imágenes diagnósticas, usualmente tomografía axial computarizada de la región abdominal18-20. El 83% de los pacientes con HSC de la forma virilizante simple u homocigota diagnosticada en la vida tardía está relacionada con incidentalomas adrenales; la forma heterocigota o tardía está relacionada en un 40-50%18, 20-21, los incidentalomas se aprecian entre 1-4% de las tomografías de abdomen18-19.
Hay una forma asintomática, llamada hiperplasia adrenal críptica que sólo se descubre con pruebas bioquímicas15.
Diagnóstico
Los niveles de 17 OHP cuando se estimula con ACTH están elevados, casi siempre mayor de 2 mgr/dl o 66 nmol/L, en la mayoría de pacientes y en una minoría entre 1.2 a 2 mgr/dl (49.5 y 66 nmol/L. En recién nacidos pretérminos y a término con sufrimiento fetal tienen un valor elevado persistente de 17 OHP sin tener hiperplasia suprarrenal congénita pero raramente excede a 2 mgr/dl7,13.
Allen y cols22 evaluaron la eficacia y eficiencia ajustándolo al peso de acuerdo al nivel de 17 OHP para disminuir los falsos positivos. Encontraron que en recién nacidos con peso menor de 1700 gramos el valor definitivamente anormal era 1.35 mgr/dl y en los que tenían peso mayor de 1700, el valor anormal es de 0.9 mgr/dl.
En adultos la determinación basal de 17 OHP menor de 0.2 mgr/dl excluye el diagnóstico, y mayor de 0.5 mgr/dl, lo establece. Entre 0.2 y 0.5 mgr/dl el diagnóstico es dudoso3.
La respuesta exagerada a la estimulación con ACTH es de utilidad en las pacientes con hiperplasia suprarrenal leve, cuando los niveles de 17 OHP están entre 0.2 y 0.5 mgr/dl,3,11-13 se verifican las concentraciones plasmáticas basales de 17 OHP y una hora después de la administración endovenosa de 0.25 mgr de ACTH en este caso los valores son mayores de 1.0 mgr/dl3 . También se puede realizar otra prueba midiendo los niveles basales de P y de 17 OHP, se administra 1 mg de ACTH endovenoso y 30 minutos (min) después se vuelve a tomar otra muestra para P y 17 OHP y se hace la siguiente fórmula:
(P 30 min _ P basal) + (17 OHP 30 min-17 OHP basal) / 30 min.
Si la relación es mayor de 6.5 se hace diagnóstico; si es menor de 4.5 se descarta el diagnóstico y si está entre 4.5-6.5 probablemente la mujer sea una portadora de déficit enzimático23-24.
Otras pruebas que se han utilizado para el diagnóstico son:
– Aumento del nivel del 21 desoxicortisol1,11-12.
– Aumento de la excreción urinaria de metabolitos de la 17 hidroxiprogesterona como el pregnanotriol1,11-12.
Diagnóstico Prenatal
La producción esteroidea en el feto comienza en la segunda mitad del primer trimestre. La masa suprarrenal aumenta significativamente para esta fecha y alcanza su punto máximo aproximadamente a las 15 semanas de embarazo7. Como la orina fetal contribuye al líquido amniótico desde el segundo trimestre de embarazo época en la que ya ha comenzado a funcionar la glándula suprarrenal, esto ha permitido identificar fetos con hiperplasia suprarrenal congénita; midiendo las concentraciones de la 17 OHP en líquido amniótico después de la semana 14, la cual está elevada solamente en la variante perdedora de sal13,25. El valor normal está entre 18-269 ngr/dl, y es diagnóstico cuando es mayor de 300 ngr/dl.25; también puede medirse el valor de androstenodiona, cuyo valor normal está entre 10-83 ngr/dl; y es diagnóstico cuando es mayor de 134 ngr/dl25.
También se puede hacer diagnóstico prenatal con el análisis de DNA del locus HLA DR o el gen CYP21, por biopsia de vellosidades coriónicas; estos métodos permiten hacer diagnósticos más tempranos que la concentración de la 17 OHP en líquido amniótico25-26.
Un nuevo método utilizado es la reacción en cadena de la polimerasa de alelos específicos27 con la ventaja de que disminuye el tiempo requerido para el diagnóstico.
La ecografía de tercer nivel puede sugerir el diagnóstico mediante identificación de vagina y útero en un feto con genitales externos masculinizados14.
Tratamiento
El principio del tratamiento médico para la deficiencia de la 21 OHasa incluye reemplazo de la producción de cortisol, la cual suprime el incremento de la secreción de la ACTH en todas las formas clínicas y remplazo en la deficiencia de aldosterona en pacientes con pérdida de sal1, la terapia con glucorticoide es necesaria para una homeostasis normal de energía y glucosa; para prevenir los signos y síntomas del exceso de andrógenos y promover un normal crecimiento, maduración sexual y mantener una adecuada fertilidad1,14. Schwitzgebel VM, y cols describieron 4 casos de embarazos en pacientes con hiperplasia suprarrenal congénita clásica las cuales fueron tratadas desde el nacimiento con corticoides28. En pacientes con pérdida de sal un remplazo de análogos de mineralocorticoides es necesario para mantener un adecuado balance hidroelectrolítico con una presión arterial normal1,7. El tratamiento también debe incluir un adecuado aporte de sal7. Para niños y adolescentes los glucorticoides recomendados son la hidrocortisona a dosis de 8-12 mg/m2 al día dividido en 2 a 3 dosis o fludrocortisona 0.05 _ 0.15 mgs1.
Al final de la adolescencia y edad adulta los corticoides recomendados son prednisona a dosis de 6 mg/m2/día o la fludrocortisona 0.05-0.2 mg. Este último por ser un análogo mineralocorticoide sólo se usa para la forma perdedora de sal1. La dexametasona también puede ser utilizada a la dosis de 0.6 mg por metro cuadrado14. La terapia con glucorticoides en algunas mujeres no obstante no es satisfactoria para eliminar el hirsutismo. El tratamiento con glucorticoides mas análogos de GnRH, acetato de ciproterona, o anticonceptivos orales combinados de etinilestradiol con acetato de ciproterona o clormadinona puede ser más efectivo en estos casos29. En general todos los anticonceptivos orales tienen utilidad ya que estos aumentan la globulina transportadora disminuyendo los niveles de andrógenos libres, sin embargo se prefieren los compuestos con acetato de ciproterona o clormadinona.
El monitoreo terapéutico requiere evaluación de la velocidad de crecimiento, ganancia de peso, cambios en la edad ósea, presencia o ausencia del vello sexual y agrandamiento del pene o clítoris, como también del nivel de 17 OHP, androstenodiona y testosterona o de sus metabolitos urinarios1.
El tratamiento debe suprimir las concentraciones de 17 OHP a un nivel de 300 a 900 ngr/dl8. En mujeres adultas se recomienda la valoración periódica de Cortisol sérico para evitar la sobresupresión y se debe mantener en concentración menor o igual a 2 microgr/dl3.
También se han utilizado la flutamida, un antiandrógeno y la testolactona, un inhibidor de la conversión de estrógeno a andrógeno, pero faltan más estudios que respalden su uso6.
Finalmente las niñas con genitales ambiguos pueden requerir cirugía reconstructiva; los objetivos son reconstruir el periné, el introito, la separación de vagina, uretra y clítoris y la reducción de éste a un tamaño apropiado a expensas de sus cuerpos cavernosos y conservando su glande. La edad adecuada para la corrección quirúrgica es aún motivo de controversia, debe hacerse antes de que la niña se vea a sí misma o sea vista por otras personas como anormal8,14.
Tratamiento Prenatal
El tratamiento prenatal es realizado con la administración temprana de dexametasona a la madre1, 13, 25. La dexametasona diferente al cortisol o prednisona atraviesa la placenta en una forma activa, biológicamente lo que causa supresión de la ACTH adrenal y supresión de la producción de andrógenos13.
La dosis es de 20 microgramos por kilogramo de peso 2 a 3 veces al día, es decir, entre 1 a 1.5 mg/día1, 3, 7, 13, 25. Como la diferenciación de los genitales externos comienza a partir de la semana 7 de gestación, el tratamiento debe comenzarse desde la cuarta semana o a más tardar, antes de la semana 7 de gestación1, 26. La eficiencia es del 86%, básicamente evitando la virilización cuando se usa antes de este periodo1. Un criterio enérgico y aún motivo de controversia consiste en empezar tratamiento en todas las mujeres embarazadas con riesgo de tener un hijo con HSC; éste se administra tan pronto como se reconoce el embarazo y si el feto es varón se interrumpe la administración de dexametasona, y si es mujer, se efectúa análisis del DNA para identificar el gen de la 21 OH; si el feto no está afectado se interrumpe el tratamiento3. Durante el parto puede necesitarse aumentar la dosis especialmente si se va a someter la paciente a una cesárea; se recomienda en la mañana de la cirugía administrar 400 mg de hidrocortisona o su equivalente y posteriormente retornar a la dosis usual.
Los efectos maternos indeseables de la dexametasona incluyen exceso de ganancia de peso, fascies de cushing, estrías permanentes, intolerancia a la glucosa o diabetes mellitus franca, hipertensión, labilidad emocional, dolor epigástrico y edemas1,25,30. En humanos no se ha documentado ningún efecto teratogénico con el uso de dexametasona sin embargo, el uso de corticoides en animales durante el embarazo se ha asociado con disminución de la circunferencia cefálica y disminución en el peso de la glándula suprarrenal placenta y peso fetal15,25.
Deficiencia de 3 beta hidroxiesteroide deshidrogenasa/ delta 5-delta 4 isomerasa
La 3 beta OHeDHasa cataliza la conversión del delta 5-3 beta hidroxiesteroide a delta 4-3 beta cetosteroide en las glándulas adrenales y en las gónadas así como también en otros tejidos extra adrenales y extragonadales1. Está impedido el paso de pregnenolona a progesterona (P) de 17 hidroxipregnenolona a 17 hidroxiprogesterona y de deshidroepiandrosterona (DHEA) a androstenodiona1,13-14.
La deficiencia de 3 beta OHeDHasa en la corteza adrenal resulta en deficiencia de Cortisol con o sin deficiencia de Aldosterona e incremento de la secreción de ACTH resultando en incremento de la producción de precursores esteroides delta 5 como la pregnenolona, 17 hidroxipregnenolona (delta 5-17 P) y androstenodiol31.
La deficiencia severa de 3 beta OHeDHasa causa pérdida de sal y genitales ambiguos en niños por no tener progesterona1,14, y causa pérdida de sal, y genitales normales o ligeramente virilizados en niñas por exceso de andrógenos1,14. Muchos pacientes no sobrepasan la infancia temprana.
La forma leve de 3 beta OHeDHasa en hombres adultos causa varios grados de hipogonadismo y en mujeres resulta en hirsutismo, desórdenes menstruales y síndrome de ovario poliquístico1,12-13.
Los genes que codifican esta enzima están en el cromosoma Ip en la región 11 a 13 y se heredan de manera autosómica recesiva1,8.
Diagnóstico
El diagnóstico se hace con la medición del nivel de delta 5-17 P y DHEA y relación delta 5-17 P/ 17 OHP y delta 5-17 P/ cortisol o DHEA/ androstenodiona1.
La testosterona y la androstenodiona son normales o ligeramente elevadas3. Después de la administración endovenosa de una dosis rápida de 0.25 mgr de ACTH la Delta 5-17P se incrementa en grado importante en un plazo de 60 minutos3. La cifra normal de delta 5-17 P es de 1050 ngr/dl3.
Tratamiento
Administración de glucocorticoides y mineralocorticoides14. Durante la pubertad pueden necesitarse esteroides sexuales para inducir un desarrollo adecuado de los caracteres sexuales secundarios; las niñas que tuvieron virilización in útero pueden necesitar posteriormente correcciones quirúrgicas de genitales externos.
Deficiencia de 17 alfa OHasa
La 17 alfa OHasa es necesaria para la conversión de pregnenolona en 17 hidroxipregnenolona y de progesterona en 17 OHP14.
La deficiencia conduce a disminución de Cortisol, testosterona y estradiol pero no de Aldosterona; por el contrario, toda la línea mineralocorticoides se aumenta, concentrándose
en un incremento de DOCA que conduce a un aumento del intercambio de sodio por potasio en el túbulo distal, retención de sodio, expansión del volumen plasmático, supresión de la renina plasmática e hipokalemia; por lo tanto, no hay pérdida de sal y puede producir hipertensión13-14. Los genitales externos son normales en mujeres, pero puede haber falla en la adrenarquia y pubarquia13,14, y causa pseudohermafroditismo masculino13-14. La conversión enzimática está codificada en el cromosoma 1013.
El diagnóstico se hace por disminución de 17 hidroxiprogesterona13 y concentración urinaria disminuida de 17 hidroxiesteroide y 17 cetosteroide y las concentraciones de DOCA y corticosterona están aumentadas al realizar estimulación con ACTH13.
El tratamiento se hace con glucocorticoides, que conducen a una supresión rápida del exceso de DOCA. En la pubertad se requiere administrar testosterona en los pacientes masculinos y estrógenos en los femeninos.
Deficiencia de 11 beta hidroxilasa
La forma clásica de la deficiencia de la 11 OHasa produce del 5-8% de los casos de HSC8; aproximadamente un caso en 100.000 nacidos vivos15.
La deficiencia de esta enzima impide el paso de DOCA a corticosterona y de desoxicortisol a Cortisol. Los genes de esta enzima el CYP 11B1 y el CYP 11B2 están localizados en la parte media del brazo largo del cromosoma 83,13 y se hereda de una forma autosómica recesiva15. Debido a esto hay disminución de la corticosterona y el Cortisol por lo tanto la acumulación de DOCA desoxicortisol y andrógenos. Estos pacientes presentan hipertensión, hipokalemia y supresión de la renina plasmática13,14. Puede haber cardiomiopatía y retinopatía relacionadas3.
Los fetos femeninos tienen genitales externos masculinizados e internos normales14. Después del nacimiento hay un crecimiento somático rápido, aparece clítoromegalia, hirsutismo, acné y maduración epifisiaria temprana14.
En la deficiencia leve las pacientes manifiestan hirsutismo, acné y amenorrea3.
El diagnóstico se confirma por la determinación del metabolito urinario de 11 desoxicortisol (Tetra hidrodesoxicortisol) y el de la DOCA (tetrahidro DOCA) pero sería preferible la determinación en el plasma de 11 desoxicortisol y de DOCA14.
El diagnóstico prenatal se puede realizar midiendo niveles de 11 desoxicortisol en líquido amniótico y 11 desoxicortisol en orina materna; igualmente puede realizarse por diagnóstico genético molecular32. El diagnóstico de hiperplasia suprarrenal de iniciación tardía se establece cuando las concentraciones de 11 desoxicortisol pasan de 25 ngr/ml 60 minutos después de la administración de ACTH3. El tratamiento se hace con glucocorticoides como en las formas anteriores13.
Deficiencia de 20 hidroxilasa
Es una condición muy rara de ocurrencia14, compromete el paso de colesterol a pregnenolona y la síntesis de los 3 tipos de esteroides suprarrenales lo que lleva a un acúmulo de grandes cantidades de colesterol y ésteres de colesterol que se ve en la glándula como células corticales repletas de material lipoide por lo que se denomina hiperplasia suprarrenal lipoide14.
Hay ausencia de genitales externos masculinos; las mujeres afectadas tienen desarrollo genital normal, la falta de mineralocorticoides conduce a pérdida severa de sodio, hipovolemia e hipotensión14. La mayoría de los pacientes no sobrepasa la infancia temprana14.
Deficiencia de 18 hidroxiesteroide deshidrogenasa.
Este bloqueo sólo compromete la producción de Aldosterona lo que produce pérdida de sodio hiponatremia, hiperkalemia y deshidratación14. El Cortisol se produce en cantidades normales y por lo tanto la ACTH no está aumentada14. Los esteroides sexuales también se producen normalmente por lo cual estas pacientes no presentan virilización o mal diferenciación sexual14.
Finalmente también pueden estar comprometidas otras enzimas como la 18 hidroxilasa y 17, 20 desmolasa14.
Conclusión
La hiperplasia adrenal congénita se debe descartar en todo recién nacido con ambigüedad sexual. Lo ideal de esta patología es que se tenga en cuenta en la evaluación preconcepcional, que su diagnóstico se haga a nivel prenatal en épocas tempranas del embarazo para un adecuado tratamiento y evitar todas las complicaciones que esta enfermedad conlleva. También debe ser tenida en cuenta en la edad adulta como diagnóstico diferencial en hiperandrogenismo y como causa de anovulación con su consecuente infertilidad.
Bibliografía
1. Pang S. Congenital adrenal hyperplasia. Endocrinology and Metabolism Clinics 1997; 26: 853-91.
2. Bose HS, Sugawara T, Strauss JF, et al. The pathophysiology and genetics of congenital lipoid adrenal hyperplasia. N. Engl J Med 1996; 335: 1870-8.
3. Hershlag A. Peterson CM. Trastornos Endocrinos. In: Berek JS, Hillard PA, Adashi EY. Ginecología de Novak. 12 Ed. Mc Graw-Hill. Interamericana. México 1997; 849-52.
4. Swerdlow AJ, Higgins CD, Brook CG, et al. Mortality in patients with congenital adrenal hyperplasia: A cohort study. Journal of Pediatrics 1998; 133: 516-20.
5. Pang S. Congenital adrenal hyperplasia. In Serono Symposia: Current Review of Pediatric Endocrinology, Washington, D.C., 1993; 101.
6. Merke DP, Cutler GB. New approaches to the treatment of congenital adrenal hyperplasia. JAMA 1997; 277: 1073-6.
7. Speiser PW, New MI. Diagnóstico y tratamiento prenatales de la hiperplasia suprarrenal congénita. In: Koren G. Ito S. Clínicas de perinatología. Mac Graw-Hill. Interamericana. México 1994; 3: 639-53.
8. Rebar RW. Pubertad. In: Berek JS, Hillard PA, Adashi EY. Ginecología de Novak. 12 Ed. Mac Graw-Hill. Interamericana. México 1997; 796-9.
9. Therrell BL, Berenbaum SA, et al. Results of Screening 1.9 million Texas Newborns for 21-Hydroxylase deficient congenital adrenal hyperplasia. Pediatrics 1998; 101: 583-90.
10. Nader S. Other endocrine disorders of pregnancy. In: Creasy RK, Resnik R. Maternal fetal medicine. Principles and practice W. B. Saunders. Company. Philadelphia. 3ra ed. 1994; 1017-8.
11. Azziz R, Dewailly D, Owerbach D. Clinical review 56: Nonclassic adrenal hyperplasia. Current concepts. J Clin Endocrinol Metab 1994; 78: 810-5.
12. Eldar-Geva T, Hurwitz A, Vecsei P, et al. Secondary biosynthetic defects in women with late-onset congenital adrenal hyperplasia. N Engl J Med 1990; 323: 855.
13. Miller WL. Pathophysiology, genetics, and treatment of hyperandrogenism. Pediatric Clinics of North America 1997; 44: 375-95.
14. Henao G. Hiperplasia Suprarrenal. In: Botero J, Jubiz A, Henao G. Obstetricia y Ginecología 5ª Ed. Editorial Carvajal S.A. Medellín Colombia 1997; 414-19.
15. Sperof L, Glass RH, Kase NG. Clinical gynecologic endocrinology and infertility. Sixth ed. Lippincott Williams E Wilkins, 1999 United States of America. 349-56.
16. Hawkins LA, Chasalow FI, Blethen SL. The role of adrenocorticotropin testing in evaluating girls with premature adrenarche and hirsutism /oligomenorrhea. J Clin Endocrinol Metab 1992; 74: 248.
17. Feldman S, Billaud L Thalabard J, et al. Fertility in women with late-onset adrenal hyperplasia due to 21-hydroxylase deficiency. J Clin Endocrinol Metab 1992; 74: 635.
18. Ravichandran R, Lafferty F, McGinniss MJ, Taylor HC. Congenital adrenal hyperplasia presenting as massive adrenal incidentalomas in the sixth decade of life: Report of two patients with 21-Hydroxylase deficiency. J Clin Endocrinol Metab 1996; 81: 1776-9.
19. Cook DM. Diagnostic Evaluation Update Adrenal Mass. Endocrinolgy and Metabolism Clinics, 1997; 26: 829-52.
20. Barzon L, Scaroni C, Sonino N, Fallo F, Gregianin M, Macri C, Boscaro M. Incidentally discovered adrenal tumors: Endocrine and scintigraphic correlates. J Clin Endocrinol Metab 1998; 83: 55-62.
21. Jaresch S, Kornely E, Kley HK, Schlaghecke R. Adrenal incidentaloma and patients with homozygous or heterozygous congenital adrenal hyperplasia. J Clin Endocrinol Metab 1992; 74: 685-9.
22. Allen DB, Hoffman GL, Fitzpatrick P, et al. Improved precision of newborn screening for congenital adrenal hyperplasia using weight-adjusted criteria for 17-hydroxyprogesterone levels. J Pediatr 1997; 130: 128-33.
23. Rueda González R, Rueda Sáenz R. Guías diagnósticas en infertilidad. Cali Colombia, 1987; 123-4.
24. Avivi I, Pollack S, Gideoni O, Linn S, Blumenfeld Z. Overdiagnosis of 21-hydroxylase late onset congenital adrenal hyperplasia: correlation of corticotropin tets and human leukocyte antigen typing. Fertility and sterility, 1996; 66: 557-63.
25. Mercado AB, Wilson RC, Cheng KC, et al. extensive personal experience. Prenatal treatment and diagnosis of congenital adrenal hyperplasia owing to steroid 21 hydroxylase deficiency. J Clin Endocrinol Metab 1995; 80: 2014-20.
26. Levine LS, Pang S. Prenatal diagnosis and treatment of congenital adrenal hyperplasia. J Pediatr Endocrinol 1994; 3: 193.
27. Wilson RC, Wei JQ, Cheng KC, Mercado AB, New MI. Rapid DNA analysis by allele specific PCR for detection of mutations in the steroid 21-hydroxylase gene. J Clin Endocrinol Metab 1995; 80: 1635-40.
28. Schwitzgebel VM. Tyrrell JB, Fitzgerald P, Kaplan SL. Normal females infants born of mothers with classic congenital adrenal hyperplasia due to 21- Hydroxylase deficiency, J Clin. Endocrinol Metab 1999; 84: 930-6.
29. Carmina E, Lobo RA. Ovarian suppression reduces clinical and endocrine expression of late-onset congenital adrenal hyperplasia due to 21 hydroxylase deficiency. Fertility and sterility 1994; 62: 738-43.
30. Pang S, Clark AT, Freeman LC, Dolan LM, et al. Maternal side effects of prenatal dexamethasone therapy for fetal congenital adrenal hyperplasia. J Clin Endocrinol Metab 1992; 75: 249-53.
31. Azziz R, Bradley Jr EL, Potter HD, Boots LR. 3 B-hydroxysteroid dehydrogenase deficiency in hyperandrogenism. Am J Obstet Gynecol 1993; 168: 889.
32. Rosler A, Weshler N, Leiberman F, Hochberg Z, Weidenfeld J, Sack J, Chemke J. 11 B- hidroxilase deficiency congenital adrenal diagnosis. J Clin Endocrinol Metab 1988; 66: 830.
*Jáner Sepúlveda Agudelo MD. Especialista en Ginecología y Obstetricia. Profesor de cátedra Universidad Industrial de Santander.,
**Lucy Sanguino Abril Bacterióloga y laboratorista clínica. Universidad Industrial de Santander.,
***Hermes Jaimes Carvajal MD. Especialista en Ginecología y Obstetricia. Jefe Unidad de Medicina Reproductiva. Departamento de Ginecología y Obstetricia. Universidad Industrial de Santander. Bucaramanga.
Recibido Febrero 2/2001 – Revisado: Mayo 23/2001 – Aceptado: Noviembre 26/2001
CLIC AQUÍ Y DÉJANOS TU COMENTARIO