El Síndrome de Lambert-Eaton: Fisiopatogenia de la Unidad Neuromuscular
Fisiopatogenia de la Unidad Neuromuscular
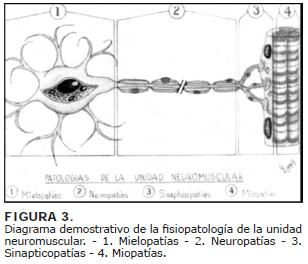
Guerrero Figueroa R. (5) clasifica las enfermedades de la unidad neuromuscular con base en un concepto fisiológico (Fig.3) que depende de la motoneurona alfa. Su axón con todas sus ramas terminales y todas las fibras musculares que inerva el axón.
La motoneurona constituye el origen de una vía final común a través de la cual se transmiten todos los impulsos a la musculatura esquelética.
Esta clasificación facilita la diferenciación entre las enfermedades de la unidad neuromuscular con las del SNC que afectan principalmente la medula espinal, el cerebro o ambos. El síndrome miasténico de Lambert-Eaton es considerado como una sinapticopatía presináptica.
En esta enfermedad la insuficiencia de la transmisión neuromuscular se debe a la liberación de un número insuficiente de cuantas de acetilcolina a partir de la terminal nerviosa por cada impulso nervioso (6-8). Estudios clínicos y experimentales han demostrado que la insuficiencia en la liberacióndel neurotransmisor se debe a un bloqueo mediado por anticuerpos. En determinadas subunidades proteicas o canales para Ca2+ localizados a nivel de los terminales axonales de la motoneurona (9-11).
Por otra parte se ha considerado en síndrome de LEMS como una enfermedad autoinmune. Con la existencia de un anticuerpo monoclonal que tiene la función homóloga con la sinaptotagmina de la membrana de vesícula sinápticas y con propiedades químicas similares a la inmunoglobulina (lgG) de los pacientes con LEMS (12-15). Sin embargo, y muy a pesar de un gran número de trabajos realizados con la sinaptotagmina, todavía no está definida la relación que existe entre ésta y la vía de ca2+ (16-18).
Lea También: El Síndrome de Lambert-Eaton: Materiales y Métodos
Recuento Neurofisiológico
Hasta el momento actual es necesario efectuar estudios electrofisiológicos para lograr hacer el diagnóstico del síndrome de LEMS. Los resultados de otros estudios básicos de laboratorio, incluidos los enzimas moleculares, son normales y no se han identificados marcadores séricos específicos.
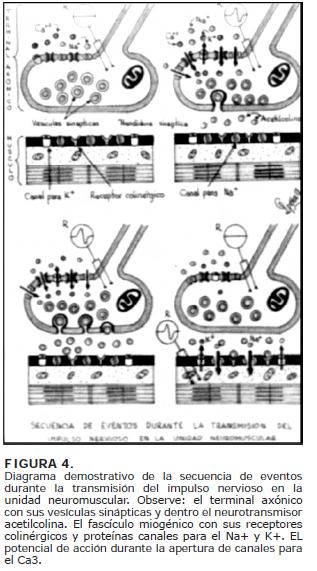
Estudios neurofisiológicos realizados en la unidad neuromuscular de una persona normal son demostrativos de potenciales evocados elicitados por un estímulo umbral. Guardando relación en la amplitud de voltaje entre el registro presináptico axonal y el registro postsináptico obtenido a nivel de la fibra miogénica (Fig.4).
En cambio, un análisis de registros obtenidos por Elqvist and Lambert (19689 (6) en la unidad neuromuscular de un paciente con diagnóstico de síndrome miasténico asociado con carcinoma broncogénico. Fueron demostrativos de potencial de acción postsináptico con amplitud anormalmente baja, comparada con el potencial de acción presináptico.
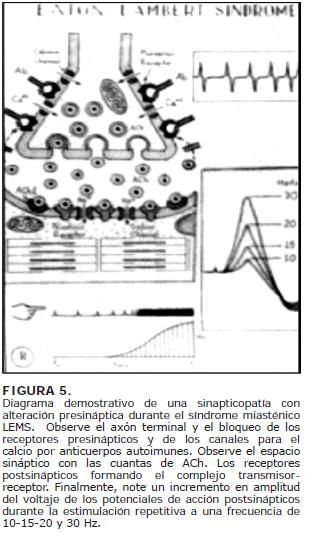
La estimulación repetida a razón de 2-3Hz hace evidente la existencia de un defecto en la transmisión neuromuscular. Fue postulada por los autores como una insuficiencia en la liberación cuántica de acetilcolina y proporcionó la primera identificación que el mecanismo patógeno del LEMS. Comprende un deterioro de la entrada del ca2+ a nivel de las terminales axonales motoras (fig.5).
Sin embargo, a niveles de unos 10 a 50 Hz hay un notable incremento de la amplitud de la respuesta evocada postsináptica (2 a 20 veces el calor original).
Resultados electrofisiológicos
Estos resultados electrofisiológicos nos conducen a investigar la existencia de un mecanismo más complejo, envuelto en la entrada del Ca2+, y consiste:
- En el síndrome de LEMS la estimulación de bajafrecuencia y esporádica de 1 a 3 Hz. Induce un bloqueo parcial de algunas subunidades especificas que regulan la entrada rápida del Ca2+. En el terminal axonal presináptico, sin modificar o alterar la función fisiológica de otras subunidades que son responsable por la entrada lenta del Ca2+ al axón terminal. Permitiendo la liberación cuántica de Ach a la hendidura sináptica y como causa de la persistencia del potencial en miniatura (MEPP) o ruido transináptico,
- La alteración o bloqueo parcial de subunidades para el Ca2+ hace que el contenido cuántico medio de Ach liberado al espacio sináptico. Durante la estimulación a baja frecuencia, sea menor y como consecuencia la reducción ligera en la amplitud del potencial de acción postsináptico, y
- La estimulación a frecuencia por encima de 5 a 50 Hz además activa el bloqueo de receptores presinápticos a nivel de las terminales axonales impidiendo el mecanismo básico de recaptación del neurotransmisor. Y como resultado, una mayor cantidad de Ach en el espacio sináptico que induce el incremento en la amplitud del voltaje del potencial postsináptico miogénico.
CLIC AQUÍ Y DÉJANOS TU COMENTARIO