Tumor mixto maligno en conducto auditivo externo (CAE)
Presentación de un caso y revisión de literatura
Malign mixed tumor in external ear canal (EAC).
Case Presentation and literature review
Juan León I., M.D. *; Ernesto Ried G., M.D.**;
Iván Gallegos M., M.D.***; Andrés Ortega T., M.D.**
* Médico Residente de Otorrinolaringología de la Universidad de Santiago de Chile – Hospital Clínico de la Fuerza Aérea de Chile.
** Médicos Otorrinolaringólogos del Hospital Clínico de la Fuerza Aérea de Chile.
*** Médico Patólogo del Hospital Clínico de la Fuerza Aérea de Chile.
Resumen
Se presenta un caso de siringoma condroide maligno en una paciente con una masa a nivel de CAE izquierdo y cuyo cuadro clínico se caracterizó por una oclusión total del lumen del conducto asociado a secreción purulenta y líquido serohemático. La escisión es la forma de tratamiento. Este tipo de expresión tumoral es infrecuente y corresponde a un tumor mixto de la piel que incluye elementos glandulares sudoríparos (siringoma) y tejido conectivo tipo cartilaginoso (condroide), por lo tanto es un tumor epitelial derivado de glándulas ecrinas o apocrinas con cambios secundarios en el estroma, presentando además una similitud histológica con el adenoma pleomorfo en glándulas salivales.
Palabras clave: Tumor mixto; siringoma condroide; adenoma pleomorfo; oído.
Introducción
El siringoma condroide es un tumor benigno poco habitual que se distingue por una proliferación epitelial tubular ecrina o apocrina similar al de una glándula sudorípara asociada a una matriz estromal cartilaginosa. Esta asociación es la que lo caracteriza y se le denomina “Tumor Mixto”, presentando desde el punto de vista histológico una marcada semejanza con el adenoma pleomorfo de las glándulas salivales (1).
El término de tumor mixto se comenzó a emplear a partir del siglo XIX al encontrar en glándulas parótidas tumores que presentaban una combinación de células dentro de una matriz con rasgos epiteliales y mesenquimales (1,2).
De acuerdo a la literatura estos tumores son bastante complejos por la capacidad de diferenciación que poseen las células mioepiteliales en distintas líneas celulares adoptando formas escamosas, condroides, plasmocitoides o elementos fusados (2).
Se localizan generalmente en cabeza y cuello. Según el sexo hay una mayor incidencia en la mujer que en el hombre y principalmente se presenta entre la 6ª y 7ª década de vida siendo una excepción en edades tempranas (menores de 20 años). Es de crecimiento lento y su tamaño varía entre 0,5 a 3 centímetros de diámetro, presentando un aspecto amarillento o eritematoso. Usualmente la lesión se aprecia costrosa y de fácil sangrado. Tiende a ser asintomático a no ser que se infecte (1,3,4).
El rasgo más notable y esencial para el diagnóstico del siringoma condroide a través del análisis histológico es la presencia de un estroma mucinoso. En la fase inicial del desarrollo, el estroma está compuesto de tejido conectivo que es azul alcalino conteniendo hialuronidasa positiva, mucopolisacárido ácido resistente y células fibroblásticas estrelladas que sella el carácter mixoide.
La patogénesis de la metamorfosis del estroma es controversial. Se especula que hay verdaderas metaplasias cartilaginosas y alteraciones de la matriz que son el resultado de las células mioepiteliales migratorias (1).
Son muy pocos los casos existentes de siringoma condroide maligno (3,4). La neoplasia tiende a producir metástasis en linfonodos regionales, pudiendo causar la muerte del paciente (4,5). El tratamiento de elección es el quirúrgico (escisión) y en ocasiones se complementa con radioterapia para evitar la colonización metastásica.
Material y Métodos
Mujer de 82 años con antecedentes previos de otitis media crónica bilateral operada a la edad de nueve años. En 1996 consulta por la presencia de un pequeño aumento de volumen a nivel de CAE izquierdo; en aquella oportunidad se efectuó una biopsia lo que dio como resultado un hidroadenoma.
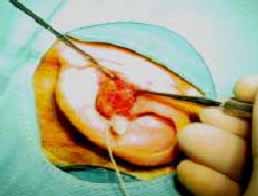
La paciente vuelve a consultar después de siete años por un importante aumento en el tamaño del tumor, llegando a ocluir el lumen del conducto (Figura 1), acompañándose además de un proceso infeccioso e hipoacusia de conducción. Fue sometida a una cirugía, con liberación del tumor e identificación del pedículo, con posterior resección hasta el pericondrio, a nivel de la base de implantación de la lesión tumoral.
Se revisó cavidad la que se encontró sana. Se envió a estudio anatomopatológico en dos trozos, que al aspecto macroscópico eran sólidos, de aspecto nodular, con superficie de corte granular y de color grisáceo.
Figura 1. Tumor (Siringoma condroide maligno) a nivel del conducto auditivo externo izquierdo.
Se demostró al examen microscópico que corresponde a neoplasia no encapsulada, de bordes irregulares, compuestas por lóbulos de tejidos cartilaginosos mezclados íntimamente con elementos epiteliales (Figura 2). El componente cartilagíneo es de celularidad levemente aumentada, sin presentar atipías ni mitosis (Figura 3). El componente epitelial se dispone formando estructuras tubulares papilares irregulares y en brotes sólidos. Corresponde a células de tamaño grande, con poco citoplasma, núcleo aumentado de tamaño, con cromatina gruesa, en partes vesiculosas, con uno o más nucléolos y numerosas figuras mitóticas [hasta 10 en 10 campos de aumento seco mayor] (Figura 4). Hay áreas con necrosis central de tipo comedocarcinoma (Figuras 5 y 6). El tumor contacta la epidermis hacia sus extremos (Figura 7), formando una especie de invaginación periférica y presenta abundantes células plasmáticas como elementos inflamatorios asociados (Figura 8). Focalmente hay túbulos con células de núcleos más pequeños, sin atipías, mitosis y presentando diferenciación apocrina con decapitación de la zona apical de sus citoplasmas.
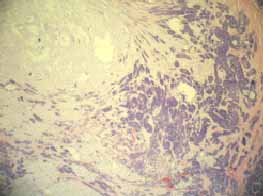
Figura 2. Tumor formado por lóbulos con centro de predominio cartilagíneo y elementos epiteliales hacia la periferia.
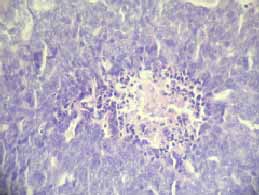
Figura 6. Se aprecia también múltiples focos de necrosis de tipo comedocarcinoma.
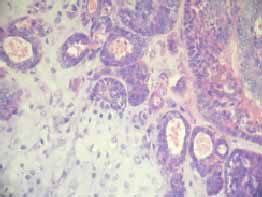
Figura 3. Cartílago de mayor celularidad y túbulos con diferenciación apocrina.
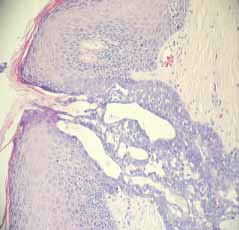
Figura 7. Hacia la izquierda se ve un tumor que presenta invaginación periférica y formación de papilas.
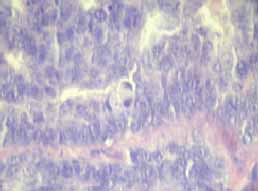
Figura 4. Células con núcleos grandes, de cromatina gruesa y numerosas mitosis.
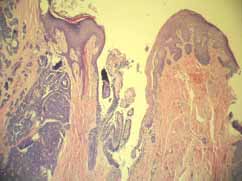
Figura 8. Focalmente la lesión cantacta la superficie epidérmica.
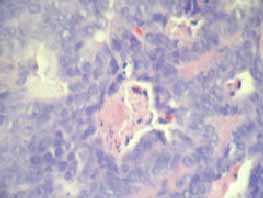
Figura 5. Focos múltiples de necrosis de tipo comedocarcinoma.
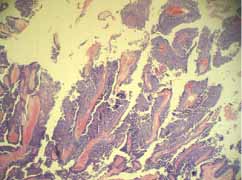
Figura 9. Evidente formación de papilas características del siringocistoadenoma papilífero.
Discusión
Damos a conocer este caso por lo infrecuente que es en su presentación clínica, aún más por su ubicación a nivel del CAE, como también por su histología. Concordamos ampliamente con lo que hemos encontrado en la literatura sobre sus rasgos clínicos, por ejemplo; su lento desarrollo, su carácter asintomático, de hallazgo más habitual en el sexo femenino, etc., pero también en relación a la diferenciación del tumor, ya que éste posee un carácter apocrino, de invaginación periférica contactando focalmente la epidermis, con formación de papilas y un infiltrado rico de células plasmáticas, todas ellas son características del “siringocistoadenoma papilífero” (Figura 9), pero con una clara diferenciación condroide, siendo esto una distinción del siringoma condroide, se concuerda también por su doble asociación, característica no poco habitual en este tipo de neoplasia.
La lesión es maligna por presentar pobre delimitación hacia los tejidos vecinos, elevado recuento mitótico y la formación de brotes sólidos con focos de necrosis central, todas las características descritas en la literatura como signos de malignidad del componente epitelial de estos tumores (1,3). Como hallazgo adicional se identifican áreas epiteliales que carecen de los signos de malignidad antes descritos que deben interpretarse como residuos del componente epitelial que explica la larga evolución del tumor. De acuerdo a este patrón mixto de diferenciación se deben tomar los elementos morfológicos presentes para poder denominarlo en forma correcta.
Conclusiones
· Desde el punto de vista clínico podemos concluir que este tipo de caso se presenta en forma muy aislada.
· Su diagnóstico es netamente histológico.
· Su tratamiento quirúrgico es diagnóstico y terapéutico, pudiéndose asociar la radioterapia cuando existe compromiso metastásico regional.
· La gran mayoría de los pacientes portadores de un tumor mixto maligno tienen buen pronóstico de vida posterior al tratamiento.
Abstract
A case of a malignant chondroid syringoma is presented here. It was found in a female patient with a mass in her left external auditive canal (EAC) and whose clinical feature was characterized by a total occlusion of the lumen of the canal associated with a purulent ear drainage and serumhematic liquid. Excision is the elective treatment. This kind of tumor expression is not frequent and it corresponds to a skin mixed tumor, including sweat glandular elements (syringoma) and connective tissue of the cartilaginous type (chondroid), therefore, it is an epithelial tumor derived from the eccrine or apocrine glands with secondary stroma changes, it also presents an histologic similarity to pleomorphic adenoma of the salivary glands.
Key words: Mixed tumor; Chondroid syringoma; Pleomorphic adenoma; Ear.
Correspondencia: Dr. E. Ried G. Félix de Amesti # 218 – LasCondes– Santiago de Chile
Email: eried@tutopia.com
Bibliografía
1. George F. Murphy, M.D.; David E. Elder, M.B.; Chondroid Syringoma. Atlas of Tumor Pathology. Non-Melanocytic Tumors of the Skin, 1990; (1) 74-78.
2. Kilpatrick, S.E.; Hitchcock, M.G; Kraus, M.D.; Kalonje, E.; Fletcher, C. Mixed Tumors and myoepitheliomas of soft tissues. A clinicopathologic study os 19 cases with a unifying concept. Am. J. Surg. Pathol, 1997; 21 (1) 13-22.
3. Requena, L.; Kiryu, H.; Ackerman, A.B. Neoplasms with apocrine differentiation Lippincott-Raven.ArdorSribendi.U.S.A. Chapter fourteen. Syringoadenomatosus papilliferus. 1997; Pages 665-675.
4. Schiano di Visconte M.; Picciano P.; Chondroid Syringoma. A case report. Chir Ital 2002 Mar-Apr; 54 (2): 241-4.
5. Maier T.; Autoptish gesichertes metastaserendes Schweissdrusenkarzinom auf dem Doden eines Naevus syringoademomatosus papilliferus. Zentalbl all Pathol 1949; 85:377-380.
CLIC AQUÍ Y DÉJANOS TU COMENTARIO